孙熙宸
加好友
孙熙宸 2020-01-06
来源:中国生物技术网
DNA损伤修复通路(DNA damage response pathway,DDR)在维持细胞基因组稳定性中发挥重要作用。DNA损伤修复受到泛素化等蛋白质翻译后修饰的严格而精细的调控,其中,去泛素化酶通过两种主要方式参与到DNA损伤修复过程中:直接作用到损伤位点或者调控DNA损伤应答关键的因子。
鉴于DNA损伤应答调控的复杂性,鉴定新的参与到DNA损伤修复中的去泛素化酶,阐明其发挥作用的机制,有助于我们深入了解DDR修复的分子机制。
近日,北京大学生命科学学院郑晓峰教授研究组在 Cancer Research 杂志在线发表题为:The Deubiquitinase USP38 Promotes NHEJ Repair through Regulation of HDAC1 Activity and Regulates Cancer Cell Response to Genotoxic Insults 的研究论文。

该研究鉴定了一个在DNA损伤应答中发挥作用的新的去泛素化酶USP38。发现USP38通过去除去乙酰化酶HDAC1的泛素化修饰来抑制HDAC1的去乙酰化酶活性,进而调控DNA双链断裂主要修复途径之一的非同源末端连接修复(NHEJ)的修复效率,在细胞基因组稳定性维持中发挥重要作用。该研究揭示了去泛素化酶参与调控DNA损伤调控的新机制。
该研究通过激光微辐射和中彗星实验发现,去泛素化酶USP38能够被募集到DNA损伤位点,在细胞基因组稳定性的调控中至关重要。进一步研究发现,USP38可以去除去乙酰化酶HDAC1的K63位连接的多聚泛素化修饰,进而上调HDAC1的去乙酰化酶活性,去除H3K56的乙酰化修饰,提高NHEJ的修复效率。生信分析和免疫组化的研究结果表明,USP38在大多数种类肿瘤中具有低表达的现象。在肾癌细胞系和小鼠中,USP38的缺失都会导致基因组的不稳定性,并且导致细胞和小鼠对于DNA损伤刺激更为敏感。与野生型小鼠的高存活相反,USP38-/-小鼠在IR照射后20天内全部死亡,进一步证明USP38对于维持细胞的损伤修复效率和基因组稳定性是至关重要的。
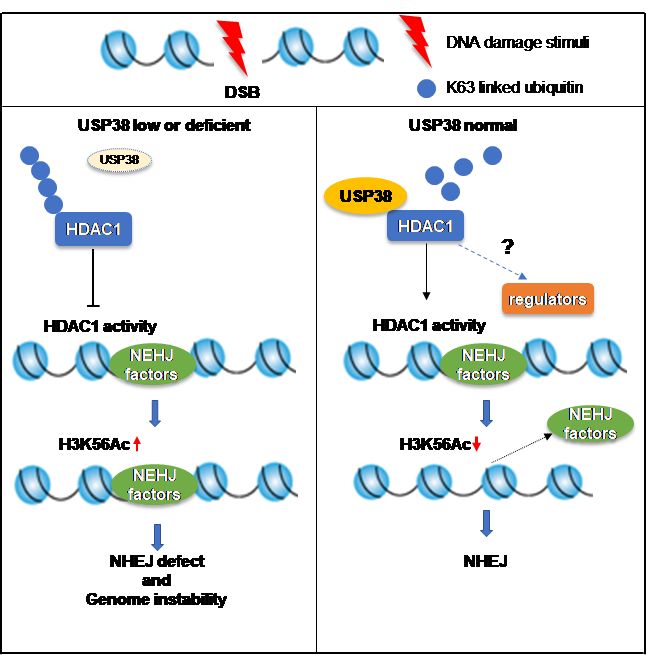
USP38通过调节HDAC1的泛素化修饰,及其去乙酰化酶活性调控NHEJ和基因组稳定性
总的来说,这项研究揭示了去泛素化酶USP38参与DNA损伤应答的机制,进一步明确了泛素化修饰和乙酰化修饰之间的作用关系,阐明了USP38在维持基因组稳定性和调节肿瘤细胞对于放化疗敏感性的机制。
来源:biotech-china 中国生物技术网
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5ODU5NDgyMg==&mid=2653946445&idx=4&sn=ebb9ce60ba64f59c3f52372eb6dbca2f&chksm=bd0cf2248a7b7b32e063b9f0abbaafe9cb0a3530ac95db581b3d5bcecd6cc0c2d2ff9bc9b124&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

小麦D基因组完整图谱首绘成功

昆明动物所等在基因组稳定性驱动的低氧适应研究中取得进展
遗传学:解密古埃及木乃伊基因组

乳腺癌有望实现精准治疗,科学家揭开基因组秘密

中国研究团队破解中国种茶树全基因组密码

Nature :酿酒酵母基因敲除库基因组结构与稳定性全分析

基因组不稳定性与乳腺癌发病有关
亚稳定性

华中农业大学教授赵书红:在基因组上“跳舞”

日本科研人员发现无呼吸微生物