科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2022-03-29
3月21日,Nature Metabolism在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)杨巍维研究组、赵允研究组,与上海交通大学附属胸科医院姚烽团队的合作完成研究成果(MAPK signalling-induced phosphorylation and subcellular translocation of PDHE1α promotes tumour immune evasion)。该研究揭示了丙酮酸脱氢酶PDHE1α亚细胞转位促进肿瘤免疫逃逸的功能及机制。
肺癌治疗颇具挑战。尽管针对免疫检查点的靶向治疗(抗PD-1治疗、抗PD-L1治疗等)在许多恶性肿瘤的治疗中展现出显著成效,且已在晚期肺癌的治疗中发挥重要作用,但并非所有PD-1阳性的肺癌患者都能从抗PD-1治疗中获益。解决肿瘤细胞对抗PD-1治疗的耐药性将具有重要的临床意义。
丙酮酸脱氢酶复合物在线粒体中催化丙酮酸转化为乙酰辅酶A、桥接糖酵解与三羧酸循环代谢。研究发现,丙酮酸脱氢酶复合物E1组分α亚基(PDHE1α)存在丰富的胞质定位;胞质PDHE1α通过促进磷脂酶PPM1B对IKKβ S177/181(IKKβ激活的关键磷酸化位点)的去磷酸化削弱了NF-κB信号通路的激活,增强了炎症因子及细胞毒性T淋巴细胞(CTLs)诱导的肿瘤细胞死亡。然而,MAPK等致癌信号(oncogenic signaling)的激活,导致胞质PDHE1α S327位点被ERK2磷酸化并转位到线粒体;胞质PDHE1α水平的下降恢复了NF-κB信号通路的活化;线粒体PDHE1α的增多提升了α-酮戊二酸的含量,并促进了炎症因子刺激下肿瘤细胞的ROS解毒。NF-κB的活化和ROS的清除共同促进肿瘤细胞在炎症因子刺激下的存活,增强了肿瘤细胞对CTLs的耐受性,促进了肿瘤的免疫逃逸和抗PD-1治疗的耐药性。
此外,肺癌患者肿瘤组织中PDHE1α S327磷酸化水平与胞质PDHE1α水平、ERK2活性和NF-κB激活相关;胞质PDHE1α水平或PDHE1α S327磷酸化水平与肺癌患者的恶性程度和预后相关。
该研究发现了PDHE1α亚细胞转位在肿瘤免疫逃逸中的新功能,揭示了磷酸化调控PDHE1α亚细胞转位及PDHE1α亚细胞转位调控肿瘤免疫逃逸的新机制,提示了抑制PDHE1α的磷酸化可阻断肿瘤的免疫逃逸并提高肿瘤免疫治疗的疗效。
研究工作得到国家重点研发计划、国家自然科学基金、中科院、分子细胞卓越中心细胞生物学技术平台/化学生物学技术平台/动物实验技术平台等的支持。
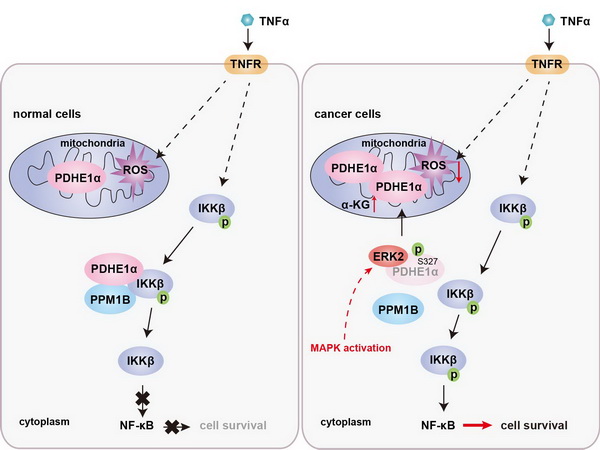
MAPK信号诱导的PDHE1α的磷酸化和转位促进肿瘤免疫逃逸
内容来源:中国科学院来源:中国科学院
原文链接:http://www.cas.cn/syky/202203/t20220324_4829301.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

磷酸化修饰组学揭示KRAS突变肿瘤的精准治疗新策略
科研人员开发出检测酪氨酸磷酸化新方法
中国抗癌协会肿瘤护理专业委员会在津成立



综述:生长素途径中的蛋白可逆磷酸化机制
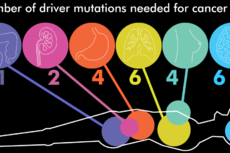
从健康细胞到癌细胞,或许只需要几个突变

Nat Biotech:“机器学习”帮助鉴定磷酸化位点
光合磷酸化作用

【大师讲堂】诺奖得主Edmond H. Fischer:磷酸化与去磷酸化调控的生物网络
蛋白质酪氨酸磷酸化的分子识别研究

化学小分子诱导靶标蛋白质去磷酸化