科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2023-04-12
3月24日,Nature Structural & Molecular Biology在线发表了中国科学院脑科学与智能技术卓越创新中心竺淑佳研究组撰写的题为Distinct structure and gating mechanism in diverse NMDA receptors with GluN2C and GluN2D subunits的研究论文。该研究结合单颗粒冷冻电镜、质脂体单通道记录、电压钳记录、分子动力学模拟、质谱分析、生化验证等多维度技术,揭示了含GluN2D亚基NMDA受体的门控机制和功能特征,诠释了含GluN2C亚基NMDA受体的不对称几何构象及特异性变构调节的机制。该研究为深度理解NMDA受体不同亚型的功能多样性及开发亚型选择性的小分子药物奠定了理论基础(图1)。
NMDA受体是介导大脑突触信号传递和突触可塑性的离子通道,参与并调控神经系统的发育、学习和记忆,同时,其功能异常与诸多神经或精神疾病的发生发展密切相关,是药物研发的重要靶点。哺乳动物大脑中的不同亚型NMDA受体,其表达分布和生物物理学性质具有多样性。含有GluN2A或GluN2B亚基的受体具有较高的通道开放概率和较低的激动剂亲和力。相反,含有GluN2C或GluN2D亚基的受体具有较低的通道开放概率和较高的激动剂亲和力。然而,决定这些功能多样性的分子基础知之甚少。
GluN2D富集表达于下丘脑、杏仁核等与情绪调节密切相关的脑区。竺淑佳研究组发现,GluN1-N2D受体具有一个比其他亚型更闭合的氨基端结构域,从而使它具有较低的通道开放概率。竞争性拮抗剂R-CPP能够通过撑开谷氨酸结合口袋,进而抑制离子通道的开放。GluN1上的可变剪接5号外显子可以使激动剂结合结构域扭转,从而提高离子通道的开放活性。鉴于GluN1-N2D受体的离子通道开放概率与GluN1-N2A受体相差50倍,研究基于结构在相互作用交界面引入一对二硫键,发现交联显著性地提高了GluN1-N2D受体的通道活性(图2a-d)。上述成果揭示了GluN1-N2D亚型的门控机制以及决定其生物物理特征的分子基础。
研究进一步发现,GluN1-N2C受体采取了与经典NMDA受体所不同的特殊非对称构象。该特性决定了小分子药物PYD-106只能结合相同基因编码的两个GluN2C中的一个亚基(图2e、f)。此外,研究还解析了在小脑颗粒细胞中高表达的GluN1-N2A-N2C受体的结构。进一步分析发现,GluN1-N2A-N2C受体中的GluN2A和GluN2C亚基分别整合了对应二异四聚体中的一个单体构象(图2g)。该研究首次揭示了GluN1-N2C受体的特殊非对称几何学特性,阐释了小分子PYD-106选择性作用于GluN1-N2C受体的机制。
研究工作得到科技部、国家自然科学基金委员会、中科院、上海市科学技术委员会的支持。
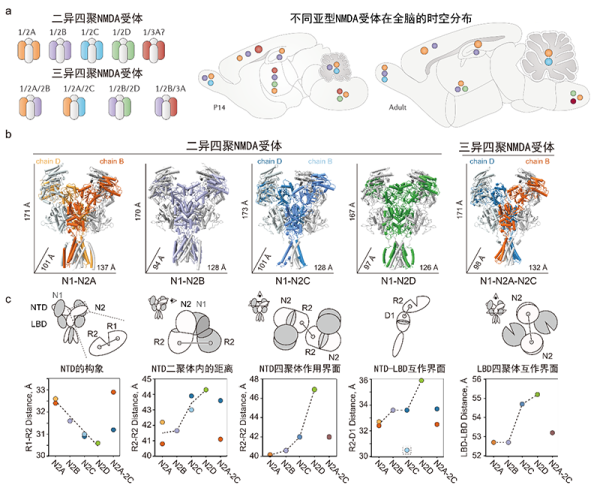
图1.决定不同NMDA受体功能多样性的分子基础。a、不同NMDA亚型在不同发育阶段的全脑分布(引自Paoletti et al., 2013);b-c、不同NMDA受体亚型的三维结构及决定功能多样性的结构基础。

图2.含有GluN2D和GluN2C受体的三维结构、门控机制和药理学特性。a、GluN1-N2D受体的三维结构;b、甘氨酸、谷氨酸和竞争性抑制剂R-CPP在其结合口袋中的电子密度云;c-d、GluN1E698C-N2D突变型受体在二硫键交联和非交联状态下的三维构象和单通道性质;e、GluN1-N2C受体的三维结构;f、GluN1-N2C受体的非对称性构象及选择性变构抑制剂PYD-106的结合口袋;g、GluN1-N2A-N2C受体的组装模式和拓扑结构。
来源:中国科学院
原文链接:http://www.cas.cn/syky/202304/t20230407_4883348.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
调控π-π堆积距离,获得16%效率的A-D-A型受体材料
【复材资讯】科学家首次实现陶瓷4D打印

重要! G蛋白偶联受体家族成员的结构解析

甲酰肽受体结构研究获进展
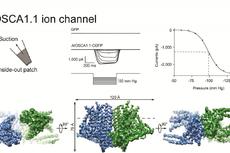
Nat Struct Mol Biol|新型机械力敏感的离子通道OSCA的鉴定、结构解析与机制研究

人体细胞内存在“铁路”系统,能自动优化结构

GABAB受体辅助亚结构单元KCTD对受体调控的结构和机制研究获进展

静电自组装法构建2D/3D Ni(OH)2/g-C3N4异质结构用于可见光产氢

上科大揭示首个卷曲受体三维结构

【复材资讯】形状记忆聚合物微纳米纤维膜在生物医学中的应用进展