科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-02-12
来源:BioArt植物
独脚金内酯 (strigolactones, SLs) 是近年来植物激素研究的热点之一,在植物分枝和生长发育中具有重要作用。SLs还可以作为根际信号分子,诱导丛枝菌根真菌(AMF)的菌丝分枝以及刺激有害寄生小草的种子萌发【1】。因此,了解植物中SLs的产生机制对农作物的产量形成以及减少寄生植物的危害至关重要。
SLs可以分为典型( canonical)SL和非典型(noncanonical)SL,典型SL包含一个三环内酯(ABC环)和一个由烯醇醚键连接在一起的单环内酯(D环),而非典型的SL具有未封闭的BC环。大多数典型SL的化学结构由4-脱氧邻苯二酚(4DO)和5-脱氧三醇(5DS)的衍生物组成,它们分别具有邻苯二酚型和strigol型SLs的最简单结构【2】。研究表明,SL的生物合成起始于类胡萝卜素异构酶DWARF 27 (D27)、类胡萝卜素裂解双加氧酶7 (CCD7) 以及CCD8,将trans-β-类胡萝卜素转化为中间体carlactone (CL)。之后,CL由more axillary growth 1 (MAX1) 编码的细胞色素P450单加氧酶CYP711A氧化生成CLA(carlactonoic acid),CLA再经进一步的反应生成SLs【3】,但是目前对SLs合成过程中的CLA的下游途径仍知之甚少。
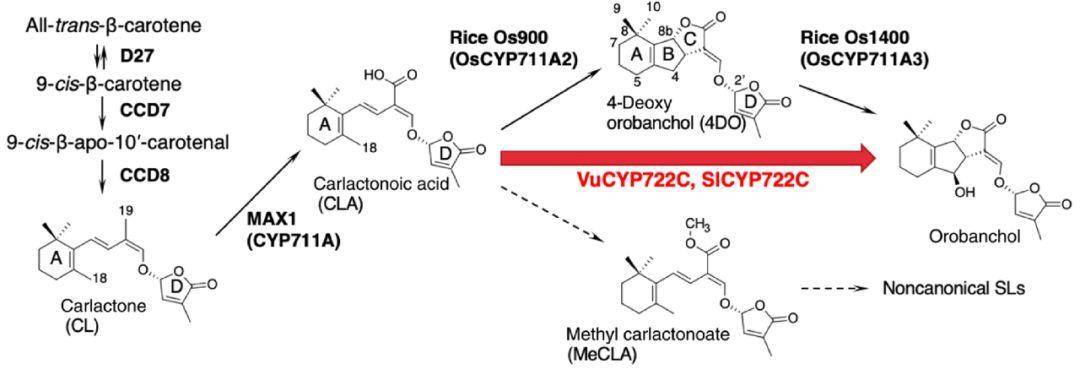
Proposed biosynthesis pathway of SLs
近日,日本Kobe University的Yukihiro Sugimoto课题组在Science Advances发表了一篇题为Direct conversion of carlactonoic acid to orobanchol by cytochrome P450 CYP722C in strigolactone biosynthesis 的研究论文,鉴定了一种新的催化CLA转化为经典SL的细胞色素P450单加氧酶。

之前研究表明,外源rac-CLA可被生物转化为邻苯二酚(一种典型SL)和orobanchyl acetate,并且在豇豆中这种生物转化被CYP抑制剂抑制,表明细胞色素P450 CYP参与将CLA向邻苯二酚的转化。该研究首先对豇豆VuMAX1的功能进行了表征,发现重组VuMAX1可以催化CL向CLA的转化,但是不能催化CLA向4DO或邻苯二酚的转化,这表明存在CYP711A之外的其他CYP负责将CLA转化为邻苯二酚。
该研究进一步通过在缺Pi营养液(缺Pi导致根分泌物中SL水平升高)中添加rac-GR24(合成的SL),发现SL水平增加(与预期的反馈调节相反),表明SL生物合成基因的上调。该研究进一步通过RNA-seq进行了共表达基因网络分析,从豇豆CCD8(VuCCD8)的转录模块中选择了未表征的CYP722C和CYP728B作为候选对象。同时,该研究表明VuCYP722C和VuCYP728B基因与SL生物合成基因共表达,表明这两个基因参与豇豆的SL生物合成。此外,该研究克隆了VuCYP722C和VuCYP728B并在昆虫细胞表达系统中进行了异源表达,发现重组VuCYP728B与rac -CLA 孵育未产生邻苯二酚,但是VuCYP722C可以。以上综合表明VuCYP722C是催化CL转化的潜在基因。
该研究还结合液质联用的结果提出了VuCYP722C催化反应的分子机理,即CLA中C-18位置的两步氧化生成18-oxo-CLA,然后通过BC环闭合反应继续产生邻苯二酚立体异构体。该研究还在番茄中通过CRISPR-Cas9技术表征了CYP722C的功能,该研究发现,SlCYP722C敲除(SlCYP722C -KO)的番茄根系分泌物中未检测到邻苯二酚但是有CLA的积累,而野生型的根系分泌物中未发现CLA,这进一步表明CYP722C通过催化BC环闭合反应从CLA合成邻苯二酚。
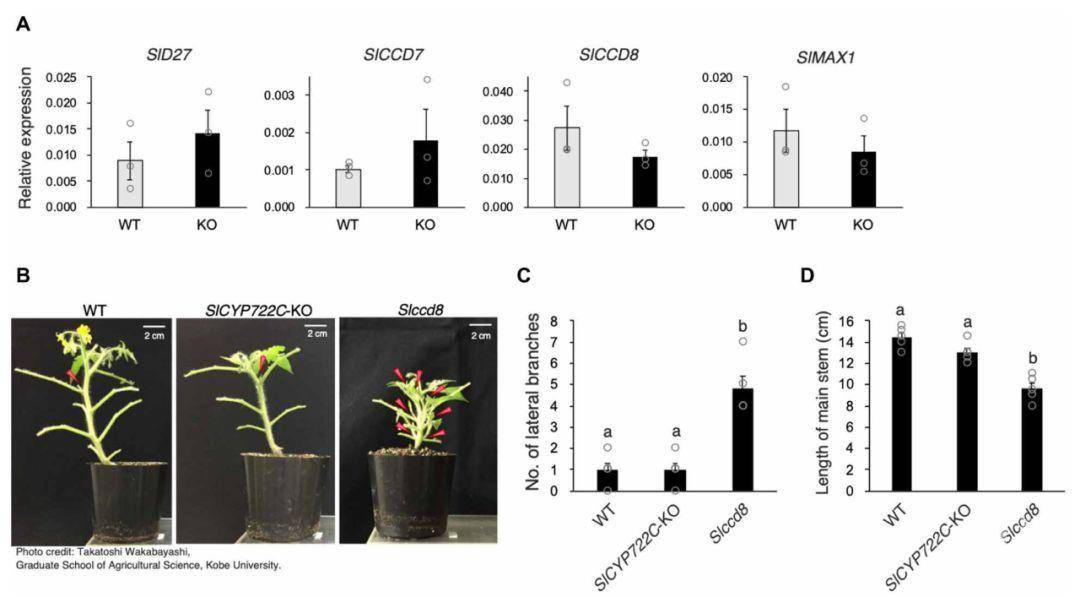
Effect of targeted mutation in SlCYP722C.
总之,该研究鉴定了一种新的邻苯二酚合酶CYP722C,该研究还表明对不同植物中CYP722家族酶的功能分析对阐明典型SL的生物合成机制具有至关重要的意义。
参考文献
【1】B. Zwanenburg, D. Blanco-Ania, Strigolactones: New plant hormones in the spotlight. J. Exp. Bot. 69, 2205–2218 (2018).
【2】K. Yoneyama, X. Xie, K. Yoneyama, T. Kisugi, T. Nomura, Y. Nakatani, K. Akiyama, C. S. P. McErlean, Which are the major players, canonical or non-canonical strigolactones? J. Exp. Bot. 69, 2231–2239 (2018).
【3】Y. Seto, A. Sado, K. Asami, A. Hanada, M. Umehara, K. Akiyama, S. Yamaguchi, Carlactone is an endogenous biosynthetic precursor for strigolactones. Proc. Natl. Acad. Sci. U.S.A. 111, 1640–1645 (2014).
原文链接:
https://advances.sciencemag.org/content/5/12/eaax9067
来源:bioartplants BioArt植物
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3ODY3MDM0NA==&mid=2247493981&idx=2&sn=23d3d6adb5cbdb489d4e8e485b026af2&chksm=fd73733aca04fa2cf4441daa7b685b8a1b0538335eabe891eb7777742c65e9c11ee9de97b00d&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

李家洋院士团队揭示一种全新的独脚金内酯信号转导机制 谢道昕评述

Karrikin与独脚金内酯信号途径共同调控水稻中胚轴发育

一种独脚金内酯受体被发现

李家洋院士团队揭示一种全新的独脚金内酯信号转导机制

Nature Plants | 绕过赤霉素途径,独脚金内酯调控种子萌发的分子机制
中科院科学家在独脚金内酯和脱落酸协同调控水稻分蘖研究中获进展
天津工生所在构建食品安全蛋白表达系统制备稀少糖方面取得进展

一种超凡的酶:新生物合成途径

昆明动物所赖仞团队首次发现凝血调节关键因子,有望成为疾病的治疗靶标

Nature Commun | 光信号和独脚金内酯协同调控植物分枝的分子机制