科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-03-09
来源:BioArt
原标题:杨建荣/陈小舒/张建之合作发现病毒密码子偏好性影响宿主表型和宿主——病毒共进化模式的新机制
真核生物基因组编码的20种氨基酸中,有18种能被多于1种“同义”密码子所编码。但由于细胞中不同类tRNA的供应量存在差异,同义密码子的使用频率也会对应地出现差别。该现象即所谓的“密码子偏好性”【1】。
过去的研究表明,密码子偏好性对基因表达主要有两个方面的调控作用:一方面,密码子偏好性能直接调节使用该密码子的基因本身的表达量(顺式调控, cis-regulation)【2】。
典型的例子就是病毒的密码子偏好性必须匹配宿主的tRNA供应(即接近宿主的密码子偏好性,因为宿主的密码子偏好性必然匹配其自身的tRNA供应),病毒才能实现高表达。这也是前段时间有针对2019新型冠状病毒(SARS-CoV-2)的研究利用其密码子偏好性推论蛇是可能的中间宿主的理论依据【3】。
另一方面,新近的研究表明,高表达的内源基因的密码子偏好性可以通过竞争性消耗tRNA资源,从而对基因组内其他基因的表达形成间接影响(反式调控,trans-regulation)【4】。
那么在病毒感染宿主的过程中,作为外源基因的病毒是否也能通过上述反式调控机制影响宿主的翻译系统,从而影响宿主的表型及宿主-病毒共进化的模式呢?
2020年3月2日,中山大学中山医学院杨建荣教授、陈小舒教授和美国密歇根大学张建之教授合作在Nature Ecology & Evolution杂志发表了题为 Dissimilation of synonymous codon usage bias in virus–host coevolution due to translational selection 的论文,解答了上述问题。
该论文的第一、二、三作者依次为:杨建荣教授团队博士后陈锋、硕士研究生吴鹏、陈小舒教授团队博士研究生邓舒韵。杨建荣教授、陈小舒教授及美国密歇根大学张建之教授是论文的共同通讯作者。
在该项研究【5】中,研究团队成员通过分析公开的核糖体图谱(Ribo-Seq)数据,证实了病毒基因的密码子偏好性同样能通过耗竭宿主tRNA,而对宿主基因表达形成反式调控作用。在模式生物(酵母)中的荧光报告基因实验进一步发现,外源基因的密码子偏好性越接近宿主,会导致该基因每单位表达量对宿主tRNA的耗竭作用(反式调控作用)变弱,降低对宿主翻译系统造成的负担;但同时也会导致该基因的表达量变高(顺式调控作用),提升对宿主翻译系统造成的负担。
上述顺式与反式调控对宿主的影响相反,但它们联合作用的结果是,与宿主密码子偏好性太像的病毒,会对宿主细胞的翻译产生抑制作用。研究团队最后分析了52种病毒及它们已知的无症状宿主与有症状宿主,发现病毒的密码子偏好性倾向于接近有症状宿主,而与无症状宿主差别较大,从而进一步支持了病毒密码子偏好性过于接近宿主会伤害宿主的结论。
传统理论认为,因为针对翻译过程的自然选择(翻译选择,translational selection),病毒密码子偏好性的进化方向应该是尽可能接近宿主,从而保证其表达量。而该研究则首次揭示了翻译选择同样也会导致病毒的密码子偏好性与宿主保持一定距离,否则宿主会出现显著的症状,影响宿主与病毒的长期共存。因此,该研究从理论上对根据密码子偏好性确定中间宿主的研究策略提出了质疑。同时,该研究为同一种病毒感染不同宿主时产生不一样症状的现象提供了新的具有普遍意义的科学解释,更为通过改造病毒来控制中间宿主种群提供了新的思路。
作者简介杨建荣教授,第13批青年千人,2016年入职中山大学中山医学院,长期致力于从进化基因组与系统生物学的角度,分析生物活动各个层面的随机现象,并发展相关的研究方法和分析工具,揭示随机现象对细胞正常生理功能和相关疾病的潜在重大影响。
陈小舒教授,第12批青年千人,2015年入职中山大学中山医学院,研究兴趣集中在运用高通量测序技术研究关键的生物学基础问题,包括影响各种错误率(DNA突变率,RNA转录错误率,蛋白质翻译错误率)的因素、分子层次和细胞层次的异质性的产生与演化规律、单细胞测序与精准医学的应用等。
原文链接:
https://www.nature.com/articles/s41559-020-1124-7
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652481896&idx=5&sn=843be14e6cc4d99034f14c58971482a9&chksm=84e23adcb395b3ca78479918694da19dac8a8dc93b85b0cd83872e6ba598b5d70a4c77b6fa8b#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Science | 密码子最优性监测中的分子机制

我国首个P4实验室正式运行,致力于最危险病毒研究

关于益生菌的科学真相
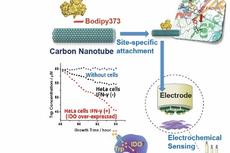
基于基因密码子扩展及新型生物正交反应“S-Click”方法改造氨基酸氧化酶

你身体里也有病毒基因:存在于众多生命中
起始密码子

穿山甲不是新冠病毒中间宿主,或是可能潜在自然宿主
注意!这5种药物在国外都是禁用的,国内却当成常备药!

翻译以密码子依赖的方式影响人类细胞mRNA稳定性
《自然》发文:麻省理工学院发现海洋中一种未知病毒