科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-03-26
来源:BioArt
原标题:Cell Research:陈万金/杨辉/左二伟合作利用CRISPR技术有望治疗脊髓性肌萎缩症患者
脊髓性肌萎缩症(Spinal Muscular Atrophy, SMA)是婴幼儿期最常见的致死性神经遗传病,主要病理表现为脊髓前角运动神经元的退行性改变。其中,严重型SMA患儿在缺乏有效干预的情况下,生存期一般难以超过2岁。运动神经元生存1(Survival Motor Neuron 1,SMN1)基因的纯合缺失是SMA致病原因。SMN2基因,作为SMN1基因的高度同源性拷贝,可表达~5%全长功能型转录本,起部分代偿SMN1基因功能。因此,通过改变SMN2基因的剪接模式,弥补SMN全长蛋白的不足,是治疗SMA的重要策略之一。虽然, Nusinersen(反义寡核苷酸药物ASO)作为第一个特异性基因修复治疗SMA药物已经进入临床,但须反复鞘内注射且需终身用药、费用昂贵(>100万人民币/年),极大限制了SMA患儿的获益。
2020年3月25日,Cell Research杂志发表题为“Base editing-mediated splicing correction therapy for spinal muscular atrophy”的研究论文,该研究证实通过新一代单碱基编辑技术能够高效修复SMN2基因的异常剪接、重启SMA患者SMN全长蛋白表达,有望成为SMA的基因治疗手段。福建医科大学附属第一医院神经内科主任医师陈万金,中科院脑科学与智能技术卓越创新中心研究员杨辉,中国农业科学院深圳农业基因组研究所研究员左二伟为共同通讯作者。
值得一提的是,2020年1月,陈万金/杨辉/施霖宇合作在National Science Review杂志发表研究论文,发现利用CRISPR/Cas9介导的非同源末端连接技术破坏SMN2基因7号内含子的的剪接沉默子后,可改变SMN2基因的剪接模式、显著提高SMN全长蛋白的表达水平,在SMA诱导多能性干细胞(iPSCs)和SMA小鼠(Smn-/-, SMN2TG/0)受精卵水平成功实现治疗。

而此次新发表的研究用单碱基编辑系统替代了之前传统的基于双链断裂的基因编辑系统,有望成为一个更为安全可靠的基因治疗策略。本研究首先采用TadA-TadA*-SaCas9n-KKH单碱基编辑器对SMA iPSCs的SMN2基因7号外显子剪接沉默子(ESS)进行编辑,发现成功编辑后的iPSCs SMN全长蛋白表达水平显著增高,其分化来源的运动神经元的功能性SMN全长蛋白颗粒增多;基于此,研究团队进一步通过显微注射获得了SMA基因编辑小鼠SC-SMAT5C(携带7号外显子第5个碱基编辑T→C),发现小鼠寿命可显著延长超过400天(未经编辑治疗的SMA小鼠寿命不超过14天)且可正常发育繁殖,证实了单碱基编辑系统对SMA治疗的有效性和安全性。
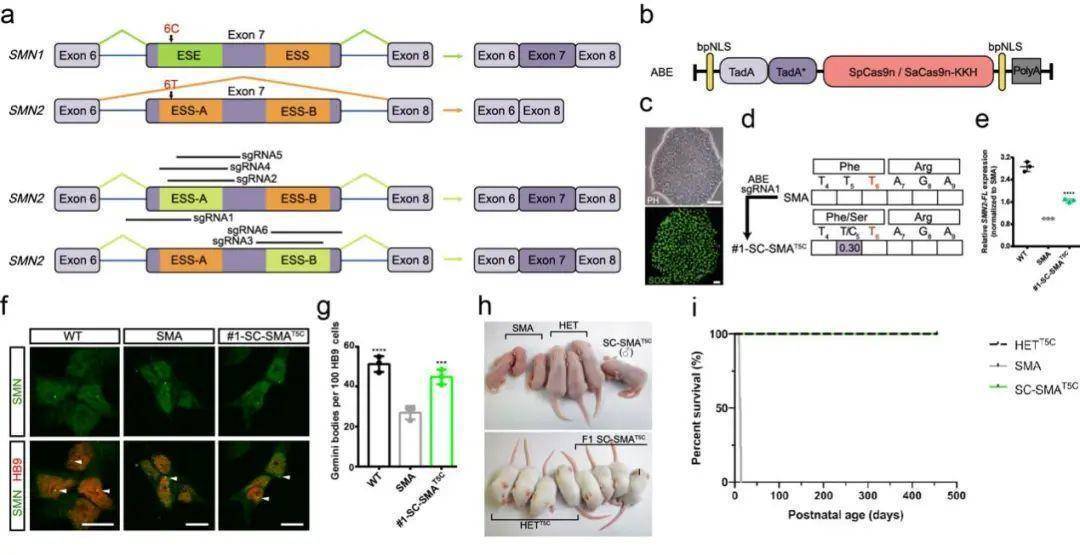
图1. ABE系统实现SMA干细胞及小鼠的治疗
为降低脱靶效应,研究团队进一步采用三种高保真性的腺苷酸脱氨酶单碱基编辑系统(TadAF148A-TadA*F148A-ABEmax; TadA*-ABEmax; TadA*V82G-ABEmax)分别在三种细胞系(HEK293T; SMA鼠胚胎干细胞; SMAiPSCs)对7号外显子ESS进行综合筛选,成功获得特异、高效编辑位点A36G(丝氨酸→丝氨酸),使得7号外显子的剪接沉默子ESS-B转换成剪接增强子,从而使得SMN全长蛋白表达水平显著提高。最后,研究团队采用电穿孔法分别在SMA iPSC分化来源的运动神经元和P0 SMN-△7小鼠的皮层神经元进行TadA*-ABEmax质粒转染,单细胞高通量测序显示A36G位点的成功编辑;首次证实了单碱基编辑器对运动神经系统的有效性,为本病将来的临床基因治疗提供了理论依据。
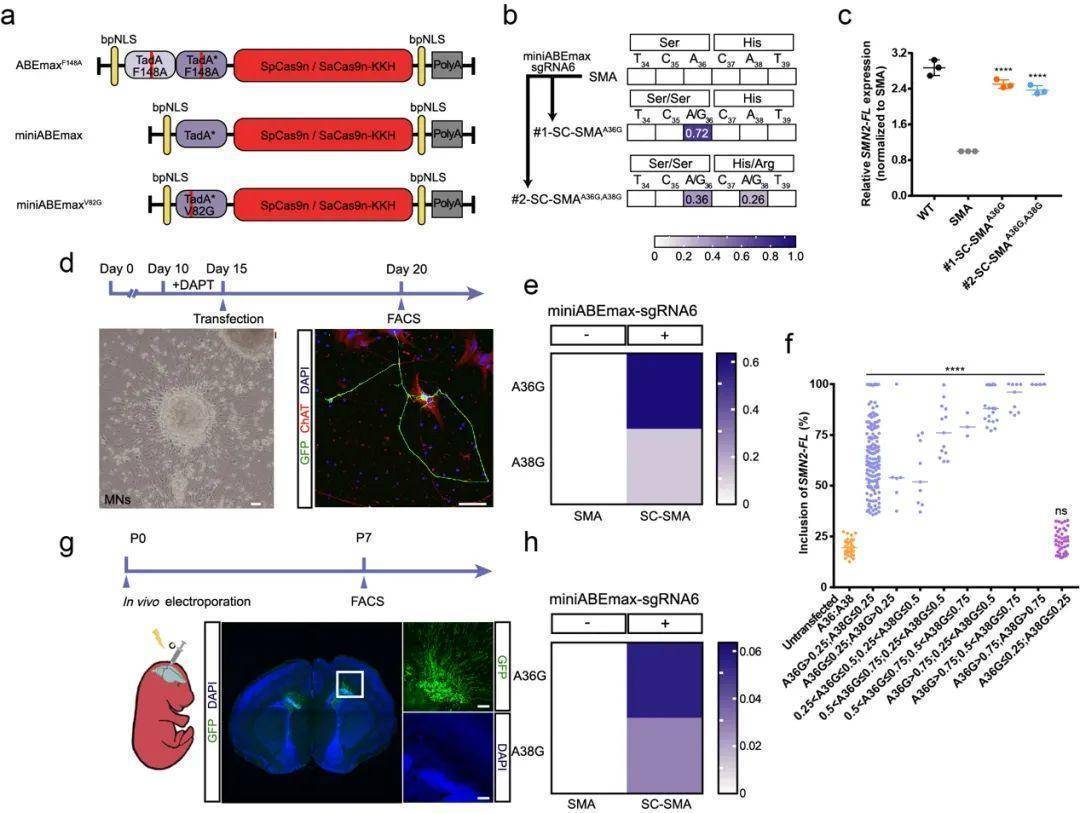
图2. 高保真性ABE系统实现SMA神经元的高效编辑
总的来说,不同于ASO药物治疗,该合作课题组共同开发建立了一种“一劳永逸”的单碱基编辑基因治疗SMA的策略,为将来SMA的临床治疗提供了新思路。
据悉,福建医科大学附属第一医院的林翔、陈海珠、陆瑛倩、洪舜彦和中科院脑科学与智能技术卓越创新中心胡新德为Cell Research论文共同第一作者;此外,福建医科大学附属第一医院的李锦晶、林翔、陆瑛倩和中科院脑科学与智能技术卓越创新中心唐骋、胡新德为National Science Review论文共同第一作者。这两项工作都得到了复旦大学上海医学院组织胚胎学系马丽香副教授的大力协助。
福建医科大学附属第一医院神经内科主任医师陈万金,国家自然基金优秀青年基金获得者、百千万人才工程国家级人选,长期致力于神经遗传病的临床及基础研究,先后发现了原发性家族性脑钙化症(PFBC)常染色体隐性致病基因MYORG (Neuron 2018, 最后通讯作者)、遗传性痉挛性截瘫(HSP)新致病基因UBAP1(Brain 2019,通讯作者)以及发作性运动诱发性运动障碍(PKD)首个致病基因PRRT2(Nature genetics2011,第一作者)。此外,近20年来一直致力于脊髓性肌萎缩症(SMA)的规范诊治,自2015年开始,即与中科院脑科学与智能技术卓越创新中心杨辉研究员合作,探索SMA新的治疗手段。此次成果的发表,也标志着中国研究者在SMA治疗领域已开始有所作为。
原文链接:
https://www.nature.com/articles/s41422-020-0304-y;
https://academic.oup.com/nsr/article/7/1/92/5559252
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652482620&idx=4&sn=0e665c70cc5d615e4bf06574f067be47&chksm=84e23f88b395b69ed313dbef010c020c01785accbfd98c10145eea4fb3dab181ce1185f264da#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

华南地区首例!南方医院完成脊髓性肌萎缩症成人患者的特药治疗

基因编辑进入新时代
基因编辑的可控开关
揭秘基因编辑技术

蚊子怕怕了,利用转基因能破坏它们生育能力,必死无疑
编辑基因创造超人,霍金的担心是不是杞人忧天



同样搞基因编辑,贺建奎 黄军就何以评价两极化



基因编辑临床试验10原则出台

中国科学家率先培育出带有基因剪刀的工具猪

重大进展!武汉大学徐永镇等团队发现次要剪接体突变可诱导脊髓性肌萎缩症相关表型