科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-04-28
来源:BioArt
责编丨兮
近年来RNA化学修饰研究引起了学术界的密切关注。在迄今为止已经鉴定的150多种RNA化学修饰中,m6A(N6-甲基腺嘌呤)修饰是哺乳动物细胞信使RNA (mRNA)内部丰度最高的碱基化学修饰 (3-5 m6A/mRNA),其生物学功能研究也最为广泛,近乎影响RNA代谢寿命过程中的每一个环节,包括转录、剪接、降解、翻译和运输等。这些研究成果的取得都得益于m6A检测和测序技术的发展,其中2012年发表的基于m6A抗体免疫沉淀的高通量测序技术(m6A-seq【1】或称MeRIP-seq【2】)最为常用,但该方法只能提供100-200核苷酸的检测窗口。
为了深入理解m6A甲基化的功能,单碱基分辨率信息是必需的,它能在碱基层次上帮助我们理解细胞内甲基化的机理和功能。领域内先后探索了一些RNA m6A单碱基或近乎单碱基分辨率的测序方法,包括基于抗体/RNA光交联的方法(PA-m6A-seq、miCLIP等)、基于RNA m6A甲基化敏感的内切酶法 (m6A-REF-seq或称MAZTER-seq)、基于m6A结合蛋白融合碱基编辑蛋白的方法(DART-seq),这些方法都促进了领域的发展,但多数都是间接的手段(除m6A-REF-seq外)。基本原理是通过抗体-RNA光交联位点的碱基逆转录突变信息或者特异性蛋白-RNA结合区域附近碱基的编辑信息,来判断突变点或编辑点近邻的腺嘌呤为m6A,这往往会在真实位点鉴定(尤其是簇位点)上产生偏差。m6A-REF-seq方法是一个好的直接方法,但是当前的内切酶只对m6ACA序列响应,还有大部分其它甲基化基序序列未被测出。因此,该领域还需要发展新的m6A单碱基分辨率测序方法,解决当前存在的问题。
2020年4月27日,浙江大学高分子科学与工程学系刘建钊课题组在Nature Chemical Biology上长文发表题为A metabolic labeling method detects m6A transcriptome-wide at single base resolution的研究,报道了一种称为m6A-label-seq的高通量测序方法,通过细胞自身代谢对全转录组RNA m6A位点进行标记,标记位点可发生化学处理诱导的逆转录碱基突变,进而实现单碱基分辨率测定。

细胞内S-腺苷甲硫氨酸(SAM)是甲基转移酶的辅助因子,可在mRNA m6A甲基转移酶(METTL3/METTL14)的作用下,将其甲基转移到mRNA上的特定腺嘌呤的N6位点形成m6A。SAM是以甲硫氨酸和三磷酸腺苷(ATP)为原料,在甲硫氨酸腺苷转移酶(MAT)的催化下合成的。作者从甲基化源头考虑,引入带有烯丙基修饰的甲硫氨酸,在细胞内MAT作用下生成烯丙基取代的辅助因子allyl-SAM或者硒代同源物allyl-SeAM (图1)。细胞内METTL3/METTL14利用allyl-SAM或allyl-SeAM,将其烯丙基修饰到mRNA上原本是m6A的位点,得到a6A(N6-烯丙基腺嘌呤),a6A在温和的碘加成条件下诱导生成环化1,6位环化腺嘌呤(cyc-A) (图1),然后,RNA cyc-A在逆转录成互补DNA(cDNA)时发生碱基错配【3】。最后,借助高通量测序和生物信息学分析突变位点,得到了全转录组m6A位点的单碱基分辨率图谱。
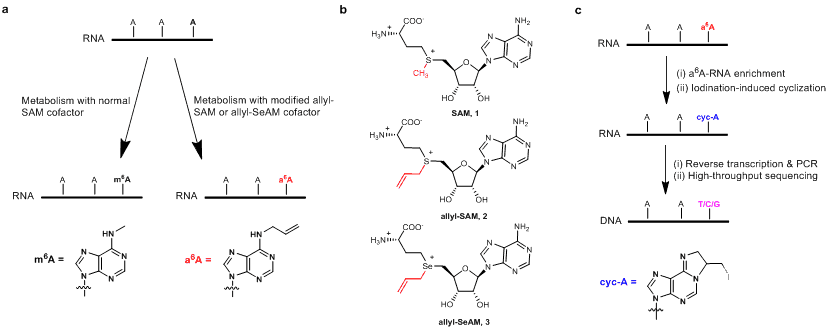
图1. 示意图描述利用代谢标记测定RNA m6A精确位置的方法
作者利用m6A-label-seq方法对人体HeLa和HEK293T细胞系以及老鼠H2.35细胞系的mRNA m6A位点、位点距离、m6A共有基序(m6A motif)等信息进行了系统分析。为了验证该高通量测序方法的准确性,作者选取了个体基因进行了低通量的测序验证。作者同时也将m6A-label-seq与miCLIP-seq、m6A-REF-seq、DART-seq等已知测序数据进行了对比,选取了16个特征位点,用独立正交的SELECT【4】 m6A鉴定方法验证了这些位点的可靠性。
综上,该研究的测序方法特点如下:(1)利用代谢对甲基化位点的源头标记并直接单碱基分辨率测定,相对于当前的间接方法有更高的准确率;(2)适用于细胞内RNA多种不同甲基化序列(m6A motif)的鉴定;(3)对测定m6A簇修饰有优势。该方法为将来研究细胞核内种类繁多的新生RNA的m6A甲基化位点及状态演变提供了重要工具。另外,该方法在标记产率和标记时间窗口尺度方面还需要优化提高,为研究更多的细胞事件过程提供便利。
浙江大学高分子科学与工程学2017级直博生舒潇与2016级直博生曹婕同学为本论文的共同第一作者,刘建钊研究员为通讯作者。通讯作者也是浙江大学生命科学研究院兼职PI。

在同期杂志,北京大学贾桂芳课题组发表了“Antibody-free enzyme-assisted chemical approach for detection of N6-methyladenosin”的研究论文。

该方法巧妙地利用m6A的去甲基酶FTO蛋白作为催化剂,将mRNA上化学惰性的m6A转化为高反应活性的中间态产物N6-羟甲基腺嘌呤(hm6A),然后利用二硫苏糖醇(DTT)的巯基与hm6A发生亚胺1,2加成反应,将不稳定的hm6A转化为更稳定的巯基加成产物dm6A。dm6A上的自由巯基可以与甲烷硫代磺酸(methanethiosulfonate,MTSEA)快速反应,实现在mRNA上m6A的位置标记生物素Biotin,最终可被链霉亲和素珠捕获,从而富集含有m6A修饰的RNA片段供后续高通量测序使用。此方法被命名为m6A-SEAL(FTO-assisted m6A selective chemical labeling method)。
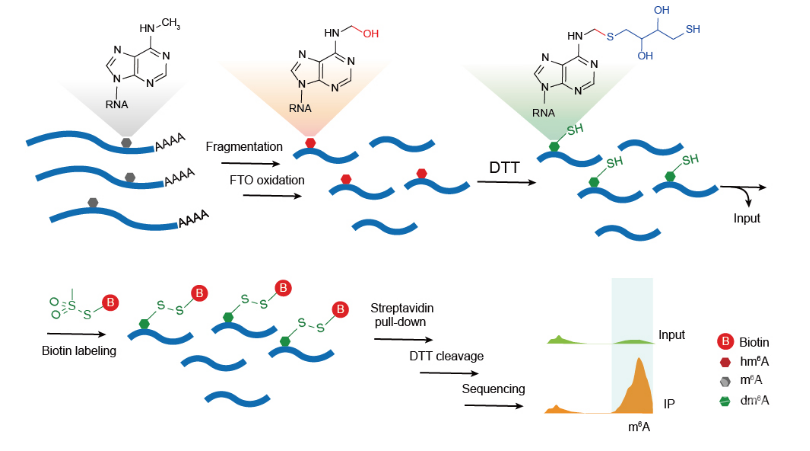
在人HEK293T细胞的polyA+ RNA上应用m6A-SEAL之后,研究者们鉴定到了8605个高置信度的m6A位点,这些位点符合m6A的保守序列(RRACH)和分布模式。早期利用m6A抗体测序技术在不同的植物中鉴定出了非经典的m6A保守基序(UGUA),但难以判断该结果是否来自抗体非特异性富集信号。研究者们在水稻中应用m6A-SEAL也鉴定到了UGUA的非经典基序,并验证了其真实性。最后通过该研究组之前开发的基于qPCR的m6A单位点检测方法SELECT验证了多个m6A位点,证明m6A-SEAL作为化学共价交联技术,要比基于抗体的方法或DART-seq具有更高的可靠性和灵敏度。
此外,除m6A外,FTO还对RNA5’帽位置的N6,2'-O-二甲基腺嘌呤 (cap m6Am)具有催化活性,能将其催化为hm6Am。为了验证m6A-SEAL测序方法是否还会同时检测cap m6Am,研究者们通过体外酶活性实验和标记实验发现目前m6A-SEAL方法中使用的FTO氧化反应条件只能特异性将m6A反应成hm6A,通过优化FTO氧化反应条件可以实现m6A-SEAL只针对cap m6Am的标记和测序。
总之,该项研究首次利用FTO酶辅助实现了m6A化学标记,并成功应用于高通量测序。m6A-SEAL具有高灵敏度和高特异性的特点,可以应用于少量mRNA样品中。未来研究者们将继续对m6A-SEAL进行优化和改造,以实现单碱基分辨率。由于FTO可以氧化催化RNA的cap m6Am和DNA的N6-甲基脱氧腺嘌呤(6mA),未来m6A-SEAL通过优化有望应用于这些化学修饰的测序。同时该方法除了可以在m6A上标记biotin用于富集,还可以标记荧光素,未来用于m6A的成像。
北京大学贾桂芳实验室已毕业的博士研究生王烨为论文的第一作者,已毕业的博士研究生肖雨、博士后喻琼和本科生董舜卿为共同作者,贾桂芳研究员为通讯作者。
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652483815&idx=2&sn=7bd24c46b6d1c0ec93f7dc4688af83b7&chksm=84e22353b395aa45bbfe19979e6e3148211c02b9b112e08796a26c1b9b38cc98cf177b58e7ca#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
利用Nanopore高通量测序技术解析污水处理体系可移动抗性基因组
精彩预告 | 高通量测序技术在临床中的应用及高通量实验室的规范化建设
MPB:沈阳生态所李琪组-土壤线虫群落DNA提取、扩增及高通量测序

Cell:高质量&高通量!马赛博士等开发单细胞测序新技术测定染色质潜力

程溪柳/刘君/库丽霞合作开发TEAseq技术,用于高通量测序鉴定玉米转座子插入突变体库

DNA测序技术取得新突破

疾控福利~纯干货的高通量测序培训班
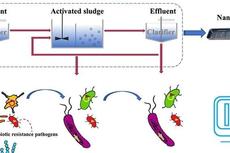
利用Nanopore高通量测序技术解析污水处理体系可移动抗性基因组

在一天内完成样本制备到结果报告全流程的高通量基因测序平台
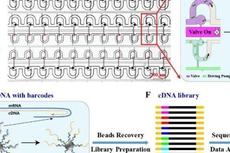
厦门大学杨朝勇教授课题组在高通量单细胞转录组测序研究中取得新进展