科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-06-05
来源:BioArt
肝癌是我国第二大致死癌症,乙肝病毒感染等病毒性肝炎和非酒精性脂肪肝炎等是肝癌的主要诱因。虽然肿瘤免疫检查点治疗在临床上的应用越来越广,但相比于其他癌症,肝癌形成强大的免疫耐受微环境使得肝癌患者长期处于免疫低应答状态,容易形成对肿瘤免疫治疗的抵抗性。因此,研究如何打破肝癌的免疫耐受,促进T细胞介导的抗肿瘤免疫应答有着重要的临床意义。

[封面解读]:“特洛伊木马故事”,肝癌微环境(寓意城墙)具有极强的免疫抑制性。研究人员发现通过靶向HDAC6释放辅助性TH17细胞效应功能,能够打破并重塑肝癌免疫耐受微环境,促进杀伤性CD8+ T细胞浸润肿瘤并触发机体抗肝癌免疫应答。
TH17细胞是一群能够分泌 IL-17A/F细胞因子、表达趋化因子受体CCR6和转录因子RoRγt的CD4+ 辅助性T细胞。它能够招募并活化肝脏内的免疫浸润,放大机体免疫监视能力。已有研究报道TH17细胞在过继转移治疗相关疾病中有着潜在的转化价值。但同时TH17细胞也具有可塑性,其能够在低水平TGF-β1诱导的情况下分化为“致病性”的TH17细胞,在高浓度TGF-β1会使其转分化为Tr1抑制性T细胞。由于肝癌微环境显著上调 TGF-β1表达,促使TH17细胞的免疫效应功能受到抑制,甚至可能变成肝癌的“帮凶”。因此,研究TH17细胞的免疫效应机制对肝癌的临床治疗有着重要的科学意义。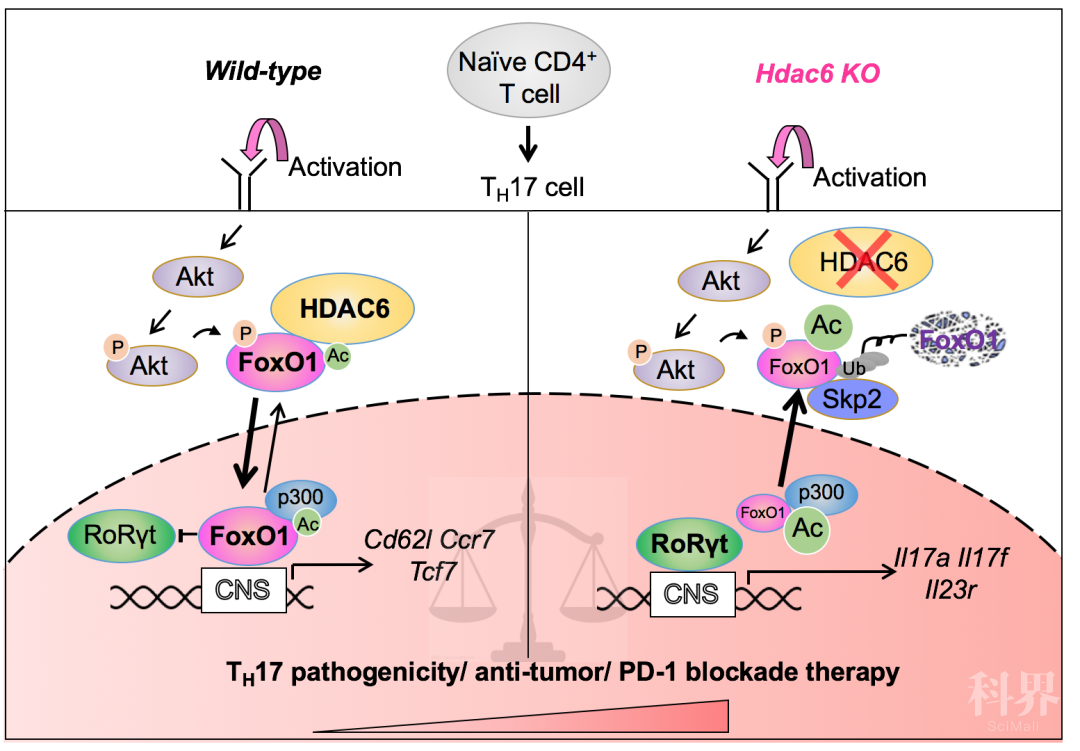
「机制示意图」:HDAC6通过对FoxO1蛋白的去乙酰化修饰促进FoxO1蛋白的核转位及蛋白稳定性从而抑制TH17细胞转录因子RoRγt的活性。当靶向抑制HDAC6能够重编程TH17细胞的免疫效应功能,促发机体的抗肿瘤能力及肝癌对anti-PD1抗体的反应,从而达到抑制肝癌进程的效果。
该工作由中国科学院生物物理研究所、清华大学生命科学学院、杜克大学和南京大学鼓楼医院多家单位合作完成。生物物理研究所感染与免疫重点实验室研究员杨鹏远教授为论文的通讯作者,杨鹏远课题组博士研究生邱伟楠为论文的第一作者。来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652487096&idx=7&sn=bbaf446909f9584d06fc347b0c1cfdd1&chksm=84e22e0cb395a71aefb67508171b3bf1f8424f7ab02ff1ac80fb0104155749cef71719380429#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

关于单细胞测序刻画肝癌免疫微环境动态特征的研究
单细胞水平肺癌T细胞免疫图谱绘就
影像学特征可用于预测肝癌患者生存期
【大师讲堂】免疫耐受是如何产生的?
【大师讲堂】免疫耐受是如何产生的?

跟移植免疫耐受说再见!1型糖尿病患者告别抗排异药物

Science子刊 | 中科院科学家找到癌症免疫耐受新方法

生物物理所揭示调控肝癌微环境T细胞免疫耐受新机制

世界肝炎日|慢性HBV感染免疫耐受期抗病毒治疗的新认识

中国科学家发现肝癌发病新机制