科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-06-18
来源:BioArt
肠道微生物合成数百种分子影像宿主的生理功能,其中含量最丰富的代谢产物主要包括脱氧胆酸(Deoxycholic acid,DCA)和石胆酸(Lithocholic acid,LCA)在内的次级胆汁酸(Secondary bile acids),DCA和LCA在体内可以积累达到500 μM浓度并且具有抑制艰难梭状芽胞杆菌生长【1】、促进肝癌(Hepatocellular carcinoma)的发生【2】并通过G蛋白偶联受体TGR5调节宿主的代谢【3】的功能。DCA和LCA以及他们的衍生物是胆酸循环的主要组分,同时这些组分也是治疗原发性胆道胆管炎和非酒精性脂肪性肝炎的靶标。但是一直以来,尽管DCA和LCA对宿主生理有明显的影响,但是由于对DCA和LCA生物基因合成的了解有限以及相关基因工具的缺乏,人们对于如何调节宿主中次级胆汁酸的水平还束手无策。
为了解决这一问题并揭开次级胆汁酸合成的信号通路,2020年6月17日,美国斯坦福大学Michael A. Fischbach研究组与阿尔伯特·爱因斯坦医学院Steven C. Almo研究组合作在Nature发文题为A metabolic pathway for bile acid dehydroxylation by the gut microbiome,揭开了肠道微生物介导的胆酸脱羟基作用信号途径,为控制胆酸代谢以及合成相关替代分子提供了可能的机会。

人体肠道菌群中有数百条代谢途径,其中大部分是由尚未被识别的基因编码的【4-6】。其中次级胆汁酸DCA和LCA合成途径由于其组织艰难梭状芽胞杆菌生长、促进肝细胞癌的发生以及调节宿主的代谢【7】和免疫反应【8】而备受关注。在1980年,科学家们在肠道微生物Clostridium scindens VPI 12708中发现胆酸通过7α-脱羟基作用(图1b)产生DCA。胆酸可以作为7α-脱羟基作用发生的诱导剂的相关知识促进了包含八个基因在内的胆酸诱导操纵子bai(Bile-acid-induced operon)操纵子的发现(图1a)。
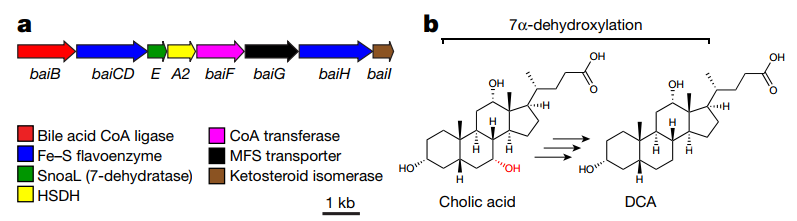
图1 bai操纵子以及7α-脱羟基作用
为了对胆酸脱羟基作用信号通路进行全解析,作者们通过在厌氧条件下的纯化和分析相关的酶,在体外重建了7α-脱羟基作用。通过体外克隆操纵子编码的Bai酶并与胆酸、NAD+、CoA以及ATP在厌氧的条件下共同孵育后,作者们发现在液相色谱和质谱分析后会出现胆酸到DCA的时间依赖性转化,说明重组的BaiB、BaiCD、BaiA2、BaiE、BaiF和BaiH足以促进7α-脱羟基作用的发生而不需要其他酶的参与。
在确定了该信号途径中必要的Bai酶之后,作者们试图对该途径的遗传控制,为肠道菌群胆酸输出提供可能的方法。但是将体外构建的DNA引入Clostridium scindens中并非易事,而且也没有办法在肠道共生体中表达bai信号通路。因此,作者们从美国菌种保藏中心筛选到了一种菌C. sporogenes,C. sporogenes与Clostridium scindens相关因此具有相似的代谢信号通路同时C. sporogenes中已经有适合的方法可以将质粒转入进行基因操作【9】。通过穿梭载体(Shuttle vector)【9】,作者们成功将Bai酶相关的质粒转入进了C. sporogenes之中产生了MF001菌株(图2)。当将与胆酸共同孵育的时候,MF001菌株可以随着孵育时间的延长而产生DCA。因此,作者们成功构建了具有核心bai基因簇并且足以促进胆酸脱羟基化作用发生的菌株。
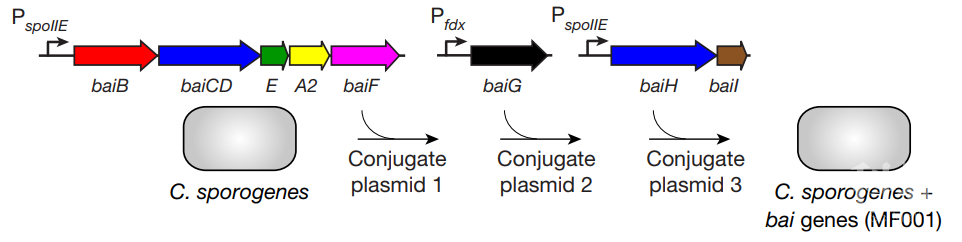
图2 利用穿梭载体产生胆酸脱羟基菌株MF001
最后,作者们将MF001菌株转入无菌小鼠之中,看其是否能够促进宿主中胆酸脱羟基化作用后产生相关的中间产物以及次级胆汁酸。在体内进行检测后,作者们发现转入MF001菌株后,可以检测到DCA的产生但是比Clostridium scindens菌株的水平要低一些,但是与阴性对照相比仍然有明显的DCA的产生(图3),这可能是由于体内环境较为复杂且可能需要其他额外因子参与导致的。但是无论怎样,该工作仍然为胆酸的调控以及工程学设计提供了一个新的起点。
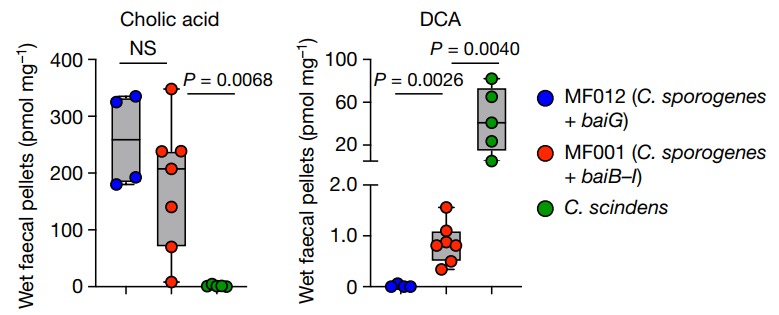
图3 体内检测脱羟基化作用信号通路的活性
总的来说,Fischbach与Almo研究组的工作揭示了胆酸7α-脱羟基作用的过程,为其他途径在肠道产生高丰度代谢物寻找了研究范本,同时通过胆酸库两个核心成分DCA和LCA完整信号通路的建立为控制微生物组的胆酸输出提供了遗传基础。
原文链接:
https://doi.org/10.1038/s41586-020-2396-4
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652488376&idx=4&sn=5a8ef146e89c9e0e871c4cbbdff92ca4&chksm=84e2510cb395d81ad71a8e34579fec67f791d13a891992f9505fa15b920c586fe43ea2e53853#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

肠道菌群与药物代谢

运动可以改变肠道菌群,并且是有益的

肠道菌群已成健康“预警器”
Nature:肥胖与肠道菌群紊乱有关,他汀类药物可以增强肠道菌群多样性!

珊瑚肠道共生菌群与珊瑚健康

肠道菌群与外科疾病

肠道菌群随季节改变

细说“肠道菌群-肠道-肝脏轴”的恩怨情仇
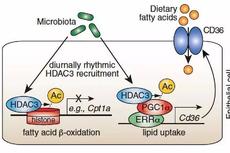
Science:肠道菌群与生物钟
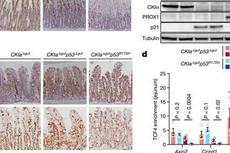
肠道菌群又登Nature:抑癌或促癌?肠道菌群说了算