科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2017-11-17
中国是肝病大国,每年约有40万人死于肝癌,在致死癌症排行榜里位列第二,且占到了世界肝癌死亡人数的一半。而在肝病的发展过程中,肝纤维化是必经阶段。此前已有研究发现,肝血窦血管化和肝纤维化之间有着千丝万缕的关系,医疗界也试图用控制血管化来对抗肝纤维化。但这层关系始终模糊,疗效也充满争议。
清华大学医学院副教授杜亚楠团队最近的一项研究首次明确阐释了上述争议背后的原因,同时创新性地提出基于胶原纤维机械力学介导的肝纤维化发病机制。该项研究为肝纤维化提供了精准干预策略,相关成果于11月14日在线发表在国际学术期刊《自然》(Nature)子刊《自然 • 材料学》(Nature Materials)。
杜亚楠在接受记者采访时表示,“目前肝纤维化、肝硬化都没有特效药,很多大药厂都在集中开发这类药物。目前临床上只能用现已有的相对比较广普的药物去尝试,尤其是晚期阶段,大量病人无药可治。而且最终很容易导致肝癌,发病率和死亡率都非常高。”
杜亚楠认为,该项研究首次从胶原纤维生物力学的角度提出了一种新的肝纤维化发病机制,可以为肝纤维化治疗提供新的靶向。
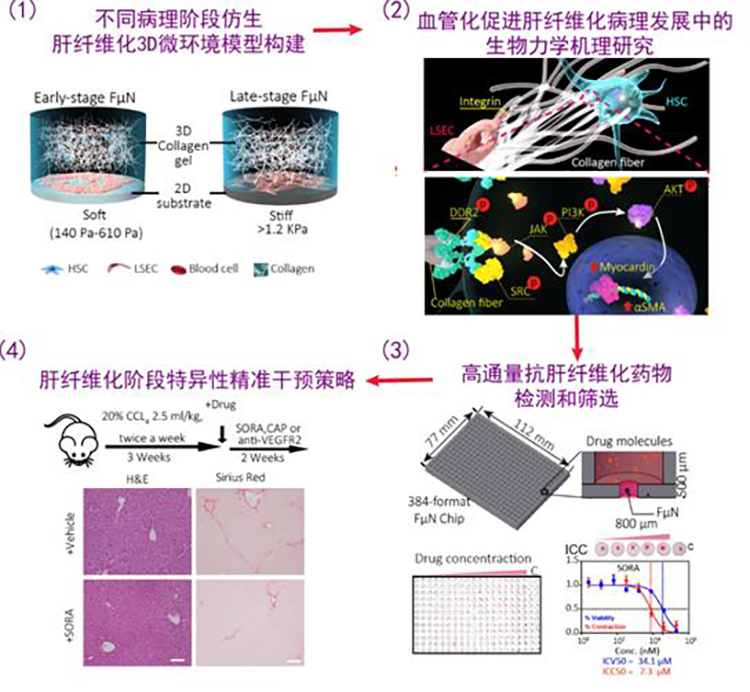
这项研究始于5年之前。最终点亮探索之路的是杜亚楠团队和临床医生的一项观察结果:早期肝纤维化确实存在大量肝血窦血管化,而晚期肝纤维化反而是血管化非常少。
通俗来讲,肝血窦就是肝脏里面的布满的血管网。杜亚楠介绍,“我们服用的药物、吃的食物都要进入血液,首先经过肝脏的解毒、代谢,再进入身体循环系统的其他部分。”然而,肝脏里的血管和其他组织中的血管并不一样。“其他组织的血管是有基底膜的,就是血管外面包裹着一层其他物质。而肝脏里的血管在正常的状态下是非常通透的,没有基底膜,它要过滤大量的血。”
但没有基底膜的通透肝血窦面临很多威胁。饮酒、乱服药物、乙肝丙肝等肝炎患者,总而言之,当肝脏在受到外界威胁和伤害的时候,肝血窦就成为第一个受害者。一旦意识到自身受到伤害,这些血管会发起“自卫”行动以阻止更多异物进入肝脏。
“自卫”措施就包括发生肝血窦毛细血管化,也就是所谓的血管新生的现象,反而长出基底膜,改变正常状态下的通透性。
早期存在大量肝血窦血管化的现象,这和目前研究者建议用抗血管化策略来应对肝纤维化是基本符合的,而这种策略实际上是借鉴肝癌治疗。
目前明确的是,在肝癌等癌症疾病中,新生血管是非常明显的一个特征,因此抑制新生血管成为了一种抗癌策略。肝纤维化中出现肝血窦血管化的现象不禁引发相关研究人士和医疗界设想:能否将抗癌抗血管化的这种治疗方法用到抗纤维化上?
但从国内外已完成的一些基础研究来看,这种治疗方案在动物模型上抗纤维化效果扑朔迷离。以肝癌常用药物,抗血管化的索拉非尼为例,争议就颇多。
“有的报道说抗血管化可以逆转纤维化。但也有人发现,抗血管化并不能逆转纤维化,有时促血管化反而会有助于肝纤维化的逆转,例如加入促进血管新生的生长因子。所以说目前抗血管化策略在治疗肝脏纤维化中的效果确实存在很大的争议。”杜亚楠提到。
这或许就和杜亚楠团队和临床医生观察到的肝纤维化在不同阶段血管化程度不同有关。
值得一提的是,在肝纤维化形成过程中,“罪魁祸首”是肝星形细胞(HSC)。要揭开上述争议谜底,研究者决定集中研究究竟有哪些途径可以激活肝星形细胞。
正常状态下,肝星形细胞处于静息状态。但这类细胞一旦激活,就将直接导致肝纤维化。肝星形细胞是纤维化肝脏中细胞外基质(ECM)的主要合成细胞,能合成和分泌胶原及糖蛋白、蛋白多糖等基质成分。而肝血窦内皮细胞则是肝血窦毛细血管化的效应细胞。
正基于上述联系,肝血窦内皮细胞对静息状态的肝星形细胞来说就是一颗“定时炸弹”,研究者也在试图深入了解这二者的相互作用。
据杜亚楠介绍,现有的研究是直接将这两种细胞体外混合培养来观察相互作用,普遍从生物化学的机制来阐释。“一些研究认为两者的相互作用是通过旁分泌,比如说肝血窦内皮细胞会分泌内皮素、一氧化氮等因子,来调节肝星形细胞的激活、收缩,包括分泌一些胶原,出现纤维化的特质。这是目前传统的一个理解。”
但杜亚楠团队认为,除了生物化学机制以外,应该还存在着和生物机械力学相关的机制,因为肝纤维化到肝硬化的发展过程伴随着组织机械硬度的逐渐增加。而这几年生物力学有了比较大的发展,或许在这个机制基础上会帮助肝纤维化产生一些新的疗法。
杜亚楠团队和临床医生合作,通过对人和老鼠的肝纤维化、肝硬化的不同阶段的体内组织切片观察到,早期肝纤维化确实存在大量血管化,而晚期肝纤维化反而是血管化非常少。基于这样的临床样本观察前提,团队构建了他们的研究模型。
在这个模型中,首先模拟肝纤维化、肝硬化过程中组织硬度逐渐增加的特点,研究团队用聚乙二醇(PEG)水凝胶制备了细胞培养支架膜(2D),并且在硬度方面设置了梯度,这个梯度就用来模拟在组织变硬过程中硬度的变化。
“我们把肝血窦内皮细胞种植到不同硬度的材料上,结果发现只在特定的硬度区间,也就是140-160Pa这样一个狭小区间内,它才会发生毛细血管化的现象。而在其他阶段,尤其是在肝硬化这个区间里,整个毛细管细化的现象就消失了,表现出的仅仅是是老化血管的一些特征。”
这部分也就可以印证此前长期存在的抗血管化治疗的争议。在肝纤维化治疗中,早期阶段使用抗血管药物是有效的,而晚期则无益,若不分阶段用同一类药物,疗效自然不一。
接着,在上述基础上,研究团队把带有胶原纤维的,包含肝星形细胞的仿生3D培养的微组织置于不同硬度血窦内皮细胞的上方。这样的一种空间构建方式,实际上也是模拟了体内肝血窦内皮细胞和肝星形细胞之间存在的Disse腔(窦周隙)。
结果发现,肝血窦内皮细胞在特定硬度区间内发生血管化的过程中,伴随着肝血窦内皮细胞的迁移,会“扯到”胶原纤维。杜亚楠将这种作用方式比作“拔河”,而且这种“拔河”会带来恶性循坏的后果。
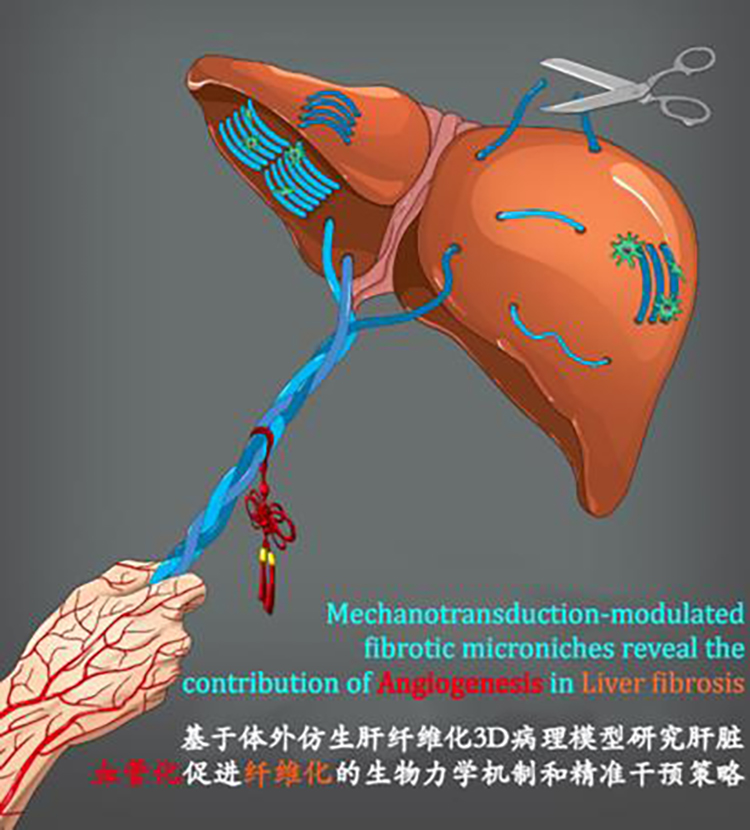
具体来说就是,在这场“拔河”中,胶原纤维就是绳子,血管化一发生,相当于一端绳子一拉,这根绳子也就是胶原纤维产生了变化,也就意味着细胞外基质被重塑。同时,绳子另一端的肝星形细胞原本处于静息状态,此时通过胶原纤维机械力的传导被激活。肝星形细胞一旦激活,又会持续分泌更多的胶原,更多的胶原继续被重塑,如此恶性循环。
不过,研究指出,这种恶性循环只会在特定的硬度区间出现,过软或过硬都不会出现。
自此,这项研究可以得出,细胞和细胞之间的相互交流并非只能通过旁分泌的游离因子来实现,还能通过胶原纤维这样的生物材料基质介导的物理作用来传导信号。杜亚楠称,“我们研究中提出的胶原纤维的机械性介导是一个全新的领域。”
既然肝星形细胞,也就是肝纤维化过程中的“罪魁祸首”被激活的机制有了新发现,这就意味着肝纤维化治疗僵局多了一种破题的可能性。
剪掉这根绳子就成为了一种可行的途径。“BAPN这样的胶原纤维抑制剂,就是这把‘剪刀’。尤其在肝纤维化晚期,因为早期抑制血管化对抑制肝纤维化是有效果的,但晚期抑制血管化是没有效果的,甚至是有副作用的。目前来看,晚期去剪这个绳子提供了一个潜在的干预策略。”
研究团队进一步结合微加工技术,将肝纤维化微环境模型进一步微小化为药物筛选阵列,形成高通量体外抗纤维化药物检测及筛选平台。
根据肝纤维化微环境模型体外药敏和动物模型如小鼠不同阶段肝纤维化疾病模型的测试,研究团队证实,如索拉非尼和抗VEGFR(抗血管内皮生长因子受体)这样的抗血管生成药物仅对小鼠早期肝纤维化治疗有效,而对于晚期纤维化逆转无效;同时证明BAPN可减轻晚期肝纤维化,提示靶向微环境细胞外基质组分(如胶原纤维)对于晚期肝纤维化的潜在疗效。
来源:澎湃新闻

中国科学家发现肝癌发病新机制
影像学特征可用于预测肝癌患者生存期
吃姜会得肝癌



新希望!一项阻止肝癌发展的新方法

演员吴孟达因肝癌入院!一发现就是晚期的肝癌怎么防?

【科普】肝癌患者合理饮食很关键
肝癌一线免疫联合疗法获批!显著延长中国肝癌患者生存期

肝癌诊疗开启“私人订制”模式

肝癌“身份指纹”被破获
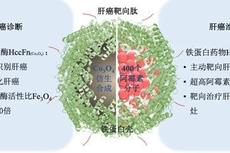
铁蛋白探针:精准靶向肝癌,使其可视化并杀死肝癌细胞