科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-06-23
来源:植物科学最前沿
染色体浓缩是细胞分裂的前提基础,有丝分裂和减数分裂都需要将复制后的细长染色体浓缩成棒状的染色体,进而保证后期的正确分离。相比之下,有丝分裂中染色体从前期到中期是快速的一步浓缩,而减数分裂包括减数分裂I和II,其中减数分裂I是该细胞分裂方式所特有,前期I又包括细线期、偶线期、粗线期、双线期和终变期,过程主要涉及到父母同源染色体之间的配对、联会和重组。为了保证这些核心事件的有序进行,染色体的浓缩是逐步进行的。研究表明,染色体浓缩主要由浓缩和粘黏蛋白复合体控制,但真核生物减数分裂进程中如何调控浓缩蛋白复合体,从而完成染色体的逐步浓缩机制尚不清楚。王应祥和马红团队2016年揭示了植物减数分裂细胞特异编码PHD结构域蛋白MMD1,其可能通过PHD识别组蛋白H3K4me3直接调控浓缩亚基CAP-D3的表达,从而控制了染色体的前期浓缩进程(Wang et al., Plant Cell)。然而,MMD1调控CAP-D3的具体分子机制仍不清楚。 为了解析MMD1介导减数分裂特异染色体浓缩进程的调控机制,研究人员从2010年开始构建不同的MMD1截短蛋白并筛选文库,于2011年鉴定到其中一个互作因子JMJ16,其编码一个H3K4的组蛋白去甲基化酶(图 1)。研究团队与该领域专家、中科院遗传与发育生物学研究所曹晓风院士合作,证明了JMJ16体内体外只能去除H3K4me2/3。已有研究表明,启动子区域该组蛋白修饰主要促进基因的表达,去除则抑制基因的表达,这将无法解释与MMD1互作而促进CAP-D3基因的表达。
为了解析MMD1介导减数分裂特异染色体浓缩进程的调控机制,研究人员从2010年开始构建不同的MMD1截短蛋白并筛选文库,于2011年鉴定到其中一个互作因子JMJ16,其编码一个H3K4的组蛋白去甲基化酶(图 1)。研究团队与该领域专家、中科院遗传与发育生物学研究所曹晓风院士合作,证明了JMJ16体内体外只能去除H3K4me2/3。已有研究表明,启动子区域该组蛋白修饰主要促进基因的表达,去除则抑制基因的表达,这将无法解释与MMD1互作而促进CAP-D3基因的表达。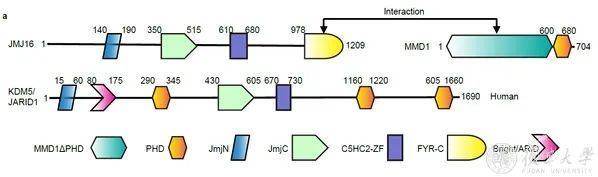 图1 MMD1和JMJ16蛋白的结构域及相互作用区域研究人员推测,MMD1可能影响了JMJ16的酶活。体内体外实验均证明MMD1确实调控了JMJ16的底物特异性, MMD1-JMJ16复合体可以去除肽段和核小体上的H3K9me3。那么MMD1又是如何调控了JMJ16的底物特异性呢?构建两个蛋白质的不同截短蛋白,鉴定出MMD1的MMD结构域(自定义,植物中保守)与JMJ16的C端FYR-C结构域互作(图 1),暗示着JMJ16的C端可能影响了其酶活结构域。为了验证这个假设,研究人员表达了只含有JMJ16-N端催化结构域的截短蛋白,发现JMJ16-N可以同时识别和去除H3K4me3和H3K9me3。进一步体外证明JMJ16-N和JMJ16 的C端FYR-C结构域相互作用,体内FRET实验也支持JMJ16的两端靠的很近或直接互作(图2)。
图1 MMD1和JMJ16蛋白的结构域及相互作用区域研究人员推测,MMD1可能影响了JMJ16的酶活。体内体外实验均证明MMD1确实调控了JMJ16的底物特异性, MMD1-JMJ16复合体可以去除肽段和核小体上的H3K9me3。那么MMD1又是如何调控了JMJ16的底物特异性呢?构建两个蛋白质的不同截短蛋白,鉴定出MMD1的MMD结构域(自定义,植物中保守)与JMJ16的C端FYR-C结构域互作(图 1),暗示着JMJ16的C端可能影响了其酶活结构域。为了验证这个假设,研究人员表达了只含有JMJ16-N端催化结构域的截短蛋白,发现JMJ16-N可以同时识别和去除H3K4me3和H3K9me3。进一步体外证明JMJ16-N和JMJ16 的C端FYR-C结构域相互作用,体内FRET实验也支持JMJ16的两端靠的很近或直接互作(图2)。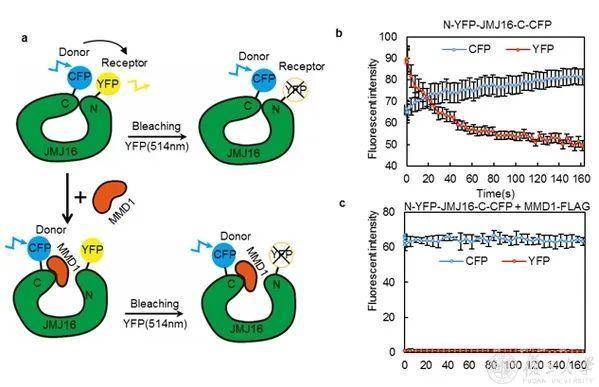 图2 JMJ16-N和-C端互作及MMD1对其互作的影响那么MMD1是如何影响JMJ16蛋白两端的互作呢?通过体外竞争实验表明MMD1可以和JMJ16-N竞争性的结合FYR-C结构域,从而解除FYR-C对于JMJ16-N的抑制效应,体内FRET-bleaching实验揭示MMD1可以拉开JMJ16的N端和C端的距离,解除其抑制作用 (图 2)。以上结果证明,JMJ16-C端结构域可能抑制了其N端催化结构域识别H3K9me3,而MMD1可以与JMJ16的C端竞争结合,可能通过锌指结构域(C5HC2)解除自抑制效应 (图 3),促进JMJ16识别和去除H3K9me3。
图2 JMJ16-N和-C端互作及MMD1对其互作的影响那么MMD1是如何影响JMJ16蛋白两端的互作呢?通过体外竞争实验表明MMD1可以和JMJ16-N竞争性的结合FYR-C结构域,从而解除FYR-C对于JMJ16-N的抑制效应,体内FRET-bleaching实验揭示MMD1可以拉开JMJ16的N端和C端的距离,解除其抑制作用 (图 2)。以上结果证明,JMJ16-C端结构域可能抑制了其N端催化结构域识别H3K9me3,而MMD1可以与JMJ16的C端竞争结合,可能通过锌指结构域(C5HC2)解除自抑制效应 (图 3),促进JMJ16识别和去除H3K9me3。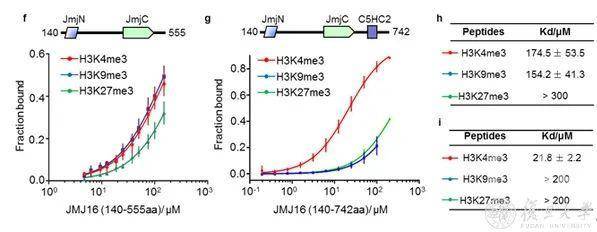 图3 荧光偏振鉴定 JMJ16酶活结构域及含锌指结构域对H3K4me3和H3K9me3的结合强度jmj16的减数分裂细胞转录组测序发现,叶片中主要是抑制相关功能基因的表达,而减数分裂细胞中表现和MMD1共同促进一批基因的表达,包括染色体浓缩相关基因。分析目的基因如CAP-D3的启动子区域组蛋白修饰,发现H3K4me1/2/3 变化不显著,而H3K9me3显著增加。由于动物中JMJ16的同源蛋白KDM5/JARID本身含有PHD结构域,研究人员推测JMJ16的定位可能依赖MMD1的PHD结构域识别H3K4me3,而MMD1的MMD结构域招募JMJ16,进而影响其底物特异性,最后调控了目的基因的表达。为了验证这一假设,研究人员构建了JMJ16的酶活结构域融合MMD1的PHD结构域并转化到mmd1的突变体,发现可以部分恢复mmd1染色体浓缩异常的表型。
图3 荧光偏振鉴定 JMJ16酶活结构域及含锌指结构域对H3K4me3和H3K9me3的结合强度jmj16的减数分裂细胞转录组测序发现,叶片中主要是抑制相关功能基因的表达,而减数分裂细胞中表现和MMD1共同促进一批基因的表达,包括染色体浓缩相关基因。分析目的基因如CAP-D3的启动子区域组蛋白修饰,发现H3K4me1/2/3 变化不显著,而H3K9me3显著增加。由于动物中JMJ16的同源蛋白KDM5/JARID本身含有PHD结构域,研究人员推测JMJ16的定位可能依赖MMD1的PHD结构域识别H3K4me3,而MMD1的MMD结构域招募JMJ16,进而影响其底物特异性,最后调控了目的基因的表达。为了验证这一假设,研究人员构建了JMJ16的酶活结构域融合MMD1的PHD结构域并转化到mmd1的突变体,发现可以部分恢复mmd1染色体浓缩异常的表型。 图4 JMJ16和MMD1在不同细胞微环境中调控基因表达的模型基于上述结论,研究人员提出了JMJ16和MMD1在体细胞和减数分裂细胞中调控基因表达的模型。在体细胞中,JMJ16的N端和C端互作,抑制了其识别H3K9me3的能力,只具有H3K4me3去甲基化活性,从而抑制包括FLC在内的基因表达(图4 a)。而在减数分裂细胞中,MMD1的PHD识别H3K4me3,而MMD结构域与JMJ16的FYR-C互作,解除了其自身C端和N端的互作,拓展了JMJ16的H3K9me3去甲基化活性,从而促进包括CAP-D3在内的基因表达,确保减数分裂染色体的正确浓缩(图4 b)。该结果也是第一次证明了含有JmjC结构域的去甲基化酶酶活底物特异性的调控机制,揭示了去甲基化酶在不同的细胞微环境中可能与不同互作因子协同精确调控相关基因的表达,且这种调控机制可能具有普遍性。王应祥、麻锦彪和马红是本研究的共同通讯作者。复旦大学已毕业博士生王君和余超逸为本文的共同第一作者。中科院遗传与发育研究所曹晓风院士和张率斌博士合作参与了工作。该项目得到国家自然科学杰出青年基金、国家重点基础研究计划项目和复旦大学遗传工作国家重点实验室的大力支持。
图4 JMJ16和MMD1在不同细胞微环境中调控基因表达的模型基于上述结论,研究人员提出了JMJ16和MMD1在体细胞和减数分裂细胞中调控基因表达的模型。在体细胞中,JMJ16的N端和C端互作,抑制了其识别H3K9me3的能力,只具有H3K4me3去甲基化活性,从而抑制包括FLC在内的基因表达(图4 a)。而在减数分裂细胞中,MMD1的PHD识别H3K4me3,而MMD结构域与JMJ16的FYR-C互作,解除了其自身C端和N端的互作,拓展了JMJ16的H3K9me3去甲基化活性,从而促进包括CAP-D3在内的基因表达,确保减数分裂染色体的正确浓缩(图4 b)。该结果也是第一次证明了含有JmjC结构域的去甲基化酶酶活底物特异性的调控机制,揭示了去甲基化酶在不同的细胞微环境中可能与不同互作因子协同精确调控相关基因的表达,且这种调控机制可能具有普遍性。王应祥、麻锦彪和马红是本研究的共同通讯作者。复旦大学已毕业博士生王君和余超逸为本文的共同第一作者。中科院遗传与发育研究所曹晓风院士和张率斌博士合作参与了工作。该项目得到国家自然科学杰出青年基金、国家重点基础研究计划项目和复旦大学遗传工作国家重点实验室的大力支持。来源:frontiersin 植物科学最前沿
原文链接:https://mp.weixin.qq.com/s?__biz=MzIyOTY2NDYyNQ==&mid=2247497282&idx=5&sn=51056b1b22ad9a993aa9d511eb034944&chksm=e8bd845cdfca0d4a91dc790781da7475839da294fc1141ead6875888a71ce34821656cbefe4b#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
染色体原位杂交
结构域
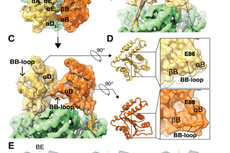
研究揭示了TNLs的直接结合、寡聚和TIR结构域激活机制

中国海洋湖沼学会理事张奇研究员主持的《鄱阳湖水文情势变化研究》出版发行
眼睛出现这种情况,可能是帕金森病的早期征兆?
分子细胞卓越中心构建染色体融合小鼠模型、模拟染色体演化过程

中国科学院南京地理与湖泊所在湖泊沉积物碳埋藏研究取得进展
染色体结构畸变

为何卢浮宫博物馆地下有台粒子加速器?
无性也能繁衍1800万年! 蠕虫基因测序解密