科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-07-09
来源:BioArt植物
miRNA是一类长度在20-24碱基的内源小分子RNA,在动植物生长发育、细胞命运决定和转换、以及环境应答等几乎所有生物学过程中发挥重要作用。miRNA初级转录本(称为pri-miRNA)可以折叠成茎区不完全配对的发夹结构,该结构可被RNase III家族核酸内切酶识别并切割后释放出成熟的双链miRNA/miRNA*。和动物相比,植物 pri-miRNA的茎环区长度变异更大(从60 nt到超过500 nt,动物中一般为~70 nt),从而增加了茎环结构的复杂性。因此植物除了经典的基部到环的加工方式,不少miRNA以环到基部的切割方式成熟,有些长的pri-miRNA还存在两次以上的连续切割 (图1)。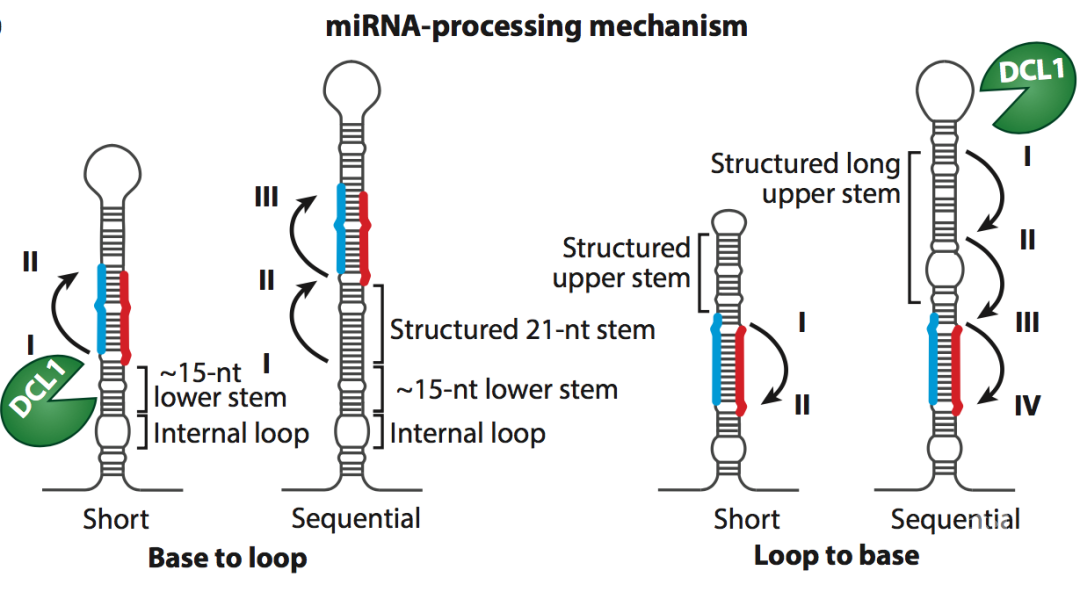 图1、植物miRNA的两种加工机制(Bologna and Voinnet, 2014 )
图1、植物miRNA的两种加工机制(Bologna and Voinnet, 2014 )
在植物中,DCL1在HYL1和锌指蛋白SE等的帮助下负责绝大多数miRNA的加工成熟。HYL1被认为是DCL1最重要的伴侣分子,推测其在miRNA加工过程中的功能类似于动物miRNA生成中Drosha的伴侣蛋白DGCR8和Dicer的伴侣蛋白TRBP。已有的研究表明,HYL1有助于提高DCL1加工的效率和准确性,但其具体的作用机制以及HYL1是否还有其他生物学功能仍不清楚。
近日,复旦大学遗传工程国家重点实验室任国栋研究员课题组在PNAS上发表了题为Hyponastic Leaves 1 protects pri-miRNAs from nuclear exosome attack的研究论文。该研究揭示了拟南芥双链RNA结合蛋白 HYL1在 miRNA加工成熟过程中保护底物分子(pri-miRNA及其加工过程中间产物)免受核酸外切体(exosome)攻击的新机制,并发现HYL1可能在DCL1介导的由环到基部(Loop-to-base)和基部到环(Base-to-loop)成熟的pri-miRNAs 加工过程中发挥不同作用。
外切体是生物体最主要的负责各类RNA降解的蛋白质机器,在rRNA加工成熟、正常RNA周转降解以及非正常RNA(如错误转录本、RNA加工副产物、靶基因切割产物等)的及时清除等细胞基本生命活动过程中发挥关键作用。外切体核心复合物共含9个蛋白(Exosome 9,exo9),在古菌和真核生物中高度保守。核心复合物通过与不同辅助因子互作参与不同RNA底物的识别和降解。根据亚细胞定位的不同,外切体可分为胞质外切体与核内外切体,核内外切体又分为核仁外切体与核质外切体。RNA解旋酶SKI2、MTR4以及HEN2分别是胞质外切体、核仁外切体与核质外切体的重要辅助成员。
该研究通过正向遗传学筛选hyl1-2的表型抑制子,结合图位克隆分离鉴定到核质外切体的另一辅助因子SOP1。SOP1蛋白C端含有5个串联的CCCH型锌指结构,可能与RNA结合有关。SOP1与HEN2共定位,参与部分核质外切体靶标RNA的降解。在hyl1-2中引入HEN2的突变同样可以显著抑制hyl1-2的发育缺陷,表明SOP1和HEN2很可能是通过外切体途径参与miRNA调控的 (图2A)。通过对miRNA以及pri-miRNA的联合分析发现,hyl1 sop1 双突变体中加工方向为环到基部的pri-miRNA较hyl1有更高的积累,对应成熟miRNA表达水平得到了显著回复,表明SOP1选择性参与hyl1突变体中加工方向为环到基部的pri-miRNA降解(图2B & C)。令人惊讶的是,hyl1 hen2双突变体中几乎所有的pri-miRNA均显著累积,但是只有环到基部成熟的miRNA得到了回复(图2B & C)。该研究结果表明当HYL1缺失时,环到基部加工的pri-miRNA的更多累积可以促进miRNA的生成,而基部到环加工的pri-miRNA则不能。加工复合体成员SE能够与HEN2相互作用,猜测可能在招募外切体中发挥功能。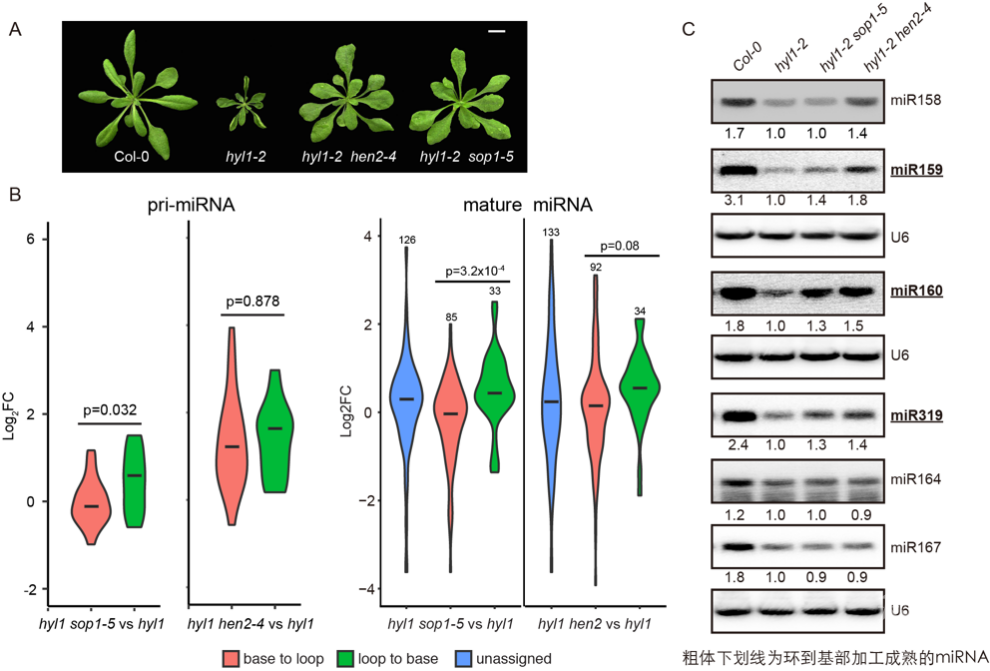 图2、HYL1拮抗核内外切体,确保pri-miRNA加工顺利进行。
图2、HYL1拮抗核内外切体,确保pri-miRNA加工顺利进行。
综上,该研究揭示了外切体在pri-miRNA生物发生中的监控作用以及加工复合体核心成员HYL1的保护功能,拓展了我们对于加工过程中pri-miRNA质量控制机制的认识。此外,该研究还系统鉴定了受HEN2、SOP1影响的差异表达基因,这些基因可作为核质外切体功能的标志基因。
来源:bioartplants BioArt植物
原文链接:https://mp.weixin.qq.com/s?__biz=MzU3ODY3MDM0NA==&mid=2247496691&idx=1&sn=350b1e3e41f28f29346ac2112eb96b8e&chksm=fd736994ca04e082e298348a323879c7f653134aa5f80167cb5ad64270693998afe4a3e4e4bf#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
细胞粘附分子
新分子图谱揭示脑细胞发育轨迹
《细胞》发文!阿片类药物迎来重大突破
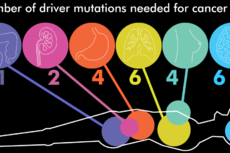
从健康细胞到癌细胞,或许只需要几个突变

人类白细胞用分子“桨”游泳
一个小小的细胞就有多达4200万个蛋白质分子

用AIE分子打造细胞“照妖镜”,可区分细胞系、评估细胞污染和鉴别癌细胞

人工细胞与生物细胞首次实现成功融合与协作
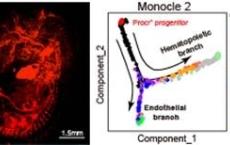
分子细胞卓越中心揭示胚胎血管内皮祖细胞身份
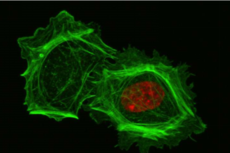
失去细胞核的细胞在3D环境中举步维艰