科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-08-17
来源:X一MOL资讯
将精确的诊断影像模式与治疗模式巧妙结合,构建多模式肿瘤诊疗一体化的系统,从而使传统医疗向“综合化”、“精准化”和“个性化”的多模式诊疗一体化的医疗策略转变,是现代医学技术的创新之举和发展趋势。在各种癌症诊断的方法中,荧光成像(PLI)由于其即时性、高分辨率、高灵敏度等优势,在细胞和活体的无损实时跟踪研究中是一个不可或缺的工具。光疗法包括光动力疗法(PDT)和光热疗法(PTT),是一种光可控、无创、无耐药性的治疗手段。其中,高效的光敏剂是实现光动力治疗的关键;与传统光敏剂相比,具有聚集诱导发光(AIE)特征的分子表现出较高的荧光强度、光稳定性以及单线态氧产生效率,且有报道表明在聚集态下可以增强ROS。PTT过程中产生的热信号也可以通过光热成像系统(PTI)捕获,实现PTI指导PTT研究。黑磷纳米片是近年来新兴的二维纳米材料,因其高效的载药能力和光热转换效率,以及其优异的生物相容性和可降解性,可作为光热剂用于PTI指导的PTT研究。但是,由于PDT肿瘤微环境的缺氧性和PTT的热休克效应,PDT或PTT单独使用难以获得令人满意的效果。而将PDT和PTT结合被认为是突破性的改进,可以克服各自的缺点并发挥协同增强的治疗效果。例如,PTT的过热效应可促进光敏剂的摄取和通过提高血流量改善肿瘤组织的供氧,从而增强PDT效应,进一步消除PTT中的耐热肿瘤细胞。
基于AIE光敏剂和二维黑磷纳米片表现出的优异的性质,香港科技大学唐本忠院士团队深圳大学AIE研究中心王东副教授近日在Advanced Materials 发表了论文,首次将AIE光敏剂联合二维黑磷纳米片简便构建获得一种新型的多模式诊疗一体化的纳米材料(图1)。该纳米材料(BP@PEG-TTPy)充分展现联合的二者组分优势互补,同时显示出优异的稳定性和生物相容性、明亮的近红外区(NIR)荧光发射、高效的活性氧(ROS)生成和光热转换效率、以及快速的细胞摄取能力和肿瘤组织的显著积聚。体外和体内评价实验表明该纳米材料在光照下实现了“1+1>2”的效果,表现出高效的FLI-PTI成像指导的PDT-PTT协同治疗,相比于单一的PDT或PTT有显著的提高。这项研究不仅扩展了AIE分子和黑磷材料的应用范围,而且为设计新一代癌症诊疗方案提供了新的思路。

图1. BP@PEG-TTPy纳米材料的制备和诊疗示意图。
在这项工作中,作者将带正电荷、亲水性的AIE光敏剂(NH2-PEG-TTPy)与表面带负电荷的黑磷纳米片(BP nanosheets)在水中通过静电相互作用结合,实现了二者组分的优势互补。该设计的优势主要表现为:(1)NH2-PEG-TTPy作为稳定剂提高了黑磷纳米片的稳定性;(2)黑磷纳米片作为载体平台高效负载NH2-PEG-TTPy;(3)BP@PEG-TTPy纳米材料兼具二者的多功能性,例如NH2-PEG-TTPy在低功率的白光辐照下所赋予的NIR荧光发射、有效的活性氧(ROS)生成,黑磷纳米片在NIR(808 nm)激光辐照下所赋予的高效的光热转换效率及其所带来的PTI成像指导的PTT治疗;(4)NH2-PEG-TTPy中的氨基和带正电荷的吡啶官能团,分别有利于其从酸性的溶酶体环境中逃逸,并进一步靶向到线粒体;(5)BP@PEG-TTPy合适的纳米尺寸(~100 nm)促进其通过EPR效应在肿瘤组织中富集。
在实验结果部分,作者首先证实了NH2-PEG-TTPy与黑磷纳米片的成功复合,进一步的理化研究结果表明BP@PEG-TTPy具有宽的紫外区至近红外区吸收、强的NIR区荧光发射及优异的光热稳定性(图2)。
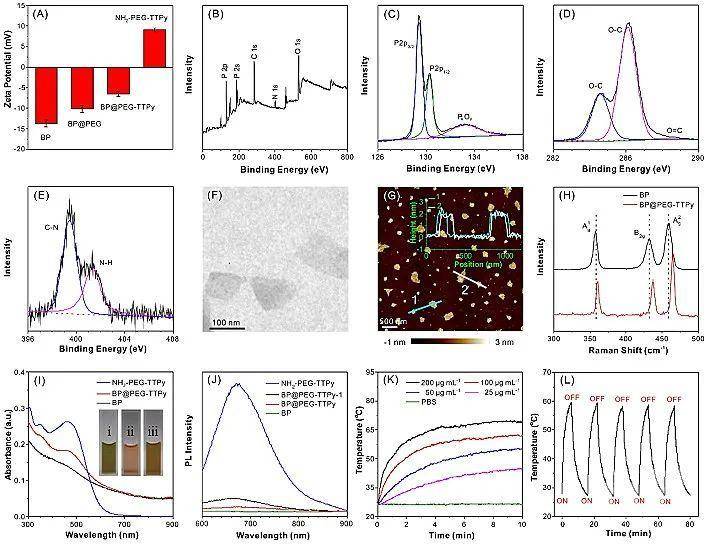
图2. BP@PEG-TTPy的理化性质表征。
BP@PEG-TTPy可以高效的产生ROS,细胞毒性实验表明其没有按毒性,且在双重光照条件下具有高效的PDT-PTT协同治疗效果(图3),远优于单一的PDT和PTT。通过分别与商用染料共染4T1细胞探究其高效治疗机制。荧光共定位分析表明,BP@PEG-TTPy进入到细胞后首先达到溶酶体,随后在溶酶体酸性环境下部分解离,解离的NH2-PEG-TTPy由于质子海绵效应从溶酶体中逃逸,在其分子结构中的正电荷的吡啶官能团协助下,通过静电相互作用靶向到线粒体。从而在双重光照条件下,实现高效的溶酶体和线粒体双重损伤,获得优异的PDT-PTT协同治疗效果。进一步通过裸鼠体内4T1皮肤荷瘤模型,研究其体内诊疗效果,结果表明BP@PEG-TTPy在双重光照下实现了高效的FLI-PTI成像指导的PDT-PTT协同治疗,相比于单一的PDT或PTT有显著的提高。

图3. BP@PEG-TTPy的ROS产生与细胞内PDT-PTT治疗效果及其机理研究。
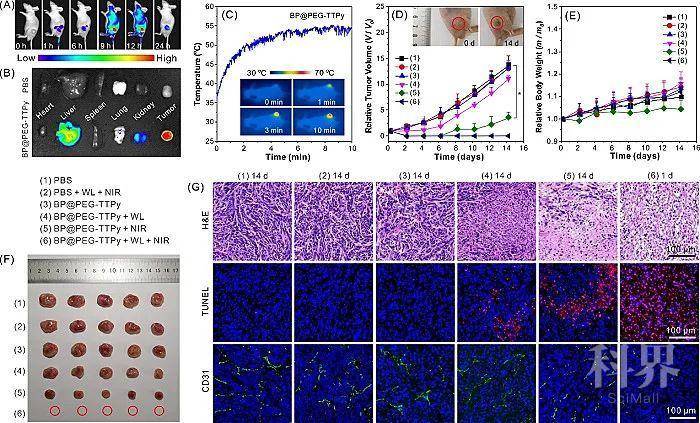
图4. 体内FLI-PTI成像指导的PDT-PTT协同治疗。
论文第一作者为深圳大学AIE研究中心博士后黄佳昌,通讯作者为香港科技大学唐本忠院士和深圳大学AIE研究中心王东副教授。课题得到了南方科技大学李凯副教授及其团队的大力支持。
Aggregation-Induced Emission Luminogens Married to 2D Black Phosphorus Nanosheets for Highly Efficient Multimodal Theranostics
Jiachang Huang, Benzhao He, Zhijun Zhang, Youmei Li, Miaomiao Kang, Yuanwei Wang, Kai Li, Dong Wang,* Ben Zhong Tang*
Adv. Mater., 2020, DOI: 10.1002/adma.202003382
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657654888&idx=6&sn=1011201b4dd70dc71d7292bffe8360f0&chksm=80f8b1b8b78f38aefc959abe328cd2950d42da61c4ea6382b68390e2cd184447d50d464a9f77&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

【走近桂籍科学家】用纳米武装电池新世界
新研究为二维材料纳米力学测试建立有效策略

层状二维材料缺陷位纳米空间分辨表征

Adv. Energy Mater.:限域合成二维纳米能源材料
中国—奥地利纳米科技及新材料研讨和对接洽谈会在深圳举行




中国微米纳米技术学会第十八届学术年会暨微系统与纳米工程高层论坛

二维材料,又发Nature!

《先进材料》评述:仿生二维纳米材料在可持续应用方面的进展
宁波材料所在二维纳米防护薄膜材料方面取得进展

二维纳米材料非线性光学特性研究取得进展