科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-03-30
来源:X-MOL(x-mol.com)
以用于治疗化疗中恶心、呕吐症状的药物格拉司琼(Granisetron)以及抗心律失常诊断用药/天然产物阿义马林(ajmaline)为典型代表,9-氮杂双环[3.3.1]壬烷桥环骨架广泛存在于天然产物和药物分子中(图1a)。在合成化学上,该类桥环结构的构建具有较大的挑战性。目前已知的方法具有原料昂贵、需多次官能团引入和转换、后期天然产物衍生较难等不足(图1b)。
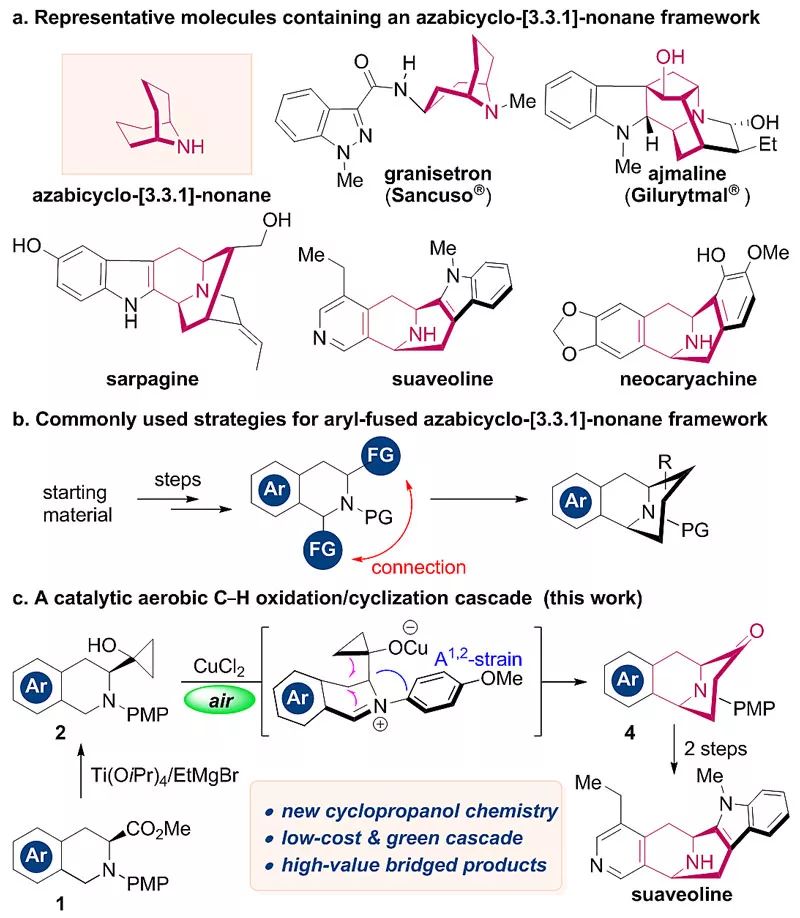
图1. 背景介绍和方法学概括
重庆大学药学院张敏研究员团队致力于发展新配体(J. Am. Chem. Soc., 2019, 141, 961)和新合成方法(Angew. Chem. Int. Ed., 2017, 56, 4829; Angew. Chem. Int. Ed., 2018, 57, 937),并应用于活性药物分子和天然产物复杂多环骨架和相邻手性季碳的构建。该团队在首次发现铜催化环丙烷醇开环亚胺离子加成的基础上,发展了一种铜催化的C-H键氧化环合串联反应新方法,实现了9‒氮杂双环[3.3.1]壬烷桥环骨架快速构建(图1c)。该方法使用手性苯丙氨酸为起始原料,使用廉价的催化剂(CuCl2)和氧化剂(空气),具有经济、绿色等优点。该反应具有较好的底物普适性,含有取代苯环(F、Cl、Br、MeO-、Me等)以及噻吩和呋喃的底物均可较好地兼容,也可适用于中环氮杂双环[4,3,1]癸烷桥环结构的构建(图2)。
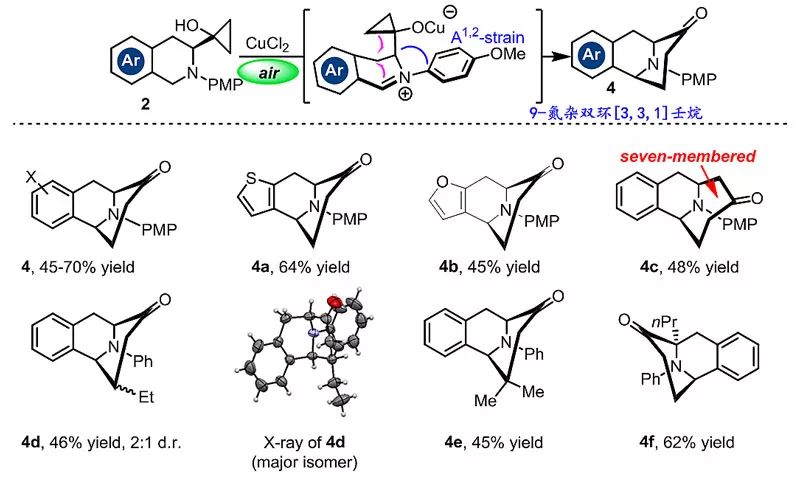
图2. 9‒氮杂双环[3.3.1]壬烷桥环结构的构建
作为该方法学的天然产物全合成应用,该团队以市售可得的L‒高丝氨酸(5)为起始原料,经9步的总步数,快速完成了(−)-suaveoline的不对称全合成(图3)。
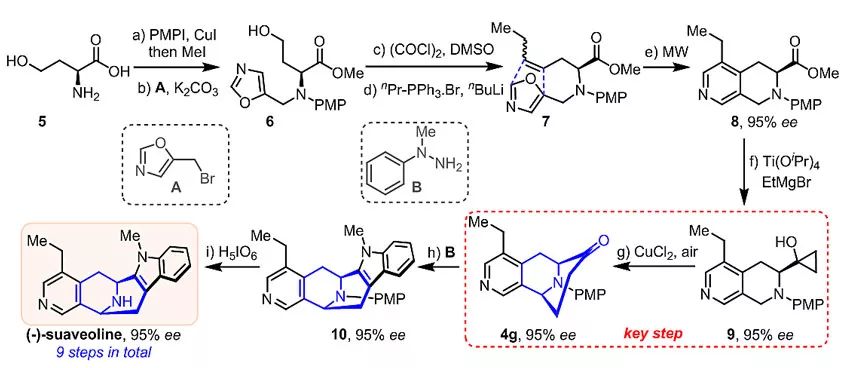
图3. (−)-Suaveoline的不对称全合成
经过机理研究,作者提出了可能的反应机理(图4)。催化剂CuCl2发挥了催化循环A和B两种催化作用。1)环丙烷醇2在Cu(II)作催化剂、空气为氧化剂的条件下被氧化成亚胺离子A,随后被分子内环丙烷醇的氧原子捕获,生成环丙烷结构保持的杂缩醛11(X-ray)。2)杂缩醛在Cu(II)作为路易斯酸的条件下开环形成亚胺离子B,环丙烷醇经过自由基开环,形成自由基中间体C。为了减少A1,2张力,取代基处于接近垂直键的构象,从而利于桥环结构的产生。自由基中间体C对亚胺加成形成自由基正离子D后,Cu(I)转移一个电子将自由基正离子D还原成最终的产物4后变为Cu(II)并完成催化循环B。相较于催化循环A,催化循环B较缓慢,是一个氧化还原中性反应,不需要额外的氧化剂参与。
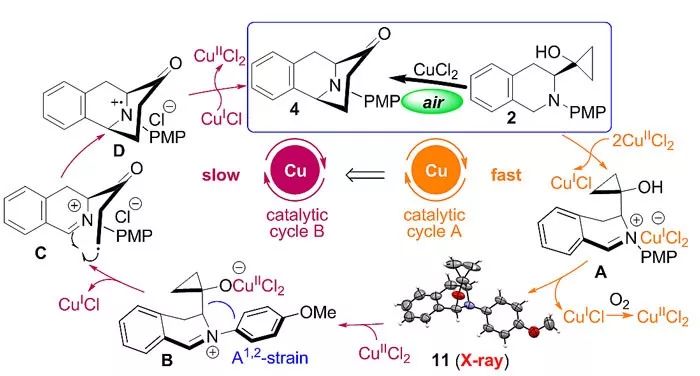
图4、假设的机理
相关成果于近日发表于Angew. Chem. Int. Ed.,博士研究生谭秋元(本科毕业于重庆理工大学)和杨钊(硕士毕业于北京工业大学)为文章的共同第一作者。
该论文作者为:Qiuyuan Tan, Zhao Yang, Dan Jiang, Yuegang Cheng, Jiao Yang, Song Xi, Min Zhang
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657608579&idx=5&sn=9a51f963f0cbd0f759b6d15c3f7df222&chksm=80f7ca53b7804345ffc40e7fd691192f4c437478386589b0d14f35c881c16c9c833a7de34715&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn