科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-04-16
来源:X一MOL资讯
锂-氧电池中放电产物过氧化锂的氧化机制和分解界面的研究对于电极催化剂的设计至关重要,但已报导的文献对这一问题存在颇多争议,这使得电极催化剂的设计缺少普遍认可的理论基础。
最近,香港中文大学的卢怡君教授(Yi-Chun Lu)及其团队采用同位素标记法以及原位质谱,首次揭示了在常规电池操作条件下过氧化锂的分解界面,并提出了催化剂的作用机理,为锂-氧电池的材料设计提供了有效的理论依据。
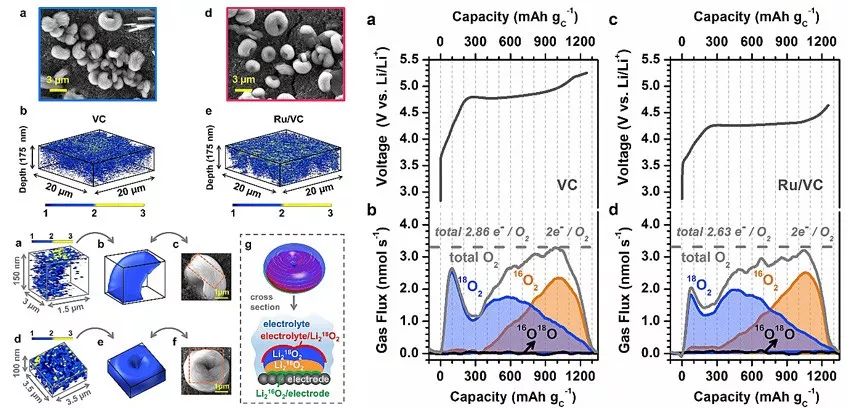
对于过氧化锂分解界面的研究,以往文献所使用的方法大多偏离锂-氧电池的实际情况。例如,采用原位光谱学方法得出的结论往往基于过氧化锂是均匀分布的膜状物,而在实际电池中人们观察到的常常是微米级的颗粒;又如,采用原位电镜研究时所施加的电位通常远远偏离锂-氧电池的正常工作电位,这些因素造成了人们对过氧化锂分解界面的认识存在诸多分歧。为此,卢怡君教授团队采用同位素标定法模拟真实锂-氧操作条件,研究了过氧化锂的分解界面。研究人员将组装成的锂-氧电池依次在普通氧气(16O2)和同位素氧气(18O2)中放电,构筑了一种壳为Li218O2核为Li216O2的颗粒产物结构。二次离子质谱表明,Li218O2主要集中在产物的表面,也就是与电解液接触的界面,Li216O2主要集中在产物的内部,也就是与电极材料接触的界面。在充电过程中,同位素氧气(18O2)首先逸出,常规氧气(16O2)随后逸出。这表明,过氧化锂的分解是在电解液/过氧化锂颗粒的界面进行的。

研究人员认为,在充电伊始,过氧化锂首先与催化剂形成了一层稳定的界面,这一界面使得过氧化锂/电极界面的氧原子被稳定而不易脱离,然后锂离子从过氧化锂的外表面迁移至过氧化锂/电极的界面,同时氧气从过氧化锂颗粒的外表面逸出。这一说法提出了催化剂的作用机制,同时解释了过氧化锂从电解液/过氧化锂界面分解的内在原因。同时,这种同位素标定加上质谱分析的方法为人们研究金属-空气电池的反应机制提供了新的思路。
相关结果发表 Angewandte Chemie International Edition 上,文章的第一作者是香港中文大学的王余博士。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657609637&idx=4&sn=2bdca2a14745242b28b3ead10f4fdc09&chksm=80f7ce75b7804763a04500b349204055df6b014acf68f078f082565f7f045a127fda123473bf&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
电化学沉积

Science:无需电解液的离子晶体管

青岛能源所成功制备柔性载硫体用于高性能锂硫电池----中国科学院
锂硫电池电解液: 发展、前景与挑战

电解液界面不稳定,要如何表征?
光电化学刻蚀
电化学灌浆
电化学效率
合肥研究院利用功能化碳纳米管材料实现对水稻伤流液中重金属离子的选择性检测----中国科学
电化学位能