科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-05-20
来源:研之成理
全文速览
本文利用 AuRu 核-天线纳米结构在光照下产生的等离激元效应,实现了在温和条件下 N≡N 键的解离。结合近常压 XPS 以及理论模拟研究发现,等离激元效应产生的热电子、局域电场增强效应以及催化剂 -N2 轨道杂化后的直接能量转移共同促进了反应过程中 N2 分子的直接解离。
背景介绍
众所周知,氨的合成对于农业生产和化工工业来说至关重要。虽然大气中约 78 % 的成分都是 N2,但是 N2 分子中非极性 N≡N 键的键能高达 941 kJ/mol,导致催化剂在温和条件下对 N2 分子的活化非常困难。目前合成氨工业中所采用的 Haber-Bosch 方法需要在大于 300 °C 的高温和超过 100 个大气压的严苛条件下进行,这造成了极大的能源消耗。实际上,目前合成氨所消耗的能量占全球总能耗的 1 % 以上,因此发展可持续的方法来实现温和条件下的高效固氮反应具有非常重要的意义。
近年来,以 Au 为代表的等离激元金属纳米材料在实现温和条件下太阳能向化学能的转化中大放异彩,受到了研究者的广泛关注。Au 纳米结构可以与可见光产生强烈的相互作用,激发表面局域等离激元共振效应,将远大于自身几何截面的光能集中在很小的范围内,并通过能量转移引起强烈的光-物质的相互作用,在实现太阳能到化学能的转化方面很有潜力。
研究出发点
近期光催化和电催化固氮反应上的取得的一系列研究成果为模拟自然条件下氨的合成提供了可能。然而在光催化和电催化过程中,转移到 N2 分子上的电子因为没有足够的能量直接解离 N≡N 键,通常采取逐步解离加氢的反应路径。虽然逐步解离的反应路径为减少固氮反应中能量的消耗提供了重要的选择,但是研究温和条件下 N2 分子的直接解离对理解固氮反应中的基本问题同样非常重要,并且相关成果也可以为传统催化剂的改进提供一些思路(例如减少在 Haber-Bosch 过程中的能量投入)。
为了实现在温和条件下 N≡N 键的解离,我们必须要从全新的角度对催化剂进行设计。虽然等离激元催化剂可以在温和条件驱动许多化学反应的发生,但是 Au 自身对 N2 较弱的吸附活化能力限制了其在光驱动固氮反应中的进一步应用。金属 Ru 作为在合成氨反应中最早研究的金属催化剂之一,其在 N2 的吸附和活化中具有良好催化性能。
熊宇杰教授/龙冉副教授团队设想是否可以结合 Au 和 Ru 各自在吸光和 N2 分子活化方面的优势,实现温和条件下的固氮反应。作者结合实验室在材料合成方面的优势,通过大量尝试,最终成功地通过一步法就可以获得 AuRu 摩尔比可调的核-天线纳米结构催化剂,该催化剂在光照下成功地驱动了 N2 分子的解离,实现了温和条件下的固氮反应。
图文解析
通过 TEM、EDS-mapping 以及 EXAFS 等表征方法,确认了催化剂样品的核-天线纳米结构,实验结果表明 Au 元素主要富集在内部的核结构中,而 Ru 元素则主要富集在表面的天线结构中。
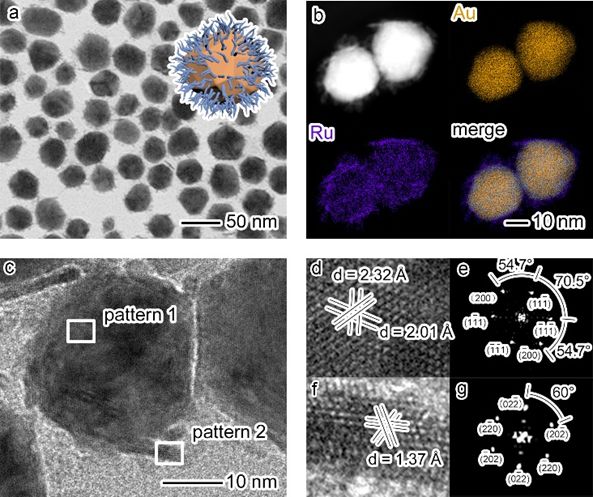
▲Figure 1 (a) TEM image of AuRu0.31 core-antenna nanostructures. (b) EDS elemental mapping profiles of AuRu0.31 nanostructure showing the distribution of Au (orange) and Ru (purple) elements. (d) Magnified HRTEM image and (e) corresponding FFT pattern taken from pattern 1. (f) Magnified HRTEM image and (g) corresponding FFT pattern taken from pattern 2.
为了评估该催化剂在固氮反应中的性能,作者在 2 atm 的 N2 气氛以及 400 mW·cm-2 全谱光照下对一系列具有不同 Au/Ru 摩尔比例的 AuRu 核-天线纳米结构催化剂在纯水中的固氮性能进行了测试。阳离子色谱的测试结果(Figure 2a)表明,当样品中 Ru 的摩尔比例逐渐提高时,得益于催化位点的增多,氨的产率随之上升。在不加任何牺牲剂的纯水中,AuRu0.31 样品的固氮性能大约是纯 Au 颗粒的 7.3 倍,最高可以达到 101.4 μmol·g-1·h-1。不过当 Ru 的摩尔比例继续提高时,由于样品的吸光能力受到了较为明显影响,催化剂的性能反而有所降低。此外,为了探究产物氨中氮的来源,作者使用 15N 同位素标记的 15N2 进行了固氮反应,通过 1H-NMR(Figure 2b)确认了产物氨中的氮确实来源于反应所使用的氮气。

▲Figure 2 (a) Catalytic ammonia production rates by bare Au, AuRu0.14, AuRu0.23, AuRu0.31 and AuRu0.39 in the first 2 hours (full-spectrum, 400 mW∙cm-2, pure water, 2 atm N2). (b) 1H-NMR (400 MHz) spectra of solution after N2 fixation reaction using AuRu0.31 as a catalyst in 15N2, 15N2+14N2 or 14N2 atmosphere.
作者进一步对催化剂表面 N2 分子的吸附活化过程进行了深入探究,首先采用低温傅里叶变换红外光谱(LT-FTIR)对 N2 分子的吸附振动模式进行了表征(Figure 3a)。在催化剂吸附 N2 分子之后,一个较宽的红外吸收峰出现在 2248 cm-1 处,这与垂直吸附的振动信号相符。
随后作者利用原位傅里叶变换红外光谱(in-situ DRIFTS)对 AuRu0.31 催化剂表面 N2 还原的催化过程进行了监测(Figure 3b)。将湿润的 N2 引入反应体系之后,随着光照时间的增加, 3000–3600 cm-1 处的 N-H 键伸缩振动信号逐渐增强。此外,在 1404 cm-1 处出现的吸收峰可以归属为光照下产生的 NH4+ 的变形振动峰。以上结果证明了在光照和水分子存在的情况下 AuRu0.31 样品可以催化 N2 分子转化为氨。对比实验中,使用 Ar 替代 N2 进行实验时并未发现上述 N-H 信号。值得一提的是,在 Figure 3b 中并未出现 N2Hy 中 N-N 振动的信号(位于 1100-1300 cm-1),这说明该体系经历的固氮反应路径与光催化和电催化过程中 N2 分子逐步解离加氢的路径有所不同。
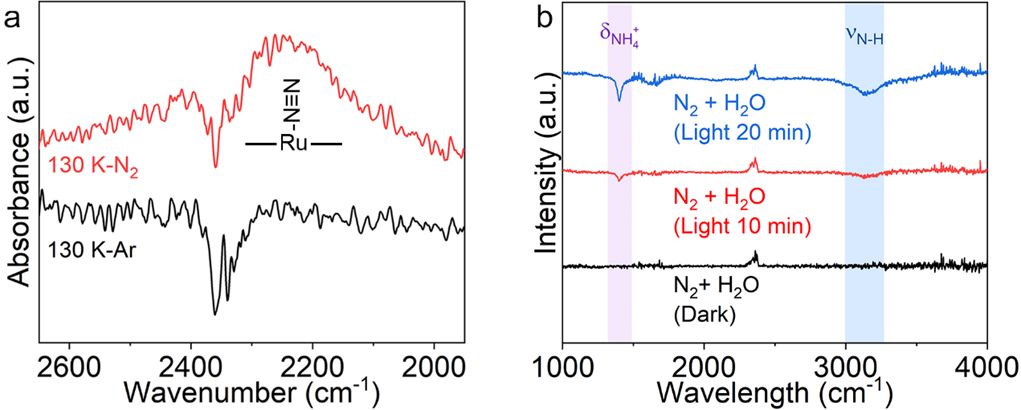
▲Figure 3 (a) LT-FTIR spectra of N2 molecules after N2 adsorption on AuRu0.31 at 130 K. (b) In-situ DRIFTS spectra recorded for N2+H2O over AuRu0.31 nanostructures under the same irradiation condition. The background has been subtracted from the spectra
随后作者使用原位近常压 X 射线光电子能谱(in-situ NAP-XPS)对 N 1s 谱图在光照反应下的变化进行了检测。如图Figure 4a 所示,位于399.6 eV 的宽峰为样品表面 PVP 中吡咯型氮元素产生的信号,该信号在反应过程中保持稳定。在引入分压为 0.5 mbar 的高纯 N2 后,气态 N2 的 XPS 峰出现在了 405.1 eV 处(Figure 4b)。开始光照后,化学吸附态的氮原子信号(≡N)首先出现在 395.3 eV 处(Figure 4c)。这一信号的出现证明等离激元催化剂表面的 N2 分子在光照下直接发生了解离。
随着光照时间的增加,氮原子部分加氢产生的 =NH 和 -NH 的 XPS 信号相继在 397.2 eV 和 398.0 eV 处出现(Figure 4d-e)。并最终在 400.8 eV 处出现了吸附在催化剂表面的氨产物的 XPS 信号(Figure 4e-f)。尽管在 X 射线光电子能谱中,N2Hy 与 N-H 的信号不太容易进行区分,但在反应开始时 395.3 eV 处出现的吸附态氮原子(≡N)的信号为 N2 分子在等离激元驱动下的直接解离提供了直接有力的证据。
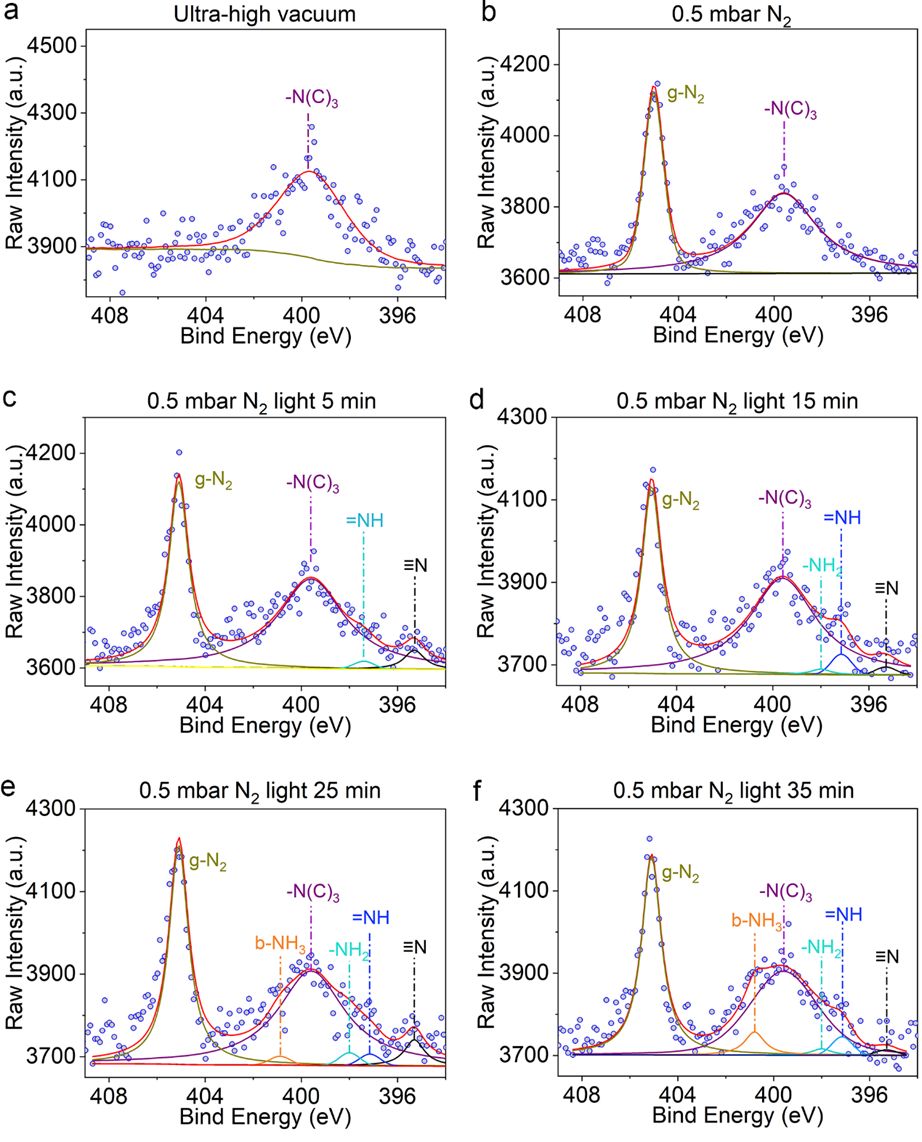
▲Figure 4 N 1s XPS spectra of AuRu0.31: (a) under ultra-high vacuum, (b) under 0.5 mbar N2 gas without light, (c-f) under 0.5 mbar N2 gas with incident light for different time.
为了进一步理解等离激元效应在 N2 分子解离过程中的作用,熊宇杰教授/龙冉副教授团队与宾夕法尼亚州立大学的陈星博士进行合作,对不同条件下的简化模型(Au22Ru6)进行了模拟计算。他们首先在不加入电荷和电场的情况下,对 N2 分子在 Au22Ru6 上的吸附情况进行了分析。计算发现,吸附的 N2 分子优先以竖立的方式吸附在金属 Ru 的表面,键长为 1.128 Å,这与之前 LT-FTIR 得到的实验结果一致。当 Au22Ru6 带上一个单位的负电荷后,Au22Ru6 上的 N2 分子的 N-N 键长仅小幅度地伸长到 1.130 Å。这表明单纯依靠热电子的转移很难实现 N2 分子的解离。
陈星博士向计算体系中引入一个 1.0×108 V·m-1 的电场,在该电场的作用下,N-N 的键长增加到了 1.165 Å,证明了局域电场增强在 N2 分子活化中的重要作用。如果同时考虑等离激元产生的热电子和局域电场增强,N2 分子的键长将进一步增加到 1.170 Å(Figure 5)。图中电荷密度的变化直观地展示了 N2 分子和 Au22Ru6 团簇电子结构之间的杂化情况。该计算结果表明 N2 分子在催化剂表面的解离,是光照下等离激元产生的热电子和电磁近场增强效应共同作用的结果。
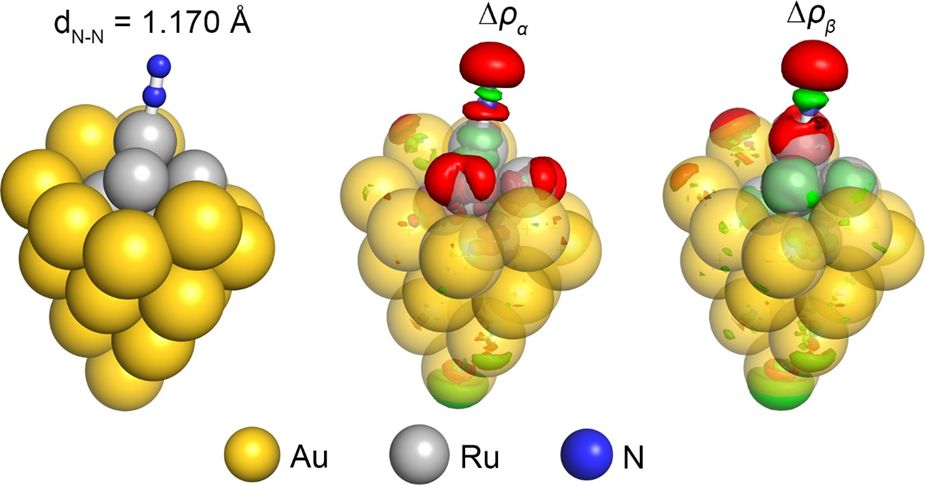
▲Figure 5 The optimized structures of N2 adsorbed on Au22Ru6 cluster, both charged by 1e and experienced with an electric field of 1.0x108 V·m-1.
总结与展望
熊宇杰教授/龙冉副教授团队通过构筑 AuRu 核-天线纳米结构催化剂将具有吸收可将光能力的等离激元金属 Au 和可以吸附 N2 分子的金属 Ru 结合起来,实现了温和条件下(常温、低压和光照)纯水中的固氮反应。在光照下,通过表面等离激元产生的热电子和电磁近场增强效应的共同作用,N2 分子可以直接在催化剂表面发生解离,这为传统催化剂的改进(例如减少在 Haber-Bosch 过程中的能量投入)提供了参考,也为用于光驱动化学转化的等离激元催化剂的设计提供了新的思路。
来源:rationalscience 研之成理
原文链接:http://mp.weixin.qq.com/s?__biz=MzIwMzE5MzQ1NQ==&mid=2649325745&idx=2&sn=3e00bc5f783892c7787cc4475345c0d7&chksm=8ece0db1b9b984a70d57a1179e9bb6009c510fe09267e9a068f405f4107471ecd199ab6436eb&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
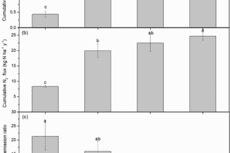
遗传发育所农业资源中心在土壤N2排放通量方面取得进展
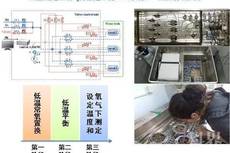
高频动态定量田间土壤N2排放的方法研究取得新进展
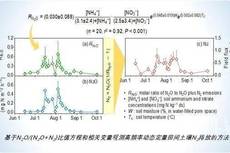
SBB: 高频动态定量田间土壤N2排放的方法研究取得新进展
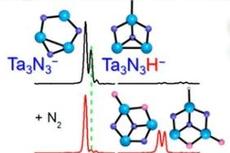
JACS:北京理工大学马嘉璧副教授团队及合作者在气相团簇化学领域取得重要进展
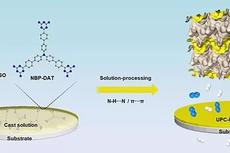
具有压力响应H2/N2分离性能和溶剂蒸汽修复能力的氢键有机框架膜

1天3篇Science,德国科研团队大爆发丨顶刊日报20190323
N2,N2-二甲基-2 ,4-嘧啶二胺
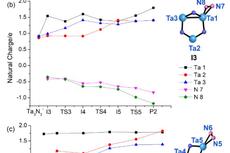
室温下Ta3N3H0,1-阴离子团簇固定、还原N2
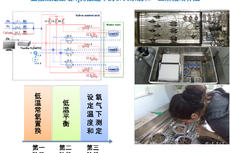
高频动态定量田间土壤N2排放的方法研究取得新进展
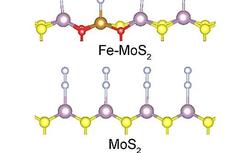
Fe单原子锚定MoS2纳米片增强N2电还原合成氨活性