科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-14
来源:BioArt
哈姆雷特说:“生存还是毁灭,这是一个问题”。而这也是我们体内每一个细胞所作出的最基本的决定。随着单细胞分析技术的发展,科学家们发现,不论是在正常生理状态下,还是在药物处理条件下,每一个细胞对于命运——是增殖还是静息抑或是死亡——都有自己的选择【1,2】。
化学药物治疗(简称化疗)是目前治疗癌症最有效的手段之一。在传统化疗过程中,化疗药物通常每几周以最高耐受剂量给癌症病人注射一次,尽管这种方式可以杀死大部分肿瘤细胞,但是经常也会导致一小部分肿瘤干细胞增殖形成新的肿瘤。同时,由于高剂量的化疗对肿瘤周围基质细胞(包括免疫细胞和血管内皮细胞)也造成了严重伤害,复发的肿瘤通常恶性程度更高,可以转移至全身各处。
近年来出现的新型化疗方式“非致死剂量化疗”也称“低剂量化疗,因其具有毒副反应小、患者耐受性明显提高、疗效更佳等优势,已逐渐成为临床中常用的治疗策略。越来越多的实验发现,经受“非致死剂量化疗”的细胞形态和代谢活动发生重要改变,更趋向于“选择”进入衰老的状态【3,4】,因此,诱导癌症细胞衰老成为新的治疗策略开始被探索,但是,随着研究的深入,人们发现这些策略在执行过程中也同时出现了一部分 “选择”增殖的细胞【5】,并且从长远来看,衰老的癌症细胞对健康也有一定的副作用【6】。
研究已经证实,对化疗诱导的衰老起重要调节作用的关键分子是周期依赖激酶抑制剂p21(CDKN1A),一方面,早期高表达的p21可以促进细胞最终的衰老,另一方面,又有一部分研究发现化疗中早期高表达的p21导致细胞最终进入增殖的命运。面对这样截然相反的结果,我们不禁想问,在化疗过程中,p21这个早期信号到底是如何影响细胞最终是增殖还是衰老的命运的呢?
2019年6月13日,来自美国加利福尼亚大学的Chien-Hsiang Hsu、Steven J. Altschuler和Lani F. Wu在Cell上发表题为Patterns of Early p21 Dynamics Determine Proliferation-Senescence Cell Fate after Chemotherapy的文章,在单细胞水平清晰阐明了 “非致死剂量化疗”早期p21的动力学状态在细胞最终增殖或衰老的命运抉择过程中的因果关系,为癌症化疗策略的优化提供了坚实有效的基础。

研究者们首先建立了一个实验体系,可以使得癌细胞进入增殖或者衰老两种状态,即在第一天给予癌细胞低剂量化疗药物,第2-5天去除药物,于第5天即可观察到存在衰老和增殖两种细胞亚群。那么是什么早期信号实践控制着细胞的这种命运决定呢?作者将关注点聚焦在衰老调节因子p21上,同时利用CRISPR介导的荧光标记技术(eFlut)在A549细胞系建立p21两条等位基因均标记mVenus的单克隆细胞(A549 p21V),以期在单细胞分辨率下监测p21的水平,从而将早期p21的表达与细胞最终的命运相关联。结合计算机算法分析,结果发现,不同命运的细胞,其p21动力学表现不同(图1),令人惊讶的是,在给药期间(1天),选择增殖的细胞很快就诱导并维持这高水平的p21表达,而衰老亚群细胞p21表达水平低,其诱导出现延迟。
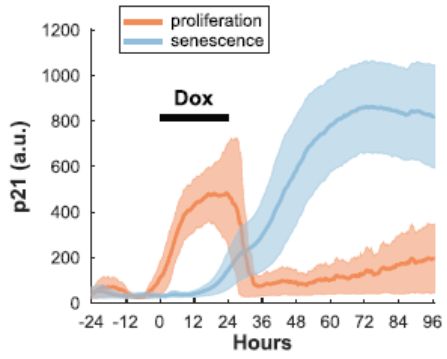
图1 不同命运细胞的p21动力学曲线
由于p21主要通过调节细胞周期而影响细胞的增殖,本文的研究者进一步探讨给药时间下p21动力学和细胞周期进程之间的关系以及它们和细胞命运的关系,结果显示,在给药时间下,p21的动力学存在3个不同的模式(图2左),其中G1期衰老细胞的p21表达显著高于G1期的增殖细胞,而两者均高于S/G2期衰老细胞的p21。进一步单细胞分析揭示了不同的细胞周期中p21和DNA损伤之间的关系,结果发现G1期细胞的损伤水平最低,但是p21的表达却最高(图2右)。
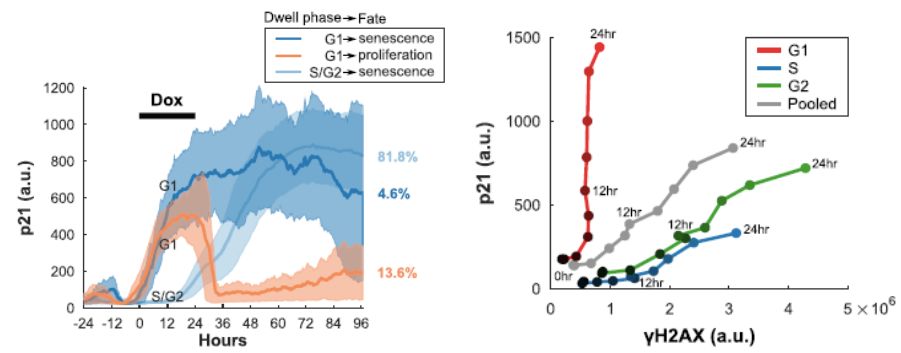
图2不同命运细胞的细胞周期与p21动力学曲线(左);不同细胞周期的细胞中p21与DNA损伤的关系(右)。
早期的研究表明,化疗药物阿霉素主要将细胞阻滞在S/G2期,在DNA损伤发生的同时p21转录激活,但是这显然与本研究的结果不同,通过深入的实验,本文作者揭示了其中的机制,即ATM信号通路的激活导致了G1期药物诱导的p21高表达,而S/G2期p21表达的降低则是由于Chk1信号的抑制以及蛋白酶体的降解,从而解释了在给药时间下,处于S/G2期的细胞(化疗药损伤最严重的时期并且大多是衰老细胞)p21表达最低的原因。
有意思的是,本文研究人员在治疗过程中抑制和增加p21的表达时均发现增殖的细胞减少,这就提示在细胞命运选择中,存在一个p21“黄金区域”,在这个区域内p21的增加会导致化疗后增殖细胞比例增加,这也提示我们,当药物浓度较低时,目前在化疗过程中选择增加p53以增强p21的治疗策略可能会产生癌细胞增殖的不良后果。
综上所述,本文首次揭示,在低剂量化疗过程中,细胞的增殖-衰老命运的抉择取决于p21动力学的三个不同模式,药物诱导的p21延迟或p21的急性表达将导致细胞衰老,而处于中间的p21应答则导致细胞增殖,继而找到了一个有利于细胞在药物治疗后继续增殖的p21“黄金区”,从而为临床上化疗策略的改进、联合用药等提出了新的指导方向。
原文链接:
https://doi.org/10.1016/j.cell.2019.05.041
参考文献
1. Barr, A.R., Cooper, S., Heldt, F.S., Butera, F., Stoy, H., Mansfeld, J., Nova´ k, B., and Bakal, C. (2017). DNA damage during S-phase mediates the proliferation-quiescence decision in the subsequent G1 via p21 expression. Nat. Commun.8, 14728.
2. Ryl, T., Kuchen, E.E., Bell, E., Shao, C., Florez, A.F., Monke, G., Gogolin, S., Friedrich, M., Lamprecht, F., Westermann, F., et al. (2017). Cell-Cycle Position of Single MYC-Driven Cancer Cells Dictates Their Susceptibility to a Chemotherapeutic Drug. Cell Syst. 5, 237–250.
3. Gewirtz DA, Holt SE, Elmore LW. Accelerated senescence: an emerging role in tumor cell response to chemotherapy and radiation. Biochem Pharmacol. 2008;76:947-57.
4. Litwiniec A, Gackowska L, Helmin-Basa A, Zuryn A, Grzanka A. Low-dose etoposide-treatment induces endoreplication and cell death accompanied by cytoskeletal alterations in A549 cells: Does the response involve senescence? The possible role of vimentin. Cancer Cell Int. 2013;13:9.
5. Reyes, J., Chen, J.Y., Stewart-Ornstein, J., Karhohs, K.W., Mock, C.S., and Lahav, G. (2018a). Fluctuations in p53 Signaling Allow Escape from Cell-Cycle Arrest. Mol. Cell 71, 581–591.
6. Demaria, M., O’Leary, M.N., Chang, J., Shao, L., Liu, S., Alimirah, F., Koenig, K., Le, C., Mitin, N., Deal, A.M., et al. (2017). Cellular Senescence Promotes Adverse Effects of Chemotherapy and Cancer Relapse. Cancer Discov. 7, 165–176.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652471271&idx=4&sn=3d4dcb07b49ea629fa706a8bc9029300&chksm=84e2ec53b3956545b85b1d407c25249945ce5656a73afe79ef776af299b701a707f4068da611&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

中心粒如何独立于细胞周期进行复制
细胞生物学: 模型原始细胞也许可预测原始细胞周期
【大师讲堂】细胞周期与癌症发生有着怎样的联系?
哈佛大学医学院Kucherlapati教授访问中国抗癌协会


澳大利亚icon医疗集团访问中国抗癌协会秘书处



Cell Meta:单细胞代谢差异的潜在推手:氧化磷酸化、糖酵解、细胞周期

华中农大揭示植物细胞周期如何“刹车”?
中国抗癌协会王瑛秘书长出席河北省肿瘤防治宣传周启动仪式



Cell Stem Cell | 辛利组揭示微环境调控前列腺干细胞增殖的机制

Yuu Kimata教授对细胞周期蛋白在多细胞生物中的更多潜在功能进行展望