科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-06-22
来源:X一MOL资讯
羧酸化合物在自然界中广泛存在,而利用这种含有特定官能团的化合物作为底物在合成化学和生物过程中扮演着重要的作用。脱羧官能团化是可见光诱导的有机合成方法学中研究最多的反应(没有之一!!!),但是目前关于可见光诱导的脱羧反应基本上都是脂肪羧酸及其衍生物的脱羧官能团化,而涉及到芳基羧酸或其衍生物的脱羧官能团化的反应少之又少,目前有两篇文献报道,羧酸的脱羧芳基化(Chem. Sci., 2017, 8, 3618-3622)和芳基羧酸衍生物的脱羧硼基化(J. Am. Chem. Soc., 2017, 139, 7440-7443),这两篇文章均是德国明斯特大学的Frank Glorius课题组所报道。
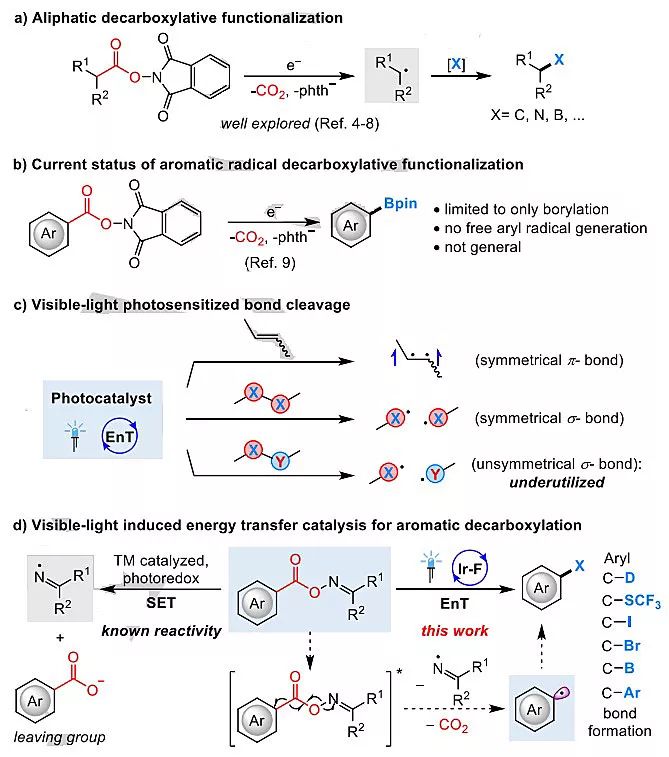
图1. 脱羧官能团化。图片来源:Angew. Chem. Int. Ed.
芳基羧基脱羧难以进行主要原因是其动力学稳定性,脱羧反应的速率常数(芳羧基vs烷羧基:~105 s-1 vs ~109 s-1),因此,与烷羧基相比芳羧基的脱羧反应仍然是一个巨大的挑战。最近,Frank Glorius课题组在可见光的条件下,通过能量转移(Energy Transfer, EnT)的方式实现了芳基/烷基羧酸衍生物的脱羧官能团化(图1d),该文章发表于Angew. Chem. Int. Ed.。
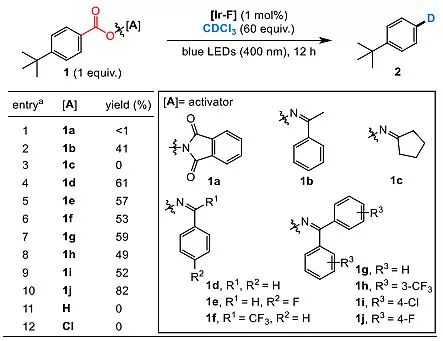
图2. 条件的筛选。图片来源:Angew. Chem. Int. Ed.
文献中报道的可见光促进的脱羧反应一般都是通过单电子转移(SET)过程来实现的,关于EnT对化学键的敏化通常是键能弱的π-键(如环加成反应、E/Z异构化、去消旋化等),对称的σ-键及过渡金属络合物,而通过可见光诱导的EnT实现非对称的σ-键的敏化和切断还未见报道。这主要是由于在光催化剂下非对称σ-键的固有电负性倾向于SET过程而不是EnT过程。确实,如羟胺衍生的活性酯通过可见光诱导的 SET对N-O键的还原,在含氮中心产生自由基,同时生成一个稳定的苯甲酸根负离子。而相反,EnT过程可以产生协同碎片化/脱羧过程而产生芳基自由基。更重要的是该过程在不需要还原剂的情况下,脱羧过程能够自发产生,并使催化剂实现循环。
在这里,Ir(dF(CF3)ppy)2(dtbbpy)]PF6由于其长的激发态寿命(τ = 2.3 μs)和高的三线态能量(60.8 kcal mol-1)被作为光敏剂(催化剂),而N-O键解离能只有~45 kcal mol-1。作者选取了12种芳基羧酸衍生物(其中图2中entry 11为羧酸),选取脱羧氘代作为模板反应,因为氘代标记的产物在新药研发中的疾病诊断和药物工业化中占据重要地位。为了选出更高活性的芳基自由基,氘原子就选用了最常用和便宜的氘代试剂如氘代氯仿,通过这些羧酸衍生物的脱羧实现其氘代的反应。根据结果的对比,最后发现取代基为1j时候,收率最高。
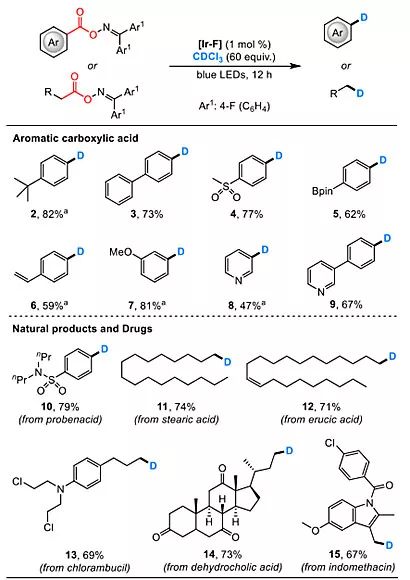
图3. 脱羧氘代反应。图片来源:Angew. Chem. Int. Ed.
在确定了最优的取代基后,作者对羧酸底物进行了拓展。一系列带有推电子和吸电子的羧酸底物在优化的条件下均能给出相应的脱羧氘代产物,并且该方法还具有较优的官能团兼容性,比如磺酰基、硼酯、烯烃、烷氧基以及磺酰胺均能兼容;作者也对一些含有羧基的天然产物和药物分子进行了考察,值得注意的是这些复杂分子除了10外都是脂肪羧酸,因此,也说明该策略对脂肪链的羧酸也同样适用。
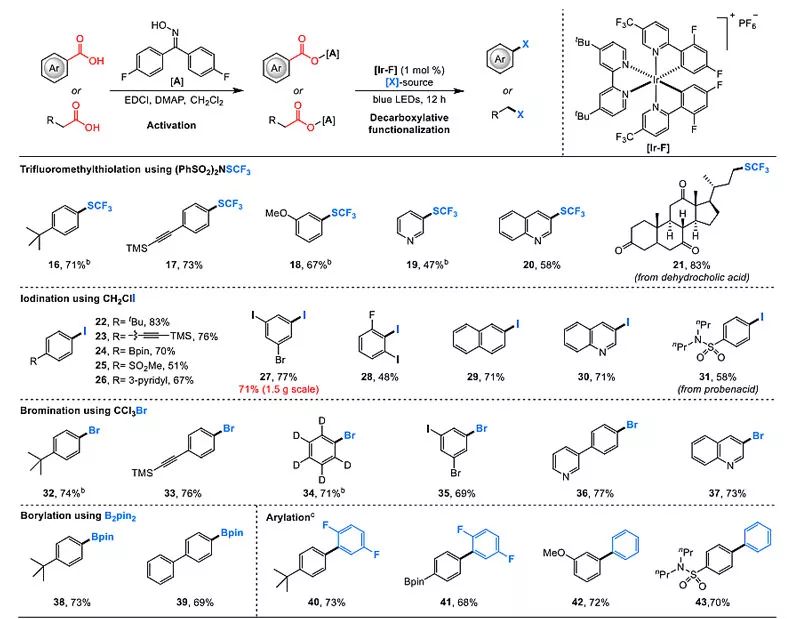
图4. 底物的范围。图片来源:Angew. Chem. Int. Ed.
除了脱羧氘代,作者也对底物进行了脱羧之后的其它取代反应。比如利用(PhSO2)2NSCF3作为弱亲核性芳基自由基的捕获剂,实现了脱羧硫三氟甲基化,在这里作者选取了五个芳基羧酸和一个复杂的烷基羧酸作为代表性的例子;此外,作者分别利用氯碘甲烷和溴仿作为碘和溴源,通过脱羧得到碘代和溴代的产物;最后通过该方法得到的芳基自由基也能被硼酯和芳烃所捕获,可得到相应的硼烷和芳基化产物。
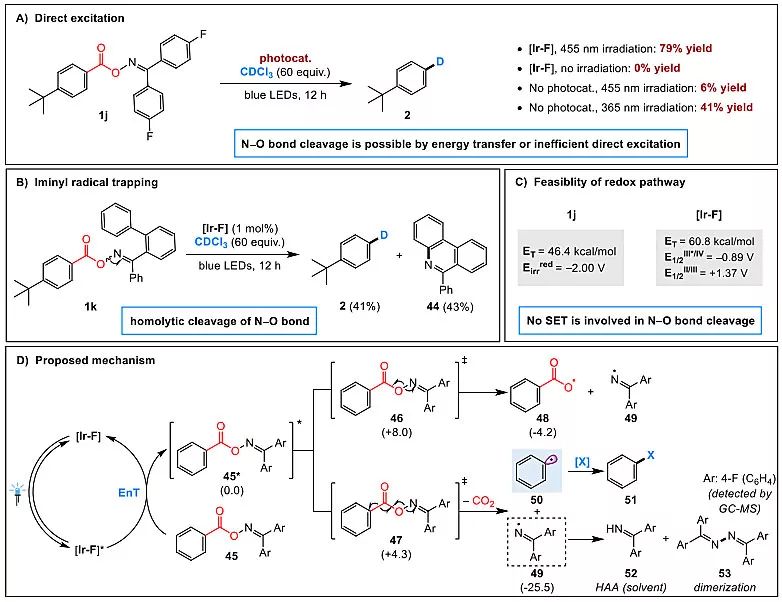
图5. 反应的机理。图片来源:Angew. Chem. Int. Ed.
最后,作者探讨了反应的机理。首先,作者通过Stern-Volmer磷光淬灭实验即1j对光催化剂激发态[Ir-F]*的磷光淬灭,证实发生了激发三线态的振动跃迁。其次,作者探讨了该反应进行EnT机理的可行性。一方面,三线态过程的反应可以直接被光激发,这区别于单线态机理。作者确实观测到,使用365 nm的LED灯照射,可以产生同样的产物2,只不过产率稍低。另一方面,EnT实验过程应该同时产生N-中心亚胺自由基50和芳基自由基。作者通过分子内捕捉得到产物45,证实形成了亚胺自由基,且产率和脱羧产物2相当。再次,作者探讨了该反应进行SET机理的可行性。作者考察了1j的电化学参数,1j的不可逆还原电势为-2.0 V(vs SCE in DMF),这排除了通过IrIII*或IrII的SET还原过程。而与此相反的是,比较1j的计算三线态能量数据与[Ir-F]*的三线态能量,进一步证实了[Ir-F]*到1j的三线态能量转移的热力学可行性。
由此作者提出了该反应的机理如图5D。假如,46*只能发生N-O键均裂产生自由基49,然而49的直接脱羧难以发生(因为羧基自由基与芳香-π-体系的共轭稳定性),49会参与快速的氢原子攫取(HAA)过程,且快于脱羧过程。进一步可通过DFT计算排除这一路径。两个路径的能量计算表明,通过48的协同碎片化/脱羧过渡态能垒相比于47的碎片化过渡态能垒有3.7 kcal mol-1的能垒优势,这也与实验中观测到的现象,脱酸过程优于羧酸形成相一致。
总结
Frank Glorius课题组在可见光的条件下,选取Ir(dF(CF3)ppy)2(dtbbpy)]PF6作为光敏化试剂,通过能量转移的方式,实现了非对称的σ-键的切断,成功的得到了一个通用的脱羧反应策略。该方法可以从相应羧酸衍生物得到芳基和烷基自由基,然后它们能分别被用于不同的碳杂原子和碳碳键形成反应。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657614096&idx=3&sn=ebad25f20e7415ba21c31a584c4b6333&chksm=80f7d0c0b78059d62ffa9b3ce7ef95a0e546603fd5de0f9427a3cf73a4ed39df253c8b3b4442&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Angew:可见光一照,MOF吞云吐雾
可见光可引发氧化吲哚芳基化反应

可见光介导的β-氯代酮的合成
聚合反应方法新突破:用细菌实现可控自由基聚合
Armido Studer课题组报道苯炔作为自由基受体实现自由基的串联反应
“声东击西”!基于自由基Smiles重排的迁移还原交叉偶联反应
可见光探测器
JACS:首例自由基关环/开环串联聚合反应
“新玩法”实现双光子量子纠缠
从健康的角度看不可见光