科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-10-14
来源:BioArt
细胞是生命的基本组成单元,其概念提出,最初是基于列文虎克在显微镜下观测到的“小室”形状的物理结构。数十微米直径、皮升级容积的细胞内包含着数以千万记的生物大分子。细胞的物理性质(包括硬度,体积,分子拥挤)随着细胞种类的改变,细胞外微环境的改变而改变。时至今日,生物学的发展已经在分子生物学和遗传学上取得了巨大成就,然而,细胞物理性质在生物功能上的作用依然不清晰。近年的研究发现,细胞内的物理微环境显著着调控着细胞内的分子过程。事实上,所有的分子生物过程都发生在拥挤的生物大分子微环境中。尽管分子拥挤对分子生物过程的影响已经在体外体统和合成生物学系统中得到了广泛的验证。但是分子拥挤在细胞内,特别是组织器官水平上的功能并没有得到理解和验证。
组织和器官是由拥有不同物理性质的细胞有序地搭建而成。举例来说,自我更新的小肠表皮,有序的折叠成隐窝和绒毛结构。小肠干细胞(Lgr5+)在小肠隐窝底部自我更新。快速自我跟新的小肠干细胞(Lgr5+)在隐窝底部产生压力,并将分化后的小肠上皮细胞推向绒毛顶端。与此同时,小肠内的渗透压往往随着饮食和消化而改变。复杂的物理微环境导致小肠内的细胞存在极大的异质性和稳定性。然而细胞的物理性质和力学微环境如何调控小肠隐窝的功能仍未知。
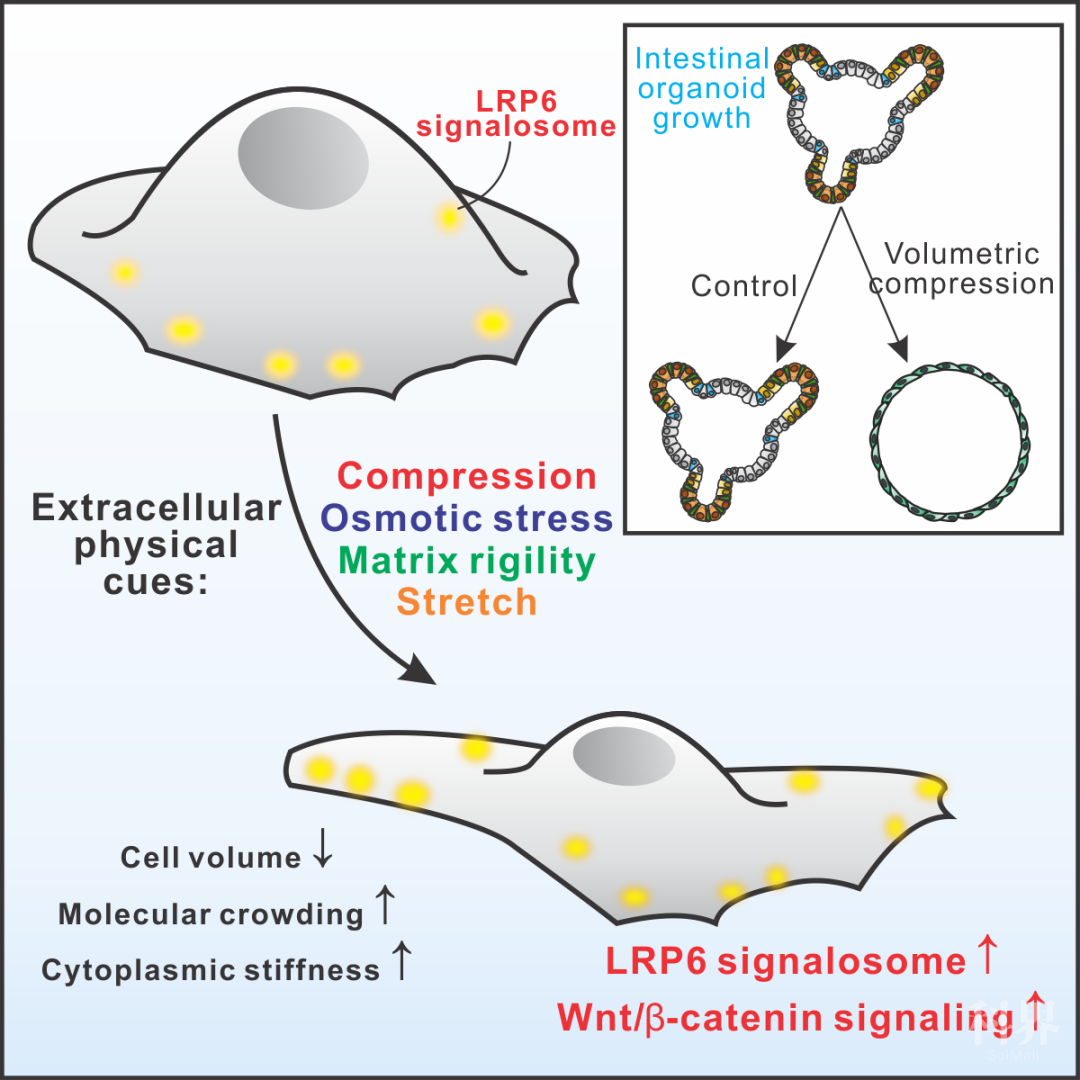
2020年10月13日,麻省理工学院郭明(Guo, Ming)课题组在Cell Stem Cell 上发表了题为“Volumetric Compression Induces Intracellular Crowding to Control Intestinal Organoid Growth via Wnt/beta-Catenin Signaling” 的研究论文, 该论文报道了细胞内分子拥挤在小肠类器官力学传导和干细胞命运调控中的作用。该文章发现,细胞的物理性质(体积、软硬、分子拥挤)会遵循普遍的软物质物理规律、响应细胞外多种物理力学刺激(包括渗透压、基质软硬、力学拉伸和挤压)。改变后的细胞质物理微环境影响着细胞内生物大分子相互作用的平衡和速率,从而调控细胞内的信号转导。在类器官水平,类器官在物理挤压的作用下增强了Wnt信号通路的激活,从而使得小肠干细胞在自我更新和分化中选择自我更新,促进了类器官的生长。作者发现,在高渗培养液挤压的条件长时培养(~1个月),可以有效的诱导成熟分化的小肠类器官(crypt organoid)转化成为以干细胞为主的干细胞团类器官(ISCs sphere)。

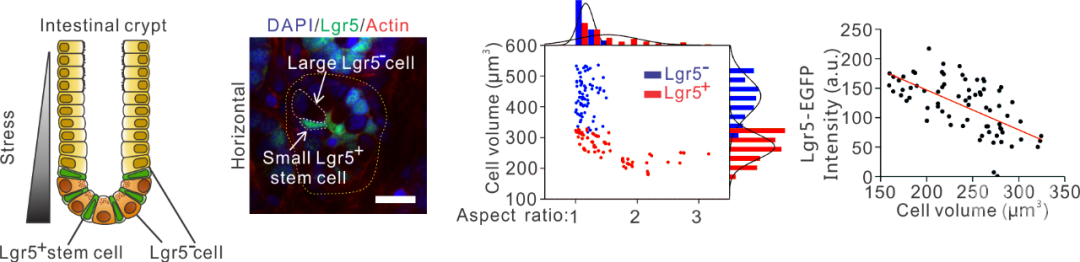
本文的研究人员首先从真实的小肠组织出发,寻找细胞物理性质和小肠细胞干性的相关性。通过共聚焦成像荧光标记小肠干细胞(Lgr5-EGFP)的老鼠小肠组织,并结合细胞力学、生物物理实验手段,发现小肠干细胞特有的物理性质,相较于其他分化后的Lgr5-细胞(如Paneth cells)相对比较小,且细长,细胞内分子拥挤程度更高。更重要的是,在小肠隐窝之中,小肠干细胞干性标记物的表达量和细胞的体积呈明显的负相关性。小肠干细胞标记物Lgr5是Wnt/beta-catenin信号通路的靶基因,通过荧光成像转导因子beta-catenin,研究人员确认了细胞体积和Wnt/beta-catenin信号强度的负相关性。
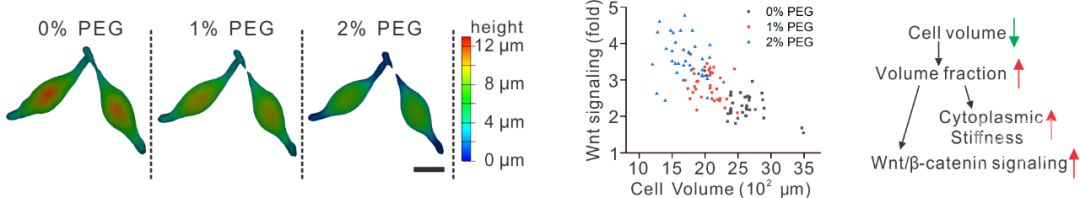
既然Wnt/β-catenin信号通路强度和细胞体积之间存在着负相关性,那是否可以通过调节细胞体积,反向调控Wnt/β-catenin信号通路么?答案是肯定的。作者通过不同力学刺激(高渗透压、基质软硬、力学拉伸和力学挤压)调控肠道细胞体积,发现细胞体积的变化总是伴随着Wnt/β-catenin 信号强度的相反变化。其原因是:细胞的体积变小会造成细胞内生物大分子的浓缩,细胞内的分子拥挤促进了LRP6-Axin信号体(LRP6-Axin signalosome: Wnt信号通路的受体复合物)的形成,使得LRP6和Axin等信号体蛋白倾向于发生多聚,最终放大原本由Wnt配体激活的Wnt/β-catenin信号通路。
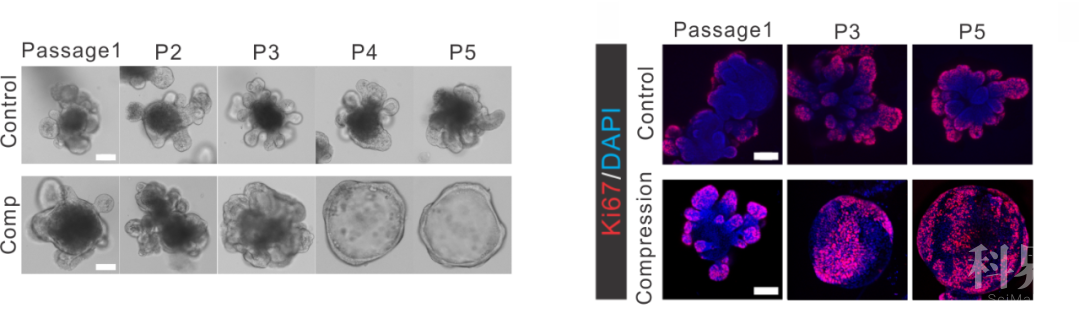
Wnt/β-catenin信号通路是小肠类器官发育的主要调控通路。小肠干细胞在Wnt/β-catenin靶基因高表达时,进行自我更新;Wnt/β-catenin信号下降时,小肠干细胞开始分化成成熟小肠内皮细胞。研究人员进一步探索物理力学刺激是否在组织器官水平同样调控类器官中细胞的物理性质和生长。作者发现,渗透压挤压,和力学挤压均可调控类器官中的细胞体积和细胞内分子拥挤。在挤压条件下,作者观测到小肠类器官内分裂的细胞数目明显增加,并且小肠干细胞在类器官中的比例明显增加。更显著的,类器官在挤压的条件下长时间培养,可以诱导成熟分化的小肠隐窝类器官,转化成为干细胞纯度更高的干细胞团类器官。更进一步的,作者通过短发卡RNAs(short hairpin RNA)扰动Wnt/β-catenin信号通路,确定力学挤压是通过调控Wnt/β-catenin信号通路调控干细胞的生长;作者通过二维器官培养技术(2D enteroid culturing),结合分子成像,确认了在小肠类器官中,分子拥挤是通过稳定LRP6-Axin信号体的形成,调控了Wnt/β-catenin信号的增强。
本文第一作者李一伟博士介绍:“本研究在类器官生长的模型中探索了细胞物理性质和生化信号转导的相互作用。细胞作为一种软材料,响应微环境中的力学刺激是符合普遍的力学规律的。细胞质作为细胞内生化活动的载体,其物理环境的改变势必改变生化反应的平衡和速率。基于此,我们提出,细胞的物理性质,不同于传统的力学感受器分子(mechanosensor),同样可以起到传导细胞外物理力学信号的作用,是对细胞力学传导机制的补充和完善。基于此理解,研究者们可以设计工程学方法,用于类器官的培养和大规模生产,最终用于再生医学、药物筛选等领域。”
本文的通讯作者郭明(Guo,Ming)教授介绍:“我们课题组致力于细胞生物物理和生物力学研究,这篇工作和近年发表的工作(Nature Physics 2020; Science Advances 2020; Annual Review of Fluid Mechanics 2020; PNAS 2019.116.17175; PNAS 2019. 116. 9245; Soft Matter 2019; PNAS 2018; PNAS 2017,114, E8618; PNAS 2017, 114, 9529; JMPS 2017)一起,揭示了细胞力学、分子拥挤等物理现象在类器官、肿瘤等多细胞活体系统中的重要作用。”
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652503306&idx=4&sn=ab72d33777016945fd027f0e55c6e1d4&chksm=84e26ebeb395e7a8ecc4a0f618c089045c86e1540a7a6510efa05ffc01b771cec2a5dcbffc69&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
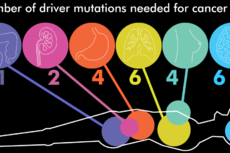
从健康细胞到癌细胞,或许只需要几个突变
口服法小肠造影
双气囊小肠镜
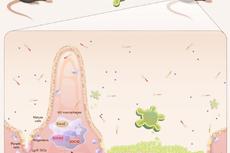
小肠类器官治疗缺血性肠损伤的作用及机制获揭示

学术造假必遭严惩,为何仍不断有人冒险

人体细胞内存在“铁路”系统,能自动优化结构
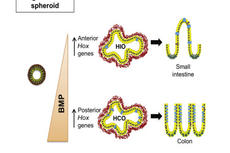
研究利用干细胞培育出结肠“类器官”
小肠造影
双气囊小肠镜

Science: SARS-CoV-2有效感染人小肠上皮细胞