科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-10-15
来源:X一MOL资讯
三磷酸腺苷(ATP)是自然界广泛存在的能量分子,为多种生命活动提供能量供给。并且,ATP是合成核酸的一种重要原料。在自然界中,ATP已经被证实可以和多种金属离子相互作用,其所形成的ATP-金属复合物被认为主要以辅助底物(co-substrate)的形式参与酶催化过程,其本身尚未被证实具有催化活性。最近,陕西师范大学王长号副教授等发现ATP和Cu(II)离子组装成Cu(II)-ATP复合物对Diels-Alder反应表现出优异的手性催化性能(Fig. 1),其中Cu(II)离子和ATP分子中腺嘌呤上N-7原子、β-位和γ-位的磷酸基相互作用之后表现出催化活性和立体选择性。
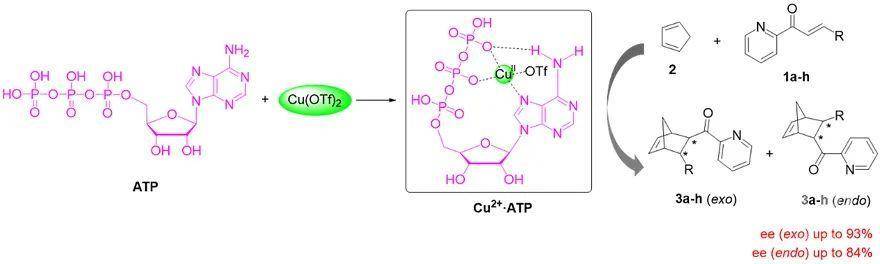
Fig. 1 The assembly of a Cu(II)-ATP complex (Cu2+•ATP) and the Cu2+•ATP catalyzed enantioselective Diels-Alder reaction
自上世纪80年代Cech和Altman发现具有催化活性的RNA(ribozyme)以来,关于核酸的催化功能一直是核酸化学的研究热点。基于核酸具有丰富空间构型的特点,近年来国内外学者利用核酸作为生物骨架与金属物种组装成核酸杂化催化剂研究其手性催化功能。2005年,Roelfes等利用双螺旋DNA为生物骨架和非手性Cu(II)配合物组装成DNA杂化催化剂,成功实现了将DNA的手性转移到目标产物中(G. Roelfes, B. L. Feringa, Angew. Chem. Int. Ed., 2005, 44, 3230)。2012年,李灿等利用G-四链体DNA(G4DNA)为生物骨架和Cu(II)离子相互作用组装成人工G4DNA金属酶,通过调变G-四链体的构型,实现了人工G4DNA金属酶催化不对称反应的产物绝对构型发生反转(C. Li et al., Angew. Chem. Int. Ed., 2012, 51, 9352)。除此之外,人工双螺旋DNA/RNA、发卡型DNA、G-三链体DNA、肽核酸等也被作为生物骨架组装成核酸杂化催化剂用于手性催化研究。但是,在已报道的核酸-金属杂化催化剂中,核酸骨架一般含有几十到几百个核苷酸单元,这不利于获得核酸杂化催化剂的精细结构和研究其手性催化机理。最近,该课题组发现含有两个腺苷酸的天然环状RNA分子(c-di-AMP)和Cu(II)离子能够特异性结合组装成人工金属核酸酶,它对Friedel-Crafts反应和Diels-Alder反应均表现出优异的手性催化活性(C. Wang et al., Angew. Chem. Int. Ed., 2020, 59, 3444; Eur. J. Org. Chem., 2020, 2020, 4417)。研究表明,c-di-AMP和Cu(II)离子形成二聚体结构参与到手性催化反应中。因此,发展结构稳定、组成简单的核酸杂化催化剂有助于研究核酸催化剂的活性中心以及核酸手性催化的构效关系,并且对于揭示自然界中核酸物种的潜在催化活性具有重要意义。
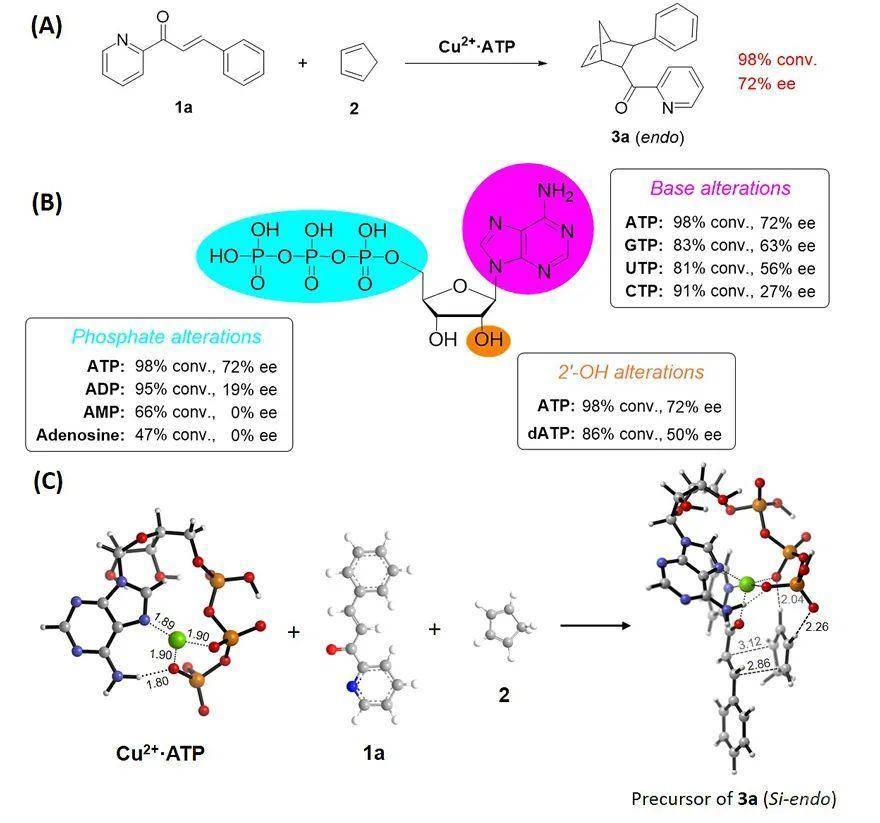
Fig.2 (A) A benchmark enantioselective Diels-Alder reaction of azachalcone 1a and cyclopentadiene 2 catalyzed by a Cu2+•ATP complex. (B) The effect of ATP analogues for the benchmark Diels-Alder reaction. (C) DFT calculation of the precursor formation of 3a (endo) with the favorable Si face attack.
本研究中发现Cu(II)离子和ATP特异性结合组装成Cu(II)-ATP配合物(Cu2+•ATP),它对氮杂查尔酮类底物和环戊二烯的Diels-Alder反应表现出优异的催化活性和立体选择性,底物转化率大于80%,产物的endo/exo比例可达96:4,其中exo产物的ee最高达到93%,endo产物的ee最高达到84%(Fig. 1)。以Cu2+•ATP催化氮杂查尔酮1a和环戊二烯2的Diels-Alder反应为模型,底物转化率为98%、endo产物的ee为72%(Fig. 2A)。反应动力学结果表明单独ATP对反应速率几乎无影响,而加入Cu(II)离子形成Cu2+•ATP后反应速率提高近13倍,这说明在Cu2+•ATP中Cu(II)离子是催化活性中心,ATP提供了空间手性骨架。一系列ATP类似物的控制实验表明,ATP分子中β-位、γ-位的磷酸基以及腺嘌呤上N-7原子对于Cu2+•ATP的手性催化活性至关重要(Fig. 2B)。随着ATP分子中磷酸基数目的减少,相应Diels-Alder反应的活性和手性选择性大幅下降。另外,含嘌呤类碱基的核苷三磷酸(ATP和GTP)在相应反应中表现出相当的手性催化结果,但是含嘧啶类的核苷三磷酸(CTP和UTP)则表现出较低的手性催化活性。核磁滴定实验也证实了上述结论,当ATP溶液中加入微量Cu(II)离子(Cu2+/ATP=1:500)后,N-7原子邻位的H-8原子的氢谱和β-磷酸基、γ-磷酸基的磷谱发生明显位移、强度降低且逐步宽化,说明Cu(II)离子很可能与β-位、γ-位的磷酸基以及腺嘌呤上N-7原子相互配位形成配合物。进一步结合DFT理论计算解析Cu2+•ATP的精细结构和催化机理。DFT计算结果表明,Cu(II)离子和ATP的N-7原子、β-磷酸基的氧原子、γ-磷酸基的氧原子发生配位作用,同时6-位氨基和γ-磷酸基的氧原子之间形成氢键,此时Cu2+•ATP的结构最稳定(Fig. 2C)。此优化的Cu2+•ATP模型中的Cu(II)离子和氮杂查尔酮1a相互作用形成中间体(Cu2+•ATP-1a),环戊二烯2和β-位、γ-位的磷酸基产生氢键作用,优先进攻Cu2+•ATP-1a中间体的Si面,这导致生成3a的endo型产物,并且其绝对构型为Si-endo,这与实验中获得的结果相吻合(Fig. 2C)。本研究表明ATP和金属离子相互作用能够形成手性催化物种,这为发展基于单个核苷酸的杂化催化剂和理性设计高效人工金属核酸酶提供研究基础。特别是,ATP和天然金属离子结合所表现出的催化活性可能会参与原始化学环境中手性的起源以及基于ATP的前生物合成。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657663871&idx=5&sn=f9861d4b908fa971481b1c695f601c7e&chksm=80f892afb78f1bb98fbfb8c469ea2c2b9832e5e7aa3d52c860b45131a696712b192975bcc29b&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

【有机】铁金属中心手性八面体配合物:拓展廉价金属不对称催化

结合手性磷酸催化和中心到轴手性转变策略构筑轴手性芳基-苯并吲哚
电荷转移配合物
兰州化物所钯催化不对称碳-氢羰基化反应研究取得进展

铜-胍配合物催化手性汇聚烯丙基的硼化反应
合肥研究院在狄拉克半金属Cd3As2纳米片中观测到平面霍尔效应----中国科学院

2018未来科学大奖揭晓,袁隆平等7位科学家获奖

【每日科技速递】北京科技奖拟增“中关村奖”
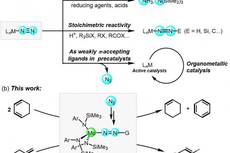
异双核钼氮镁配合物催化化学
兰州化物所在不对称碳氢键硼化研究方面取得进展

