科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-11-12
来源:生物通
“使用这种独特的模型,我们发现了自噬的基本功能,即可以使mTORC1的活性保持高水平,并显示缺失Tsc1的神经干细胞的异常发育。”

辛辛那提大学的一组研究人员发现了一种新的靶向激活某种蛋白质复合物的分子过程,从而提出了针对引发肿瘤相关疾病的新潜在疗法。
这一研究发现公布在11月11日的Nature Metabolism杂志上,由癌症生物学家管俊林教授(Jun-Lin Guan),王诚然(Chengran Wang,音译)等人完成。
王博士说:“结节性硬化症复合物(TSC)是一种遗传性疾病,会引发肿瘤在包括大脑在内的许多不同器官中形成,每年影响多达50,000人。TSC还可以通过引起新生儿和成年人的癫痫发作和自闭症等方式影响大脑。对于这种疾病,如果发生称为Tsc1或Tsc2的基因突变,就能令其抑癌功能丧失,进而导致mTORC1的过度激活和异常功能,导致了TSC的多种症状。”
mTORC1被称为细胞的“主调节剂”,可促进大多数细胞生长。然而,它并不能促进自噬,这是一种细胞处于自食状态的调节方法,是细胞内产生燃料的有效途径。
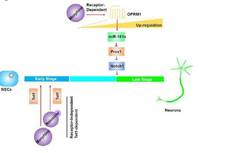
在这项研究中,科学家发现没有Tsc1的细胞具有更高的自噬活性。因此他们创建了一个“双基因敲除”动物模型——一种既不存在Tsc1,也不存在必需的自噬蛋白FIP200的模型,其中FIP200存在于发育中的神经系统和成年神经干细胞中。
作者表示:“使用这种独特的模型,我们发现了自噬的基本功能,即可以使mTORC1的活性保持高水平,并显示缺失Tsc1的神经干细胞的异常发育。”
研究人员分析了维持高mTORC1活性所涉及的自噬的分子和代谢机制,并发现mTORC1需要别用来激活能量存储,也就是缺失Tsc的细胞中的脂质滴。
“通过自噬分解脂滴,可以提供脂肪酸作为能量来源,维持缺乏Tsc1的神经干细胞的能量产生。我们还使用药理学方法靶向自噬,阻断了用于治疗缺陷的脂肪酸,从而在这些模型中模仿人的TSC症状。”
管教授认为,这些结果对于增加对这种疾病的形成,以及如何将其靶向分子水平的认识至关重要。
加州大学癌症生物学教授Francis Brunning Endowed表示:“现在我们更加了解由Tsc基因突变和mTORC1过度活跃引起的TSC涉及的信号传导途径和代谢改变。这将有助于开发新的治疗概念,治疗这种破坏性疾病。”
来源:gh_c1fce5726992 生物通
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5NzMwNjYyMg==&mid=2675531271&idx=2&sn=165d2e38379a3642b52b5e3ca9564cbd&chksm=bc51f7968b267e80acdbe57f76d20c531e89c8d31ca1660e2c40e88bfd3bd746fbae0cf4456a&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

新突破! 二维实验系统成功应用于四维材料研究
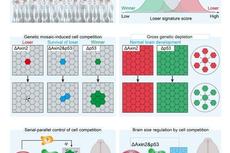
遗传发育所揭秘神经干细胞的内卷式竞争
新研究:自闭症与神经干细胞功能障碍

大型恒星比想象的更多
神经干细胞移植走向临床:回顾与展望
长期追踪活体小鼠大脑中特定神经干细胞活动的新方法:鉴别一种新的长寿神经干细胞
更好的期刊,更好的科学——中国科技峰会·世界科技期刊论坛专家观点荟萃



研究人员揭示神经干细胞分化新机制
神经干细胞
广州生物院揭示神经干细胞分化新机制