科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-11-23
来源:新叶社
我国科学家全球首创脊柱侧弯大规模人工智能筛查系统
来自上海交通大学附属新华医院、中山大学中山眼科中心和西安电子科技大学的研究团队近日在Communications Biology杂志上联合发表长文“Development and validation of deep learning algorithms for scoliosis screening using backimages”,报道了该团队开发的全球首创脊柱侧弯大规模人工智能筛查技术。
该研究团队采用患者的x光射线和超声影像作为患者脊柱侧弯的金标准标签,通过对带标签的外观图像进行模型训练,首次明确背部外观特征与脊柱侧弯严重程度的关系,建立了基于背部裸露外观照的脊柱侧弯人工智能筛查系统;同时创新性的采用目标检测网络定位患者的裸露背部,并利用多个卷积神经网络满足不同筛查任务的需求。该模型在筛查青少年是否患有脊柱侧弯,确定患者是否需要治疗,明确青少年脊柱弯曲程度,这三大方面都具有出色的表现。
该智能系统的筛查准确率已经达到了人类专家平均水平,且速度要明显优于人工,有望在大规模脊柱侧弯筛查中应用,具有重要的医学、经济和社会价值。
我国科学家成功研发上消化癌内镜人工智能辅助诊断系统
全球约50%的上消化道癌发生在中国,其中超过85%的患者在初次诊断时已为中晚期。上消化道早期癌患者五年生存率超过90%,而晚期患者的五年生存率不足10%。因此,上消化道癌的早期诊断早期治疗是提高疗效的关键。目前,内镜检查及活检仍是上消化道癌早期诊断的金标准。上消化道早期癌在内镜下没有明显的表征,而我国的内镜医生水平差异较大,导致内镜早期癌检出率低(不足10%)。因此,寻找准确有效的早诊方案,并行之有效地推广至基层,能够促进各级医院上消化道内镜诊断水平逐步同质化,提高整体医疗服务质量。
近期,中山大学附属肿瘤医院研究团队在国际学术期刊Lancet Oncology杂志上在线发表了题为“Real-time Artificial Intelligence for Detection of Upper Gastrointestinal Cancer by Endoscopy: a Multicentre, Case-control, Diagnostic Study”的研究工作。该研究联合了多学科专家攻关,成功研发出具有完全自主知识产权的上消化道癌内镜人工智能辅助诊断系统(Gastrointestinal Cancer Endoscopy Real-time Artificial Intelligence Diagnostic System, GRAIDS)。研究前期完成了上消化道癌患者内镜图像5万余张和正常人内镜图像12万余张的标识以及机器学习。在内镜图像识别困难、疾病种类多、癌变表现复杂的情况下,通过深度卷积神经网络的技术基础,研究实现准确性高、稳定性强、人机结合度高的实时人工智能辅助检测系统。同时,构建了基于云技术的多中心GRAIDS平台,可以自动捕获内镜检查图像上传至云端进行人工智能分析,实时向操作者反馈提示可疑病灶区域,指导操作者更有针对性的选择活检部位,从而提高活检阳性率。GRAIDS系统在全国5家不同地区、不同级别的医院进行多中心研究验证,在来自84424例患者共1036496张内镜图像进行识别和分析。结果显示,该系统对上消化道癌的诊断准确率达90%以上,其诊断灵敏度(94.2%)与专家级的内镜医师(94.5%)相当。随着GRAIDS系统的进一步研究推广,有望提高我国上消化道肿瘤的早诊早治水平,促进肿瘤规范化治疗,推动分级诊疗的实现。
研究人员通过单细胞测序绘制首个人胚胎造血和免疫系统发育图谱
近期,来自英国Newcastle University和Wellcome Sanger Institute等机构的科学家在Nature上以长文形式发表了题为“Decoding human fetal liver haematopoiesis”的研究,首次报道了由胎肝驱动的人胚胎造血和免疫系统发育过程的单细胞图谱。
在该项研究中,作者首先制备了受孕后4周至17周的人胚胎肝脏、卵黄囊、肾脏和皮肤组织单细胞悬液,随后利用流式细胞术和单细胞测序技术对其进行了转录组基因表达定量分析,从而构建了完整的人胚胎造血和免疫系统发育图谱。
基于这一单细胞图谱数据集,作者主要利用了基于力导向图算法的数据降维方法,以高维度基因表达谱为依据,推测了造血和免疫细胞的发育路径。这一路径推测分析给出了三个符合已知研究结果的由造血干细胞生发的血液系统细胞主要发育过程,包括红系细胞—巨核细胞—肥大细胞系、B/T淋巴细胞系及髓系细胞系。上述分析以极高的时空分辨率揭示了人胚胎发育过程中完整的血液、免疫系统动态变化过程,在契合现存大体知识框架的前提下为这一复杂生物学现象补充了丰富的细节。
利用上述的发育路径推测分析及对特定细胞群基因表达时间序列的动态分析,作者还揭示了多项关于胚胎造血及免疫系统发育的关键事件和重要过程,例如:树突状细胞群早在受孕后7周就出现于胎肝和非淋巴系组织中等。
总之,这项研究克服了人体胚胎组织在收集方面的困难,利用细分时间点的单细胞水平测序对子宫内人体造血和免疫系统发育的动态过程进行了精准刻画,揭示了造血干细胞分化为各类血细胞和免疫细胞及迁移至不同器官中进行功能特化的路径,为理解这一涉及众多功能主体和复杂互作交流的生物学过程提供了助力,是发育生物学、免疫生物学和血液生物学领域中的宝贵资源。
研究人员揭示乳腺细胞发育中细胞状态特异性转录因子网络和细胞谱系关系
美国圣地亚哥的Salk研究所的Geoffrey Wahl团队近期在Cell Reports杂志上发表文章“Single-Cell Chromatin Analysis of Mammary Gland Development Reveals Cell-State Transcriptional Regulators and Lineage Relationships”,利用最前沿的单细胞染色质可接近性图谱揭示了正常乳腺发育过程中细胞状态特异性转录因子结合位点的变化动态和细胞谱系的关系。该团队希望通过了解乳腺正常发育过程中细胞状态转换的分子机理,在未来进一步理解乳腺癌细胞可塑性和异质性的分子机理。
在该研究中,作者们首次在染色质可接近性方面,观察到胚胎乳腺原基在胚胎发育晚期已经开始获得成年鼠分化乳腺细胞特异的染色质可接近性特征。进一步通过转录因子结合位点在染色质可接近区域的富集程度,推测了转录因子在不同细胞的活跃性。作者们利用机器学习的方法预测了细胞谱系特异性的转录因子,其中包括多个已经实验验证的乳腺细胞转录因子。根据推测的每个细胞中转录因子的活跃性所构建的拟时间发育轨迹,高度吻合单细胞转录组数据。
作者还发现,相对于启动子,位于基因启动子远端的增强子可接近性数据包含更多细胞状态特异性信息。根据具有配对关系的基因和远端增强子在单一细胞中的共同可接近性,作者们预测小鼠乳腺发育过程中远端增强子的靶基因。预测的基因与远端增强子关系图谱将会为乳腺研究领域提供一项可贵的资源。结合细胞谱系特异性染色质可接近性信息和H3K27ac染色质免疫共沉淀--高通量测序(ChIP-Seq)图谱,人们可以寻找自己感兴趣基因的增强子位置和细胞谱系特异性。作者还根据基因本身的可接近性和他所属的远端增强子的可接近性,预测了一万三千多个基因的可接近性。预测的基因可接近性数据高度与单细胞转录组数据吻合。
该研究成果将会为乳腺相关研究中具体的分子机理研究设立实验假说提供方便的基础资源。
研究人员构建癌症eRNA表达图谱并揭示其在癌症临床中的应用
近期德克萨斯大学休斯敦健康研究中心的韩冷、李文博课题组合作在Nature Communications上在线发表题为“Transcriptionallandscape and clinical utility of enhancer RNAs for eRNA-targeted therapy incancer”的研究。该研究构建了迄今为止最完整的癌症增强子RNA(eRNA)图谱并揭示了eRNA在癌症临床中的潜在应用。
该项研究通过检测eRNA在约1万名癌症病人及约1000个癌症细胞系中的表达构建了目前为止最全面的癌症eRNA图谱,揭示了eRNA的癌症特异性表达/癌症种系特异性表达的特征,同时强调了eRNA作为生物标记物在不同类型癌症临床上的应用。通过研究eRNA与转录因子之间的共表达关系,发现eRNA的特异性表达与转录因子特异性调控密切相关。通过分析eRNA与编码基因之间的基因组距离及表达相关性并结合多组Hi-C数据加以佐证,该研究构建了eRNA的调控网络,揭示了eRNA在调控致癌信号通路及调节癌症临床治疗基因中的关键作用。此外,该研究通过调查eRNA与抗癌化合物之间的关系,首次证实eRNA可影响癌症细胞对抗癌药物的敏感性和抵抗性,且该影响可能会关联到相关的一条或多条癌症信号通路。
这项研究拓展了该领域对癌症基因转录调控的认知,探索了基于靶向eRNA的癌症治疗及联合治疗方案,开拓了癌症治疗新思路。
来源:gh_0929b4a25094 新叶社
原文链接:http://mp.weixin.qq.com/s?__biz=MzIxMjY2NjY5Mg==&mid=2247486933&idx=2&sn=decb8fcfff71115cc78a3b27a6a6926b&chksm=9743ddfea03454e80dbaf1d17c56242c821fc20c551204c99b37a6cd3bc0fa2f62f2e1f7c894&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
上消化道内窥镜检查
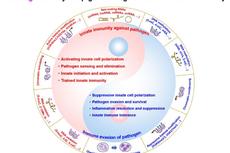
曹雪涛《NatRevImmunol》发表综述阐述抗感染固有免疫反应的表观遗传调控
上消化道摄影检查
上消化道内窥镜检查
下消化道摄影检查
消化道激素
上消化道X线钡餐
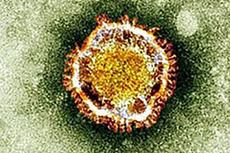
中东呼吸综合征病毒也可通过消化道感染人类
前列腺特异性抗原检查
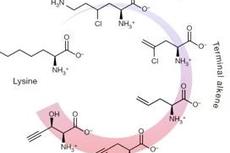
Nature | 为生物大分子的特异性标记提供理论基础——含炔烃氨基酸的生物合成