科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-11-29
来源:高分子科学前沿
细菌耐药基因的快速进化,超级细菌的不断出现和广泛传播已经成为全球面临的一个极具挑战的健康问题。中外研究人员甚至在牲畜和人身上发现了一种能对抗强效抗生素的“超级细菌”基因,这意味着人类所用抗生素中的“最后一道防线”有被攻破的风险 1 。据世界卫生组织预计,到2050年,全球由于细菌耐药性所导致的死亡人数将达到每年1000万,超过癌症引发的死亡人数。与耐药性的发展形成鲜明对比的是抗生素的开发愈发缓慢,2015年初,美国东北大学Kim Lewis教授成功发现了近30年来的第一个新型抗生素teixobactin2。
历时四年的不断探索, Kim Lewis教授团队再次发现一种新型抗生素——darobactin, 一种发光杆菌的代谢产物,含有7个氨基酸的短肽,可通过结合一个关键外膜蛋白bamA,选择性杀伤革兰氏阴性菌。本文提出一种新的杀菌机制,即通过抑制bamA外膜蛋白,破坏细菌外膜诱导细胞裂解,最终导致细菌原地爆炸(Nature, 2019, https://doi.org/10.1038/s41586-019-1791-1)。
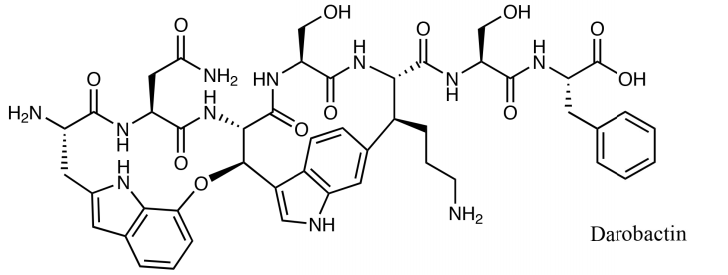
图1 Darobactin 结构
研究人员从67株嗜线虫致病杆菌和发光杆菌的代谢产物中,发现发光杆菌可产生抑制大肠杆菌E.coli的生长的化合物。经高效液相色谱和高分辨质谱的分离鉴定,NMR核磁结构分析,鉴定出该有效化合物为含有7个氨基酸的短肽W1-N2-W3-S4-K5-S6-F7,分子量996.4(如图1)。
荧光显微镜下观察发现大肠杆菌在darobactin作用后出现气泡、肿胀、爆炸的细胞形态。由于通常小于600Da的小分子才可以穿透细菌外膜,因此首先考虑该抗生素是否如多粘菌素一样作用于外膜的脂多糖LPS,但是结果发现添加LPS对darobactin杀伤大肠杆菌的效果并没有显著影响;继而研究者推测该短肽分子的靶标可能是外膜蛋白。为进一步探索darobactin的特异性结合蛋白,大肠杆菌在darobactin的sub-MIC压力下连续传代7天,获得三株darobactin耐受的菌株,对三株耐药菌株进行基因测序发现在一个关键外膜蛋白bamA的基因编码区出现了2-3个相同的突变,接着将这三个突变位点在野生型大肠杆菌中做等位突变,发现该野生型大肠杆菌即对darobactin出现显著耐药性,表明darobactin的靶标蛋白即bamA。最后研究人员通过小鼠实验,分别将敏感型和耐药性的大肠杆菌、绿脓假单抱杆菌以及肺炎链球菌注射入小鼠腹腔,发现darobactin均可以有效提高小鼠的生存率。
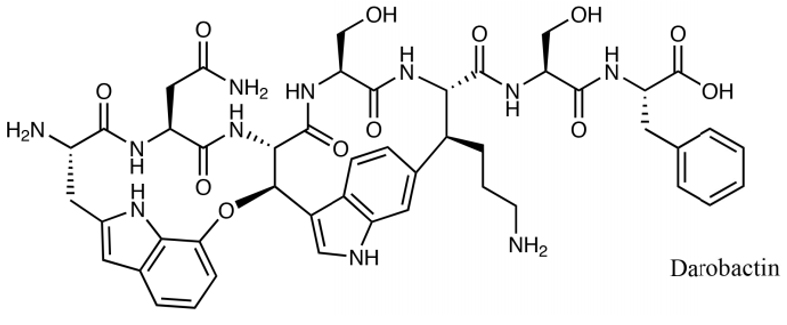 图2 Darobactin的结合靶点bamA外膜蛋白
图2 Darobactin的结合靶点bamA外膜蛋白
在耐药菌传播速度加快而抗生素开发极其缓慢的当下,Kim Lewis教授团队开发的新型抗生素无疑给全球健康带来了新的曙光。本文不仅鉴定出Darobactin 的结构,而且提出新的抗菌机制——结合关键外膜蛋白bamA,破坏细菌外膜诱导细胞裂解,导致细菌爆炸。
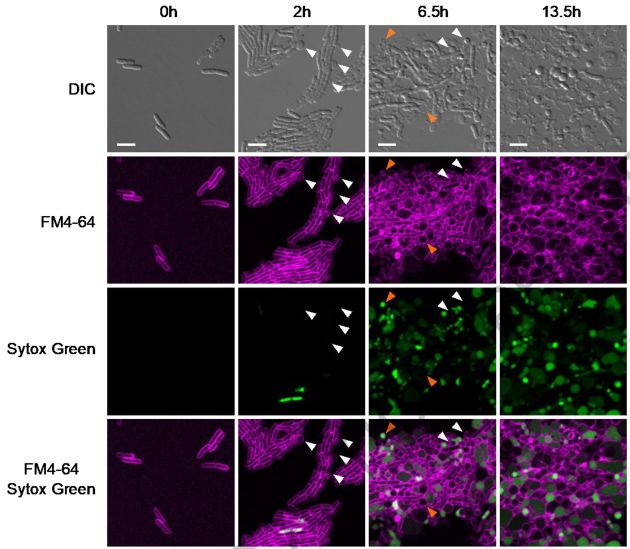
图3 Darobactin作用于E.coli不同时间内细胞形态的变化
原文链接:
https://www.nature.com/articles/s41586-019-1791-1#Sec40
参考文献:
1. Liu, Y.-Y.; Wang, Y.; Walsh, T. R.; Yi, L.-X.; Zhang, R.; Spencer, J.; Doi, Y.; Tian, G.; Dong, B.; Huang, X.; Yu, L.-F.; Gu, D.; Ren, H.; Chen, X.; Lv, L.; He, D.; Zhou, H.; Liang, Z.; Liu, J.-H.; Shen, J., Emergence of Plasmid-Mediated Colistin Resistance Mechanism Mcr-1 in Animals and Human Beings in China: A Microbiological and Molecular Biological Study. The Lancet Infectious Diseases 2016, 16, 161-168.
2. Ling, L. L.; Schneider, T.; Peoples, A. J.; Spoering, A. L.; Engels, I.; Conlon, B. P.; Mueller, A.; Schaberle, T. F.; Hughes, D. E.; Epstein, S.; Jones, M.; Lazarides, L.; Steadman, V. A.; Cohen, D. R.; Felix, C. R.; Fetterman, K. A.; Millett, W. P.; Nitti, A. G.; Zullo, A. M.; Chen, C., et al., A New Antibiotic Kills Pathogens without Detectable Resistance. Nature 2015, 517, 455-459.
来源:Polymer-science 高分子科学前沿
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5NjM5NzA5OA==&mid=2651724644&idx=5&sn=181ae69661d1442e11b5958fb9d77004&chksm=8b4a0921bc3d8037898a34444c74373fec18899f9480bcc1f5879fdd2c06eb95f0148ce8449a&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
更好的期刊,更好的科学——中国科技峰会·世界科技期刊论坛专家观点荟萃



Nature论文称,替代新烟碱的杀虫剂仍会伤害蜂群
华侨大学博士生首次在Nature发文




大型恒星比想象的更多

新突破! 二维实验系统成功应用于四维材料研究

研究分析石墨烯基纳米材料对土壤细菌菌群结构和功能的影响

利用“阿尔法折叠”预测结构,细菌“注射器”将蛋白输入人体细胞
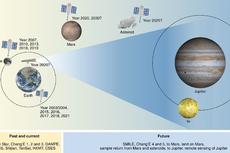
魏勇等-Nature Astronomy:中国的行星探索路线图

耐药超级细菌外部蛋白质结构曝光 就像身披“锁子甲”
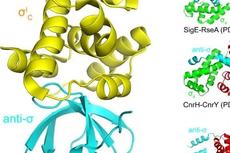
研究揭示出一类新的细菌转录调控因子的结构功能机制