科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-10-04
FTO 与多基因肥胖具有最强的遗传关联,IRX3 介导 FTO 对体重的影响。
然而,对哪些细胞以及 IRX3 如何进行这种控制知之甚少。
2021年9月23日,北京大学邱义福团队在Nature Immunology 在线发表题为“Macrophage IRX3 promotes diet-induced obesity and metabolic inflammation”的研究论文,该研究发现巨噬细胞 IRX3 促进代谢炎症以加速肥胖和 2 型糖尿病的发展。
通过增加适应性产热作用,具有 Irx3 髓样特异性缺失的小鼠免受饮食诱导的肥胖和代谢疾病的侵害。
从机制上讲,巨噬细胞 IRX3 促进促炎细胞因子转录,从而抑制脂肪细胞肾上腺素信号,从而抑制脂肪分解和产热。
JNK1/2 磷酸化 IRX3,导致其二聚化和核转位以进行转录。
此外,脂多糖刺激通过抑制泛素化来稳定 IRX3,从而增强 IRX3 的转录能力。
总之,该研究发现确定了一个新的参与者,巨噬细胞 IRX3,它控制体重和代谢炎症,暗示 IRX3 作为治疗靶点。
肥胖是由能量不平衡引起的脂肪组织的积累,即能量摄入长期超过能量消耗。
脂肪组织,包括棕色脂肪组织 (BAT) 和白色脂肪组织 (WAT),在哺乳动物的能量稳态中发挥着重要作用。
当营养充足时,WAT 储存能量,而 BAT 通过线粒体解偶联蛋白 1 (UCP1) 介导的解偶联呼吸消耗能量以产生热量。
脂肪细胞亚群,主要分散在皮下 WAT (scWAT) 中,称为米色脂肪细胞,表达 UCP1 和其他产热相关蛋白,以在暴露于寒冷环境或产热刺激下时产生热量 。
经典棕色脂肪细胞和新发现的米色脂肪细胞的适应性产热可以增加全身能量消耗,因此具有预防肥胖及其相关代谢疾病(如 2 型糖尿病)的潜力,这两种全球流行病成为人类社会主要的公共卫生威胁和沉重的经济负担。
除了脂肪细胞外,脂肪组织中还存在不同类型的免疫细胞,其中巨噬细胞是研究最广泛的,称为脂肪组织巨噬细胞 (ATMs)。
在健康和稳态条件下,ATM 与脂肪细胞协同工作以协调全身能量代谢。
然而,慢性能量过剩会刺激脂肪组织扩张并创造一个微环境,在这个微环境中,促炎巨噬细胞被招募和激活,以促进慢性炎症,局部产生白细胞介素 (IL)-1、IL-6 和肿瘤坏死因子 (TNF)。
这些促炎细胞因子已被证明是胰岛素抵抗和 2 型糖尿病发病机制的关键因素,可能是通过抑制儿茶酚胺诱导的脂肪分解和产热。
因此,了解促炎细胞因子表达的调控机制至关重要。
脂肪量和肥胖相关基因 (FTO) 的变体与人类多基因肥胖具有最强的遗传关联。
Fto-null 小鼠的体重和脂肪量减少。
相比之下,过度表达 Fto 的小鼠表现出肥胖表型。
然而,FTO 的表达或功能并未与其肥胖相关的变体直接相关。
2014 年,一项研究表明 FTO 遗传变异与易洛魁人 homebox 基因 3 (IRX3) 表达在控制体重方面存在联系,后者通常参与组织/器官模式或发育 。
该报告表明,位于 FTO 第一个内含子区域的增强子对 IRX3 的启动子发挥长程调控作用,导致脑内 IRX3 的高表达,从而抑制全身能量通过损害脂肪细胞的交感神经支配来消耗。
使用不同的方法,另一组证实了 FTO 的第一个内含子对 IRX3 基因表达的长程调节作用,并进一步揭示 IRX3 调节白色和米色脂肪细胞之间的细胞命运选择。
他们通过不同的细胞类型研究了 IRX3 的功能,但两项研究都得出结论,IRX3 与适应性产热呈负相关。
然而,两项后续研究持不同观点。
据报道,IRX3 与 UCP1 的启动子结合以驱动其转录,从而增加脂肪细胞的产热。
此外,另一项研究表明,部分抑制小鼠下丘脑 Irx3 表达会降低 Ucp1 表达并加剧肥胖。
这些不一致的结果表明可能存在其他细胞类型和机制负责 FTO-IRX3 回路与肥胖之间的遗传关联。
在这里,该研究报告了巨噬细胞 IRX3 在控制体重、代谢炎症及其相关的胰岛素抵抗和代谢功能障碍方面的新功能。
该研究发现IRX3在被巨噬细胞中的 JNK1/2 磷酸化和激活时,通过与其启动子区域结合来促进促炎基因表达,从而抑制脂肪细胞的脂肪分解和产热。
这些发现揭示了 IRX3 在 ATM 中调节能量消耗和葡萄糖稳态的新作用。

来源:iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247536876&idx=4&sn=2db8b21eaa1b32ccedc4c21fbb3b941d
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
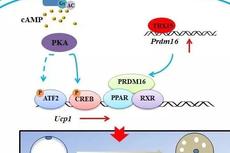
脂肪细胞转换调控机制研究取得进展
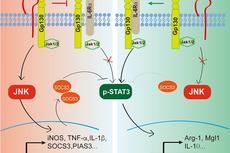
生物物理所揭示脂肪组织巨噬细胞促炎性极化的分子机制
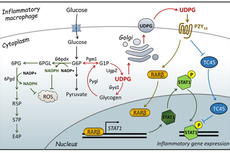
黄波团队揭示糖原代谢调控炎性巨噬细胞形成
研究揭示胆固醇代谢调控巨噬细胞抗肿瘤新机制

细胞脂肪如何“防感冒”?

肉桂香料可以燃烧脂肪细胞
Cell Metabolism:科学家发现巨噬细胞可通过清除体内排出的受损线粒体实现棕色脂肪组织的高效产热

浙大王迪团队揭示氨基酸代谢调控炎症性巨噬细胞活化的免疫代谢新机制

挖掘脂肪细胞,或是控制心血管代谢疾病的新路子
谢琦博士等解析胶质瘤干细胞脂肪酸代谢的表观调控机制