科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-10-10
多发性骨髓瘤 (MM) 是骨髓中的一种无法治愈的浆细胞恶性肿瘤,其特征是染色体不稳定性 (CIN),这会导致异质性的获得,以及多发性骨髓瘤的进展、耐药性和复发。
2021年10月7日,南京中医药大学杨烨,顾晓松及顾春艳共同通讯在Signal Transduction and Targeted Therapy (IF=18.19)在线发表题为“BUB1B and circBUB1B_544aa aggravate multiple myeloma malignancy through evoking chromosomal instability”的研究论文,该研究阐明了 BUB1B 的表达在 MM 患者中显著增加,并且与不良结果密切相关。
BUB1B 的过表达促进了细胞增殖并在体外和体内诱导了耐药性,而靶向基因BUB1B 则消除了这种影响。
机制研究表明,BUB1B 的强制表达会引起 CIN,主要通过磷酸化 CEP170 导致 MM 不良结果。
有趣的是,该研究发现存在包含 BUB1B 激酶催化中心的 circBUB1B_544aa,该中心由 BUB1B 的环状 RNA 翻译。
MM外周血样本中circBUB1B_544aa升高与MM不良结局密切相关,并与BUB1B在诱发CIN方面发挥协同作用。
此外,MM细胞可以分泌circBUB1B_544aa并以与BUB1B全长蛋白相同的方式干扰MM微环境细胞。
有趣的是,针对 BUB1B 和 circBUB1B_544aa 的激酶催化中心的 BUB1B siRNA 在体外和体内显著抑制了 MM 恶性肿瘤。
总的来说,BUB1B 和 circBUB1B_544aa 是 MM 有希望的预后和治疗靶点。
多发性骨髓瘤 (MM) 是一种起源于骨髓 (BM) 的分子和细胞遗传学异质性血液系统恶性肿瘤。
尽管几十年来免疫调节剂和蛋白酶体抑制剂等靶向药物极大地改善了 MM 患者的预后,但 MM 仍然危及生命且无法治愈。
众所周知,遗传和表观遗传畸变、克隆异质性和克隆进化在 MM 进展、耐药性和复发中起着不可或缺的作用。
然而,MM发病机制的分子基础仍未完全了解。
染色体不稳定性 (CIN) 加速了 MM 恶性肿瘤和耐药性的发展,导致治疗失败和复发,这限制了大多数当前疗法的有效性。
因此,鉴定涉及的新分子和信号通路在CIN和MM的关系中是必不可少的。
BUB1 有丝分裂检查点丝氨酸/苏氨酸激酶 B (BUB1B) 是一种保守的多功能蛋白,对有丝分裂纺锤体检查点的功能和纠正动粒-微管附着至关重要。
已证实 BUB1B 的失活会导致纺锤体检查点和严重的染色体分离缺陷。
据报道,BUB1B 的广泛升高与包括 MM 在内的各种癌症的高细胞增殖和不良临床结果密切相关。
通过在 MM 患者样本中采用序列基因表达谱 (GEP),发现 BUB1B 在 MM 中诱导 CIN。
然而,BUB1B 介导的 MM 促进的确切机制仍然不明确。
文章模式图(图源自Signal Transduction and Targeted Therapy )MM高度依赖于BM微环境,MM对应细胞与BM中其他细胞的相互作用对MM疗法的发展具有重要意义。
环状 RNA 是单链闭合 RNA 分子,它们源自前体 mRNA 反向剪接,形成共价闭合的环。
特别是,circRNA 已被阐明在癌症的发生、发展、侵袭和耐药性中起关键作用。
重要的是,circRNA 通过细胞间通讯对肿瘤微环境产生重要影响,这归因于它们在外泌体和人体体液中的丰度。
因此, circRNA 现在被视为有前景的癌症生物标志物。
在这项研究中,不仅表征了 BUB1B 在 MM 细胞增殖和耐药性中的作用,而且还确定了 BUB1B 基因的环状形式在 MM 细胞中编码了一种新的 544 个氨基酸的蛋白质,称为 circBUB1B_544aa。
有趣的是,circBUB1B_544aa 含有 BUB1B 激酶催化中心,可能会分泌到 BM 微环境中,体外和体内研究了其在 MM 中的潜在作用。
该研究还采用临床样本和患者数据来评估 BUB1B 或 circBUB1B_544aa 表达与患者预后之间的关系。
最后,该研究展示了 BUB1B 和circBUB1B_544aa 的新下游靶标。
这些发现为 BUB1B 和 circBUB1B_544aa 作为 MM 有希望的预后和治疗靶点的功能重要性提供了重要见解。


来源:iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247537353&idx=7&sn=295b672ff16f8c972ae43b9e0f9b299e
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
第22届全国肿瘤防治宣传周启动仪式在北京举行




气候变化加剧抗生素耐药性

青霉素:从发现、作用到耐药性
哈佛大学医学院Kucherlapati教授访问中国抗癌协会



有一种氨基酸吃多了,会增加癌症的耐药性

速览 | 饿死黑色素瘤癌细胞解决耐药性?
从“细菌耐药性”认识2OG加氧酶
澳大利亚icon医疗集团访问中国抗癌协会秘书处


Nature:揭示染色体碎裂导致癌细胞耐药性机制
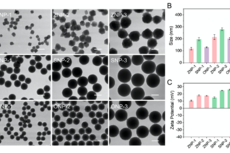
上海交大窦红静教授研究纳米材料用于单细胞水平癌症耐药性诊断获进展