科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-02-13
来源:BioArt
恶性肿瘤因快速生长而导致其对营养和氧气的需求远超正常组织。一方面,肿瘤细胞通过糖酵解分解葡萄糖而获得能量,并产生大量乳酸造成肿瘤酸化微环境;另一方面,大量生长因子的分泌刺激未成熟血管的生成,造成肿瘤血管形态异常化。异常的血管形态导致血流不畅且易漏、氧气供应减少,引起肿瘤组织发生缺氧、酸化及组织液高压,使得免疫细胞和抗癌药物无法到达病灶,大大降低治疗效果。传统的抗血管生成策略主要通过抑制肿瘤血管生成,限制肿瘤获得氧供和营养物质,进而抑制肿瘤生长和转移。这种疗法往往会引起肿瘤血管的过度“修剪”(excessive pruning)而快速引起耐药,加剧肿瘤恶化。因此,寻找一种既能恰当地修剪异常化的肿瘤血管(即减少血管生成)又能正常化剩余血管的策略,已成为近年来抗血管生成治疗和药物研发领域的努力方向。
2020年2月10日,中国药科大学吴照球团队在J Clin Invest上在线发表题为 Inactivating endothelial ZEB1 impedes tumor progression and sensitizes tumors to conventional therapies 的研究论文,揭示了血管内皮ZEB1蛋白在肿瘤发生发展中的关键作用及分子机制,并提出了靶向ZEB1蛋白联合常规化疗或免疫检查点阻断疗法的肿瘤治疗新策略。

作者报道锌指转录因子ZEB1在癌旁组织中低表达(或无表达)而在癌组织的内皮细胞中特异性高表达,其表达水平与肿瘤病理分级、远端转移正相关,与病人的总生存率负相关。接着,作者应用构建的内皮细胞特异性ZEB1敲除小鼠移植瘤模型,发现敲除ZEB1不影响荷瘤鼠重要生命器官的组织学结构和生理功能;在减少肿瘤血管生成的同时也促进剩余血管的正常化(如增加血管完整性、增强血管灌注功能以及减少红细胞和组织液外漏等),进而改善肿瘤内部缺氧、高酸的恶性环境,抑制肿瘤增殖和器官转移。此外,敲除ZEB1也促进了免疫细胞特别是CD4+、CD8+效应性T细胞向肿瘤深部的浸润,增强肿瘤对低剂量一线化疗药顺铂和免疫检查点抑制剂anti-PD-1抗体的应答(可引发肿瘤消退)。
机制研究结果表明,敲除肿瘤内皮细胞ZEB1抑制组蛋白乙酰基转移酶CBP/p300募集至TGFβs(包括TGFβ1、TGFβ2、TGFβ3)基因启动子,下调启动子上H3K4Ac、H3K14Ac、H3K18Ac等组蛋白的乙酰化水平,进而抑制TGFβs基因的转录、翻译及分泌(至周边微环境),并最终抑制胞内及胞外TGFβ/SMAD信号通路。敲除肿瘤内皮细胞ZEB1一方面通过抑制ZEB1/TGFβ/SMAD/VEGFA-ANG2信号轴并经自分泌途径减少异常化血管生成、促进剩余血管正常化,改善血管灌注功能,增加免疫细胞浸润和药物运送;另一方面通过抑制ZEB1/TGFβ/SMAD信号轴并经旁分泌途径抑制肿瘤细胞的增殖、血管渗入、血道转移和淋巴转移,增加抗肿瘤免疫(图1)。
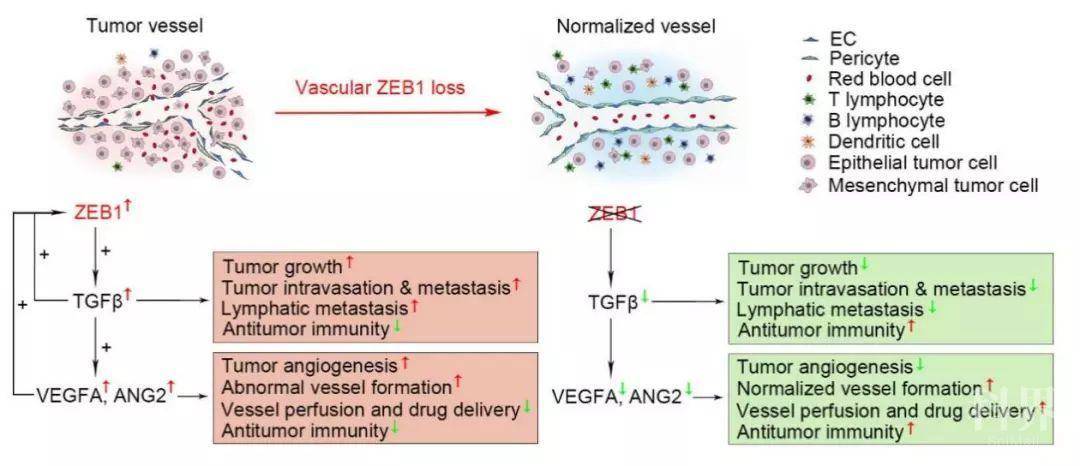
图1. ZEB1/TGFβ信号轴促进肿瘤恶性进展
课题组成员傅蓉副教授、博士生李艺、硕士生姜楠和博士生任博雪为本文的共同第一作者,吴照球教授为通讯作者。中国药科大学副校长陆涛教授对论文亦有重要贡献。
原文链接:
https://doi.org/10.1172/JCI131507.
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652480899&idx=6&sn=3cdc09f60ef3c9341cbe3800b2f8bf51&chksm=84e23637b395bf2127597620fcdb22195401c06b7376a39cc77bf22f71a1843ffeedb80fee43#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
中国微循环学会周围血管疾病专业委员会2016学术年会暨第三届朝阳血管医学论坛
蛋白质组学数据再分析揭示泛素降解系统在肿瘤发生中关键作用

3D生物打印血管动物试验成功
周围血管疾病专委会成功开展“京郊行”首站顺义:基层医师血管疾病普及与提高讲习班

新突破!开启肿瘤治疗新模式,蒋争凡/韩为东/梅倩揭示锰离子在抗肿瘤的关键作用

“敲骨吸髓”在人类手部进化中起到了关键作用

发挥智库在现代治理中的关键作用
中国抗癌协会肿瘤介入学专业委员会换届会议召开




应对全球气候变化,林业将起关键作用
中国微循环学会周围血管疾病专业委员会成功召开2015学术年会暨第二届朝阳血管医学论坛