科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-02-19
来源:BioWorld
北京时间2月19日凌晨,西湖大学周强实验室在预印版平台bioRxiv在线发表了题为Structure of dimeric full-length human ACE2 in complex with B0AT的研究论文。 新型冠状病毒感染引发的肺炎疫情爆发后,武汉病毒研究所的科学家发现,新型冠状病毒和2003年的SARS病毒一样,也是通过识别ACE2蛋白进入人体细胞的,ACE2是“新冠病毒”侵入人体的关键。研究发现,在SARS病毒和“新冠病毒”侵入人体的过程中,ACE2就像是“门把手”,病毒抓住它,从而打开了进入细胞的大门。
新型冠状病毒感染引发的肺炎疫情爆发后,武汉病毒研究所的科学家发现,新型冠状病毒和2003年的SARS病毒一样,也是通过识别ACE2蛋白进入人体细胞的,ACE2是“新冠病毒”侵入人体的关键。研究发现,在SARS病毒和“新冠病毒”侵入人体的过程中,ACE2就像是“门把手”,病毒抓住它,从而打开了进入细胞的大门。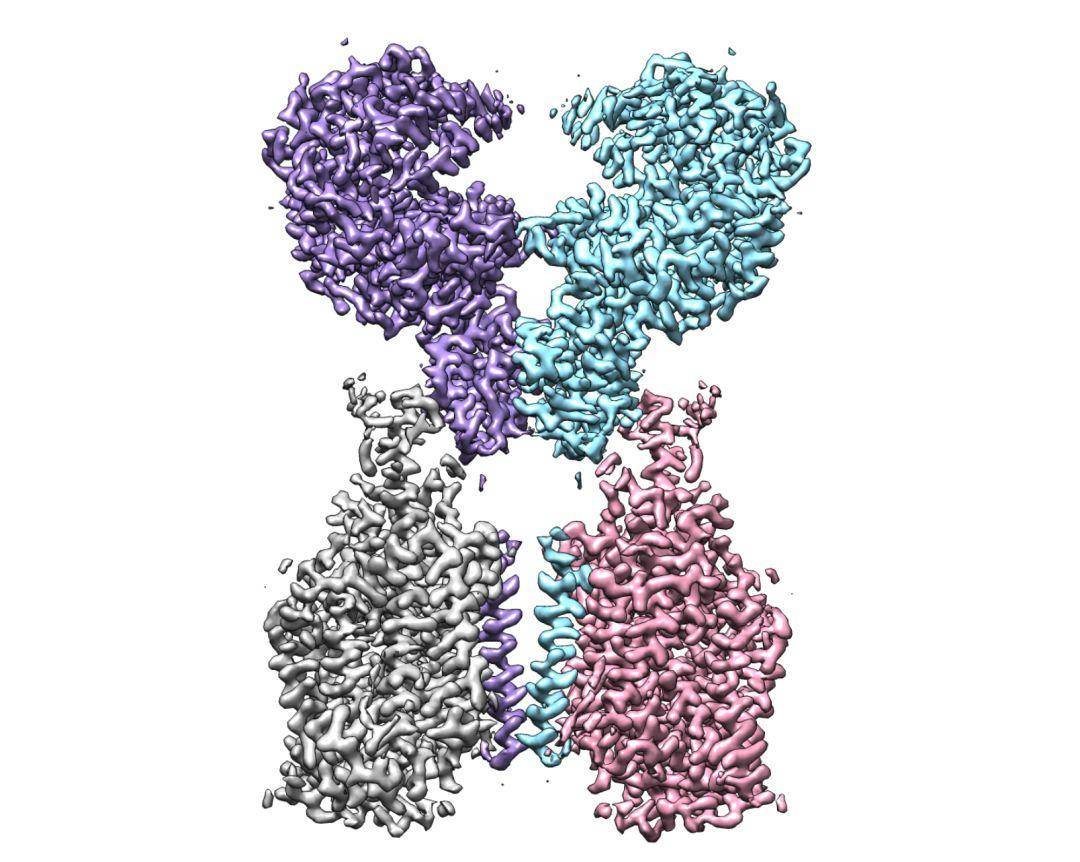
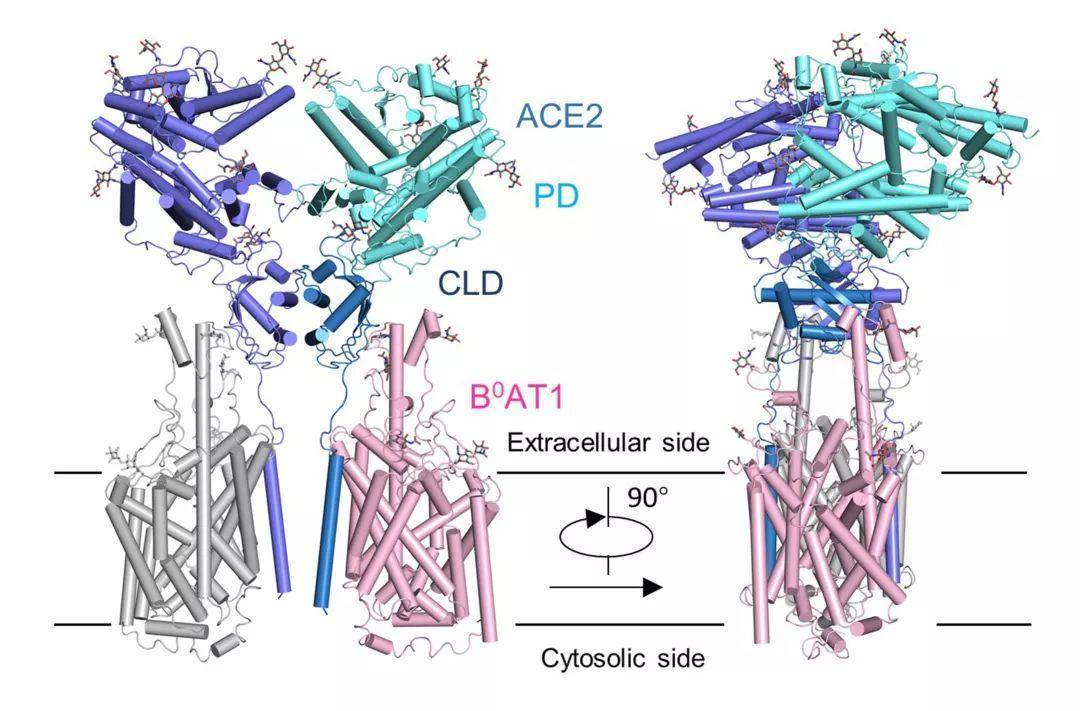
ACE2-B0AT1 复合物结构图
周强实验室针对这个问题进行了攻坚。第一步,他们要获取ACE2蛋白全长蛋白,但作为膜蛋白的ACE2本身很难在体外稳定获得。周强及博士后鄢仁鸿在文献中发现ACE2与肠道内的一个氨基酸转运蛋白B0AT能够形成复合物。根据他们过去的研究经验,这个复合物极有可能稳定住ACE2。果然,他们通过共表达的方法获得了ACE2与B0AT优质稳定的复合物,并利用西湖大学的冷冻电镜平台成功解析了其三维结构,分辨率达到2.9埃,对于病毒识别至关重要的胞外结构域分辨率为2.7埃。(注:3埃是评价蛋白质结构分辨率的分界点。3埃以内的可以认为是高分辨率结构,在电子密度图上可以很清楚的确定侧链构象,侧链之间的盐键,氢键等相互作用。)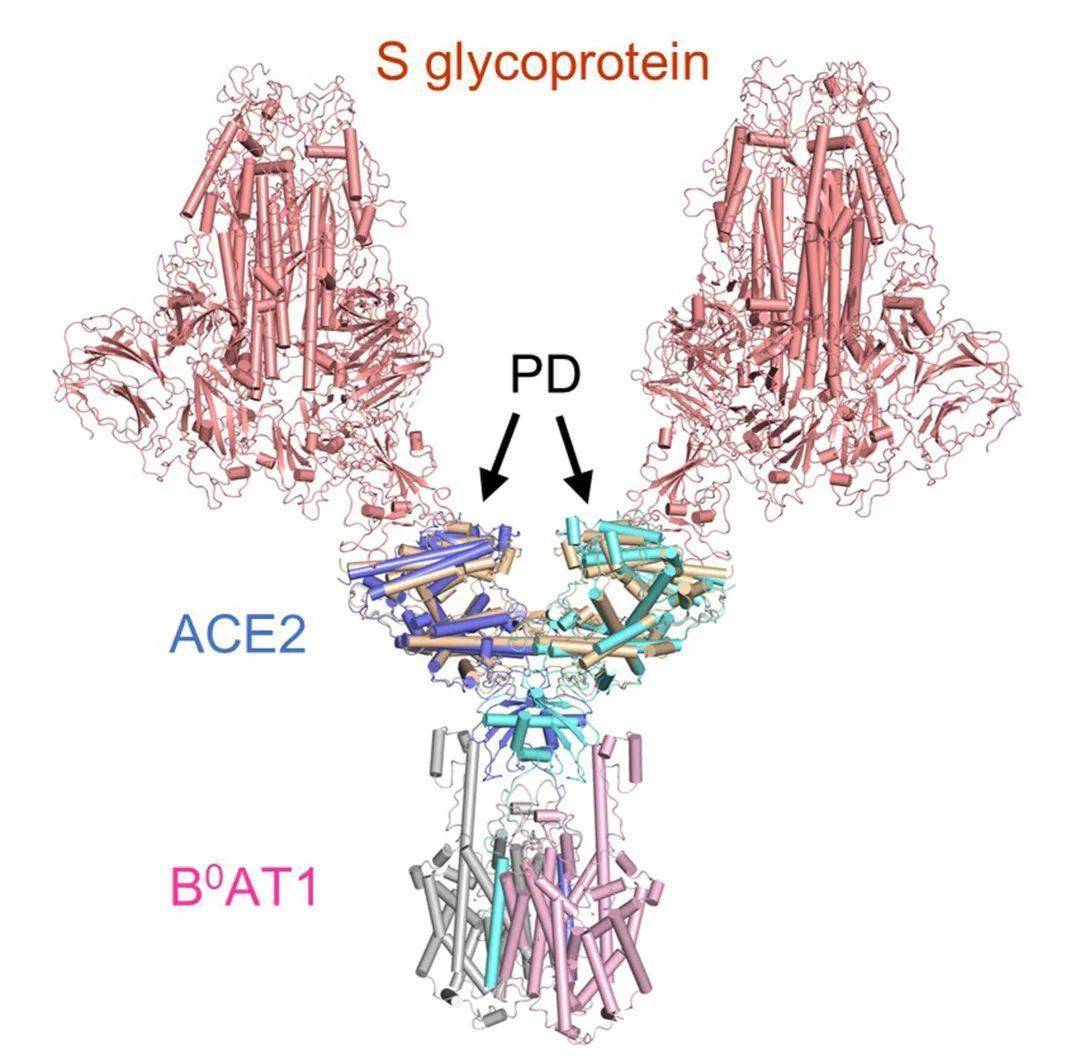 ACE2-B0AT1 复合物和之前解析复合物(SARS-CoV的S蛋白与ACE2的PD结构域的复合物)的比较,两种复合物通过PD结构域锚定在一起。通过分析ACE2的全长蛋白结构,周强实验室发现ACE2以二聚体形式存在,同时具有开放和关闭两种构象变化,但两种构象均含有与冠状病毒的相互识别界面。这一研究发现为进一步解析全长ACE2和新冠病毒的S蛋白复合物的三维结构奠定了基础。而这个工作本身为理解新冠病毒侵染细胞提供了很多有趣的线索。比如,ACE2的二聚体与新冠病毒S蛋白的三聚体是否可以发生更高层级的交联,从而促进病毒与宿主细胞膜的融合或者内吞?之前有研究表明ACE2的胞外区如果被切割,将会更有效地促进冠状病毒的侵染,但是ACE2与B0AT的复合物结构显示B0AT的存在有可能阻碍蛋白酶靠近这个切割位点,这是否解释了病毒侵染症状主要发生在没有B0AT的肺部?“总之,ACE2全长结构的解析,将有助于理解冠状病毒进入靶细胞的结构基础和功能特征,对发现和优化阻断进入细胞的抑制剂有重要作用”,清华大学全球健康与传染病研究中心主任张林琦教授说。
ACE2-B0AT1 复合物和之前解析复合物(SARS-CoV的S蛋白与ACE2的PD结构域的复合物)的比较,两种复合物通过PD结构域锚定在一起。通过分析ACE2的全长蛋白结构,周强实验室发现ACE2以二聚体形式存在,同时具有开放和关闭两种构象变化,但两种构象均含有与冠状病毒的相互识别界面。这一研究发现为进一步解析全长ACE2和新冠病毒的S蛋白复合物的三维结构奠定了基础。而这个工作本身为理解新冠病毒侵染细胞提供了很多有趣的线索。比如,ACE2的二聚体与新冠病毒S蛋白的三聚体是否可以发生更高层级的交联,从而促进病毒与宿主细胞膜的融合或者内吞?之前有研究表明ACE2的胞外区如果被切割,将会更有效地促进冠状病毒的侵染,但是ACE2与B0AT的复合物结构显示B0AT的存在有可能阻碍蛋白酶靠近这个切割位点,这是否解释了病毒侵染症状主要发生在没有B0AT的肺部?“总之,ACE2全长结构的解析,将有助于理解冠状病毒进入靶细胞的结构基础和功能特征,对发现和优化阻断进入细胞的抑制剂有重要作用”,清华大学全球健康与传染病研究中心主任张林琦教授说。
周强(右)和鄢仁鸿(左)
周强博士,1982年出生,黑龙江人。2000-2004年本科就读于清华大学,获学士学位。2004-2012年博士师从隋森芳院士,获博士学位。2015年博士后出站后在清华大学医学院颜宁教授课题组任副研究员。2019年初加盟西湖大学担任西湖学者、特聘研究员,开展独立研究工作。来源:ibioworld BioWorld
原文链接:https://mp.weixin.qq.com/s?__biz=MzU1MzMxMzcyMg==&mid=2247497230&idx=2&sn=e8e9b58471d38a9cca8f5f4379c9bb88&chksm=fbf602dbcc818bcd86a9f7d041258a1b96a659a3898358fc1ab7381657fc4458f24d30072579#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
武汉新型冠状病毒与SARS冠状病毒约有70%相似

【权威观点】专家:新型冠状病毒不是SARS冠状病毒
具有广谱抗人冠状病毒活性的多肽类融合抑制剂

【学术前沿】bioRxiv | 单细胞测序分析技术进一步揭示新型冠状病毒受体的组织和人群特征分布情况
单细胞测序分析技术进一步揭示新型冠状病毒受体的组织和人群特征分布情况
新型冠状病毒浅析

【权威观点】专家:新型冠状病毒不是SARS冠状病毒
如何预防新型冠状病毒
从“新型冠状病毒肺炎”揭新冠状病毒的身世之迷

Nature | 新冠病毒由穿山甲冠状病毒和蝙蝠冠状病毒重组而来