科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-03-31
来源:BioArt
胰腺癌(Pancreatic adenocarcinoma)是一种恶性程度极高的消化系统肿瘤,其发病率与死亡率几乎相当。据统计, 全美胰腺癌患者五年总体生存率不足7%。预计到2030年,它将超过乳腺癌、前列腺癌和结肠直肠癌,成为癌症死亡的主要原因之一【1】。早期诊断困难与缺乏有效的个体化治疗方案是导致胰腺癌预后极差的重要原因, 80%左右患者确诊时已发生肿瘤外周侵犯或远处转移,无法接受手术治疗。为了在可能治愈的阶段准确诊断胰腺癌,需要特异性、敏感性和微创性的生物标志物,而识别用于PC筛查的有效生物标志物是一项重要的未满足临床需要的工作。
近年来,以游离DNA( cell-free DNA, cfDNA)检测为代表的“液体活检”技术正成为恶性肿瘤、产前诊断和器官移植排异监测的新兴标志物【2】。外周循环中的cfDNA来源多样,包括细胞核基因组片段、线粒体核酸以及外泌体囊泡中核酸片段等,其中高度破碎的基因组片段cfDNA的主要组成部分。在癌症患者体内,肿瘤细胞在凋亡、坏死等过程中也会释放出一定量的核酸片段。目前,ctDNA的检测主要通过数字微滴PCR(droplet digital PCR, ddPCR)或者二代测序技术(Next generation sequencing, NGS)。ddPCR技术检测单点突变具有很高的灵敏度和特异性,目前已经广泛应用于肺癌cfDNA中EGFR靶点突变的检测;但由于技术限制,ddPCR很难检测短核苷酸链上的基因突变,且无法在基因组层次上对ctDNA进行大规模测序,使得ddPCR技术无法宏观描绘ctDNA突变的基因组图谱,在一定程度上限制了ddPCR的应用前景。NGS可以在基因组水平检测ctDNA携带的突变,但目前NGS方法检测ctDNA突变的灵敏度和特异性还有待进一步提高,受到建库方法和测序深度的影响比较大;尤其是超深度测序时,NGS检测ctDNA的成本较高。目前NGS检测ctDNA,研究人员主要通过双链DNA(double-strand DNA, dsDNA)方法构建cfDNA测序文库。该方法对cfDNA测序效果不佳,目前推测可能有多种原因导致了双链建库检测ctDNA突变效率较低:1)dsDNA建库方法对超短或部分降解的核酸序列建库效率较低,而cfDNA主要富集于约160bp长度,部分携带突变的ctDNA分子片段长度可能更低(约150bp左右),且cfDNA可能高度降解,因而导致双链建库测序无法高效转化cfDNA进行测序;2)外周cfDNA中尤其是其外泌体DNA中可能包含部分降解后的单链DNA短片段,dsDNA建库方法后该部分片段会导致该部分游离核酸分子直接丢失。
考古研究过程中,研究人员往往会对古生物残存的DNA进行测序,对古生物进行分类并鉴定其起源,但古生物DNA也往往高度降解残缺不全,致使双链DNA建库检测古生物基因组效能较低。2012年,Science 杂志报道Meyer等人引入了一种基于单链DNA(single-strand DNA, ssDNA)连接的测序文库制备方法【3】,并通过对已灭绝古人类基因组测序,证明该方法对高度降解破损的DNA片段测序效果更佳。ssDNA文库制备方法还可以的保留cfDNA中线粒体、微生物和部分外泌体来源的核酸片段携带的信息。近几年来,已经开始有研究小组报道使用 ssDNA测序文库对基因组或cfDNA测序,进行肿瘤基因组的分析或检测器官移植后的免疫排异反应。ssDNA建库检测器官移植患者血浆中线粒体和微生物源cfDNA的效率远高于dsDNA建库方法。2017年12月,无创产检的创始人卢煜明教授发表论文支出,ssDNA建库相对于dsDNA建库检测cfDNA,可能会富集孕妇血浆中短片段的胎儿DNA。根据以上论据和理论,仇子龙研究组提出科学假设,采用ssDNA建库方法有可能会提高癌症患者cfDNA建库转化效率,提高ctDNA中超低丰度突变的检出。
2019年3月9日,中国科学院上海生命科学研究院神经科学研究所仇子龙研究员联合复旦大学附属中山医院介入治疗科王小林教授课题组、胰腺外科楼文晖教授团队近日在EBiomedicine上合作发表题为 Enrichment of short mutant cell-free DNA fragments enhanced detection of pancreatic cancer的研究论文,提出了基于单链建库的cfDNA建库和测序方法,通过该方法较之传统的测序和PCR方法能显著提高ctDNA中低丰度突变的检出率;当肿瘤cfDNA水平较低时,如早期疾病或症状前疾病时,意义尤为重大。期刊配发了西班牙卡哈尔研究所Julie Earl教授的述评文章Towards a more sensitive detection of somatic mutations in cell-free DNA,对本文进行了解析和高度评价。

本研究建立了一种ssDNA建库进行cfDNA测序的新方法(single-strand library preparation and hybrid-capture-based cfDNA sequencing,SLHC-seq),并验证了在极低总样本量的情况下,ssDNA建库测序检测和定量基因组中超低丰度突变的效能远高于目前常用的基于双链的建库方法。研究者收集不同分期的胰腺癌患者,评估了这些患者外周cfDNA的浓度,并通过ssDNA方法鉴定了胰腺癌ctDNA的突变图谱。
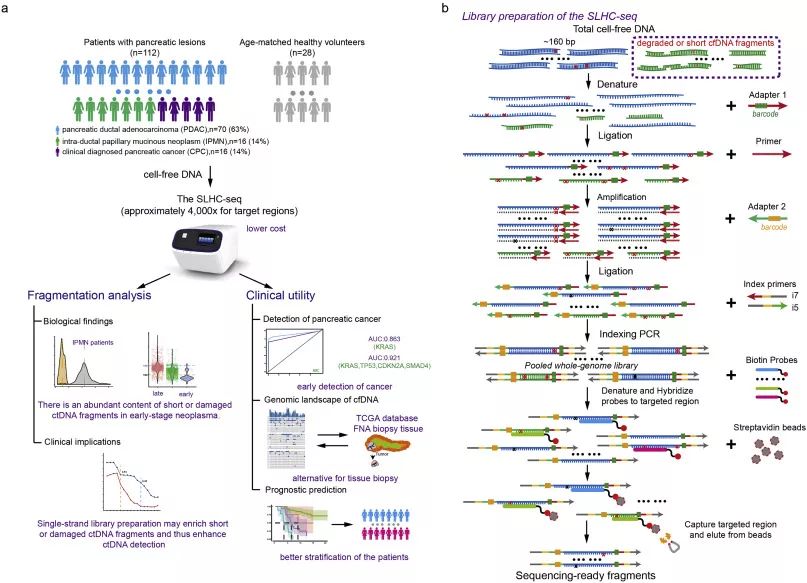
cfDNA的研究设计与单链文库制备。cfDNA片段首先变性为单链DNA (ssDNA)片段。然后,将ssDNA片段与一个唯一的分子标识符连接。利用杂交和磁珠捕获技术对预库进行富集,然后进行高通量测序。
本文描述了一种单链库制备法,用于临床队列中PC和健康对照者的游离DNA (cfDNA)测序。cfDNA分析的一个主要缺陷是高分子量基因组DNA的污染,它是在提取血液并离心提取血浆时从健康的血细胞中产生的。SLHC-seq法富集降解ctDNA的cfDNA短片段,对去除污染的高分子量基因组DNA具有重要意义。本研究意义在于,这种单链文库制备方法比传统的测序和PCR方法敏感得多。此外,该方法也可应用于石蜡包埋的组织标本、胰液或囊肿液等非液体活检标本,这些标本在DNA降解、数量少、质量低等方面与液体活检标本有相似的缺陷。与其他使用液体活检的肿瘤突变检测方法相比,该方法检测突变的效率更高。当肿瘤cfDNA水平较低时,如早期疾病或症状前疾病时,这一点尤为重要。
胰腺癌起病隐匿,早期就已是全身疾病。胰腺癌存在的KRAS、TP53、CDKN2A和SMAD4体细胞突变,可作为肿瘤cfDNA的特异性标志物,用于检测这些患者的播散性或残留性疾病。本研究还发现早期患者中普遍存在小突变片段,这可能是一种基于片段大小的胰腺癌早期检测策略。这对于家族性胰腺癌、可疑胰腺病变和晚发性糖尿病患者等高危人群的早期检测具有重要意义。

卡哈尔研究所Julie Earl教授在述评中高度评价了该研究,指出本研究所述的方法也适用于其他类型的需要液体活检的肿瘤。此外,深化了对液体活检样本的cfDNA的高效、有效地测序提供了新的思路。并认为该技术该研究具有很强的向临床转化的可能,这无疑将对肿瘤患者的临床诊疗产生积极的影响,并为预后不良的胰腺和其他肿瘤类型提供更加个性化的治疗方法。
据悉,该文章的第一作者为刘霄宇博士。通讯作者为复旦大学附属中山医院介入治疗科王小林教授、中国科学院上海生命科学研究院神经科学研究所仇子龙研究员和复旦大学附属中山医院胰腺外科楼文晖教授。
原文链接:
https://doi.org/10.1016/j.ebiom.2019.02.010
https://doi.org/10.1016/j.ebiom.2019.02.053
制版人:半夏
参考文献
1. L. Rahib, B.D. Smith, R. Aizenberg, A.B. Rosenzweig, J.M. Fleshman, L.M. Matrisian. Projecting cancer incidence and deaths to 2030: the unexpected burden of thyroid, liver, and pancreas cancers in the United States Cancer Res, 74 (2014), pp. 2913-2921.
2. M. Murtaza, S.J. Dawson, D.W. Tsui, D. Gale, T. Forshew, A.M. Piskorz, et al. Non-invasive analysis of acquired resistance to cancer therapy by sequencing of plasma DNA. Nature, 497 (2013), pp. 108-112.
3. M. Meyer, M. Kircher, M.T. Gansauge, H. Li, F. Racimo, S. Mallick, et al. A high-coverage genome sequence from an archaic Denisovan individual.Science, 338 (2012), pp. 222-226
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652468198&idx=2&sn=70a0c2e1f308837f22dd83c6cf8153f0&chksm=84e2e052b395694498c8c996b88d07bd5556d8a6794610f9b32757f25a78ecc8eaa42722db1a&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
癌症 基因组 DNA 胰腺癌 高通量测序 突变理论 dna提取 测序深度 仇子龙
做到这五点,远离胰腺癌
利用Nanopore高通量测序技术解析污水处理体系可移动抗性基因组
Nature 子刊:三代测序的DNA提取和宏基因组学分析

【癌症知多少】胰腺癌术后的那些注意事项
Cell : 张煜博士等破解癌症之王——胰腺癌“长寿”人群的秘密


中国抗癌协会王瑛秘书长出席河北省肿瘤防治宣传周启动仪式




Cell Meta:功能基因组学揭示胰腺癌细胞在不同环境下对代谢的依赖性
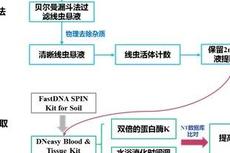
MPB:沈阳生态所李琪组-土壤线虫群落DNA提取、扩增及高通量测序
胰腺癌治疗新希望,抑制胆固醇存储,可延长胰腺癌小鼠模型寿命50%
澳大利亚icon医疗集团访问中国抗癌协会秘书处

