科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-04-08
来源:iNature
基于缺氧的药物(HBA)对固体肿瘤发挥基于缺氧的细胞毒作用。然而,由于临床研究中的效果不令人满意,这些厌氧疗法最终失败了。肿瘤的外周和缺氧核心渗透性较差;因此,可以通过改善肿瘤渗透性来治疗整个肿瘤来优化HBA的渗透。然而,使用抗血管生成剂和其他方法实现的肿瘤通透性增加也与O2的再灌注有关,这进一步削弱了HBA的作用。相反,其他旨在增加肿瘤缺氧的方法,如阻断肿瘤毛细血管,与药物渗透率低有关。因此,最近利用光动力疗法(PDT)消耗肿瘤内氧气并增强肿瘤通透性,以提高HBA的功效;但是,在移除激光后,效果无法保持。因此,仍然迫切需要新的方法来增强HBA的功效。 2019年4月5日,南京大学吴锦慧、胡一桥等在Nature Communications上发表题为“Perfluorocarbonregulates the intratumoural environment to enhance hypoxia-based agent efficacy”的文章,该研究突出了使用全氟化碳建立持久,低氧和可渗透的肿瘤微环境的厌氧疗法的前景。

PFTBA用IR780(近红外(NIR)光敏剂)负载的人血清白蛋白(HSA)进行超声乳化以形成PNP。 还通过用水或橄榄油代替PFTBA作为对照来制备IR780纳米颗粒(NP)和油纳米颗粒(ONP)。 使用透射电子显微镜可以清楚地将PNP的结构可视化为均匀的球状结构。 通过动态光散射(DLS),平均PNP直径确定为160nm,并且该值在储存7天后没有变化,表明长期稳定性。PNP中IR780的数量也由紫外 - 可见(UV-vis)吸收光谱确定。
全氟化碳,如PFTBA,都具有比水更强的吸氧能力,这可以提高周围光敏剂的光动力效率。考虑到肿瘤可以持续从循环中接收氧气,持续的氧气消耗对于抑制肿瘤中氧分压的恢复非常重要。PFTBA可以吸收更高水平的溶解氧(DO),因此可以实现这一目标。为了验证PNP是否可以作为这样的氧气纳米海绵,研究人员将脱氧的PNP添加到水中以模拟氧气吸收过程。 发现PNP溶液中的显着Δ[O2](-41.7μM),但ONP和NP溶液中仅有轻微的Δ[O2](<-12μM)。在吸收氧气后,用808nm激光照射PNP以实现氧吸收和消耗。 PNP组的Δ[O2]值进一步降低,PNP组的下降幅度远大于对照组(PNP为-160μM,ONP为-90μM,NP为-40μM)。这些结果表明PNP吸收和消耗氧气。研究人员进一步评估上述光/暗循环是否可以反复增强缺氧。 与ONP组相比,PNP组的O2减少更有效。 在四个循环后,PNP仍然可以有效地摄取和消耗O2。这些观察结果表明,PNP具有可持续和可重复的氧气吸收和消耗能力。
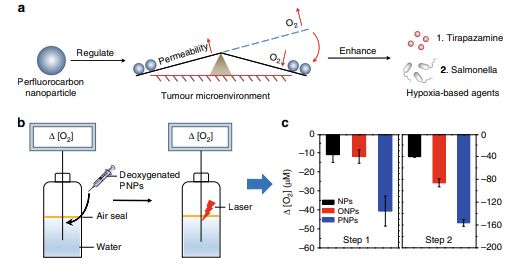
PNP介导的改善HBAs和O2吸收及消耗的原理图
基于缺氧的药剂(HBA),例如厌氧细菌和生物还原性前药,需要渗透性和缺氧的肿瘤内环境才能完全有效。为了解决这个问题,研究人员在该研究中报道,全氟化碳纳米颗粒(PNP)可用于创建持久,可穿透和缺氧的肿瘤微环境,以确保随后施用的HBA的递送和活化。除了由PNP引起的增加的渗透性和增强的缺氧之外,可以保留PNP以进一步实现肿瘤内O2再灌注的长期抑制,同时增强HBA积累超过24小时。因此,全氟化碳材料可能具有重新启动基于缺氧的药物的临床研究的巨大潜力。

原文链接:
https://www.nature.com/articles/s41422-019-0164-5
来源:Plant_ihuman iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247500170&idx=7&sn=956dcb5863a605b052cf81bf89ea69b0&chksm=fce6b255cb913b43fb3f9322fb8f5166dc88e2b29f5ecf2528c7bf6190ee5234d4e483779d82&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
导电材料强化厌氧消化机理研究中获进展

中年人要担心的不只是油腻,45岁起就该开始结直肠癌筛查
湿地甲烷厌氧氧化机制研究进展
厌氧性细菌
研究发现具有乙烷厌氧功能的古菌及其代谢途径

发光纳米颗粒可以更快更精准地检测癌症
独特的厌氧性动物:不呼吸氧气就能生存
厌氧消化
中国抗癌协会肿瘤护理专业委员会在津成立



厌氧的