科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-07-23
来源:BioArt
肠道菌群是一个具有高度复杂性和多样性的生态系统,在人的胃肠道中,大约栖居着百万亿个细菌。随着人们对肠道菌群的深入了解,其在正常生理过程以及疾病进展中所扮演的重要角色逐渐被认知。
结直肠肿瘤是最常见的肿瘤类型之一,2018年全球新发病人数达到近200万,而死亡人数将近90万人。根据研究表明,肠道菌群中的某些特定细菌在结直肠肿瘤的进展与治疗中均起到了至关重要的作用。例如,具核梭杆菌 (Fusobacterium nucleatem) 会促使肿瘤细胞发生保护性自噬,导致肿瘤细胞产生对化疗药物的耐受性。而诸如梭菌属,真杆菌属等细菌则可以通过发酵产生短链脂肪酸,从而抑制结直肠肿瘤的生长。基于这些发现,如何调控肠道菌群,进而为肿瘤化疗提供一个最有利的微生态环境显得尤为重要。
2019年7月22日,武汉大学化学与分子科学学院张先正教授研究团队(共同第一作者为博士研究生郑迪威和董雪)在Nature Biomedical Engineering期刊上发表研究论文Phage-guided modulation of the gut microbiota of mouse models of colorectal cancer augments their responses to chemotherapy,报道了一种基于噬菌体介导的靶向性纳米药物,成功用于调控肠道菌群并有效提升肿瘤化疗效果。
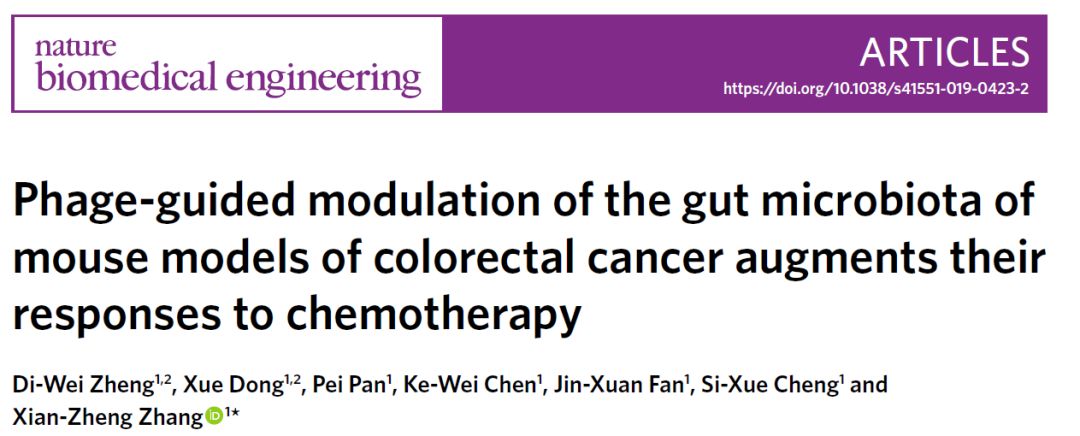
他们首先利用一株可以特异性抑制具核梭杆菌生长的温和噬菌体,并通过生物正交化学方法将该噬菌体叠氮化(A-phage)。随后,进一步合成了负载有化疗药物伊立替康的葡聚糖纳米粒子(IDNP),然后将IDNP与二苯基环辛炔 (DBCO) 共价连接制得D-IDNPs。通过无铜点击化学反应,叠氮化的噬菌体与D-IDNPs可在生理环境下共价连接形成噬菌体介导的纳米药物 (A-phage-D-IDNPs) 。动物实验证明,噬菌体可以特异性地富集在定植有具核梭杆菌的肿瘤中,并进一步介导纳米药物在肿瘤组织中的富集。通过抑制具核梭杆菌的增殖,可以有效抑制结直肠肿瘤对化疗的耐受效果。同时,D-IDNP中的葡聚糖可为特定肠道细菌发酵提供能量来源,从而提升肠道内丁酸等短链脂肪酸含量。在随后的小鼠肿瘤治疗实验中,研究人员发现这一方法可以显著地抑制瘤内具核梭杆菌的生长,同时促进内源性产丁酸菌的增殖。在小鼠原位结直肠肿瘤模型以及小鼠自发结直肠肿瘤模型上,均显著提高了结直肠肿瘤的化疗效果。该研究综合利用了生物学、化学和材料学方法,通过调控肠道菌群,从而实现提高疾病治疗的目标。
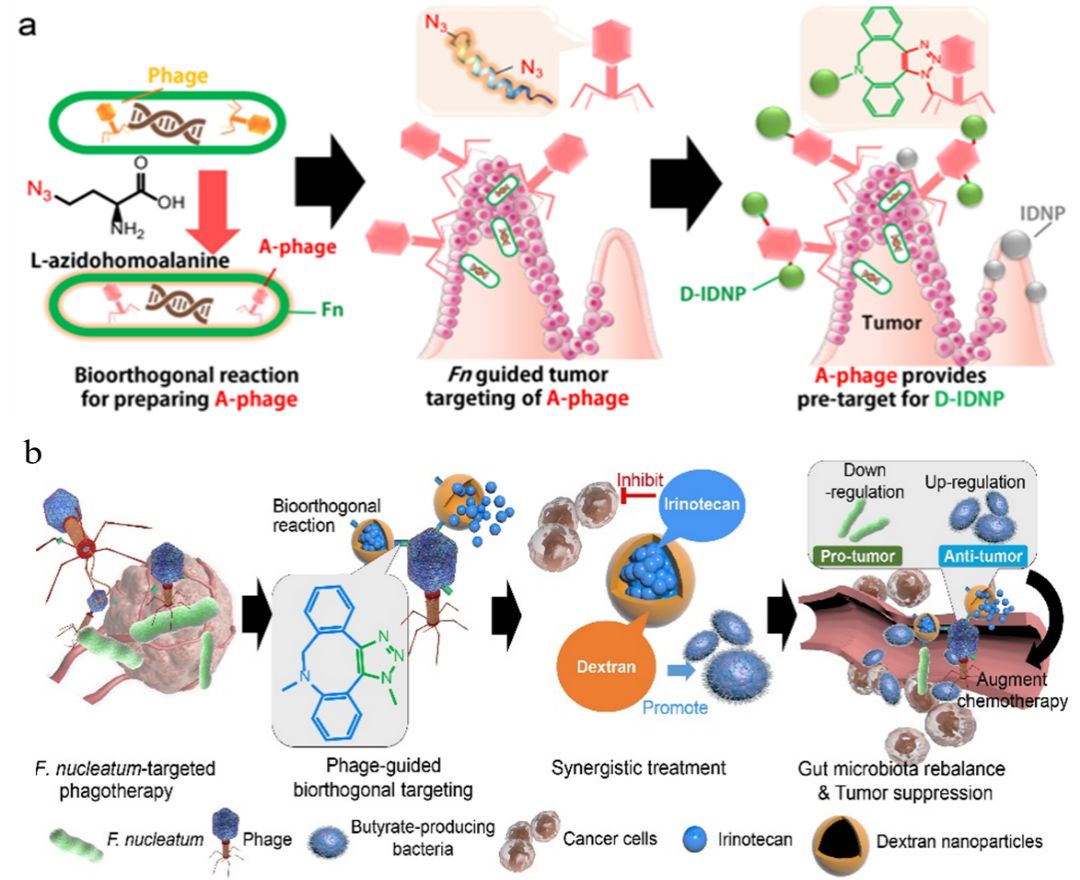
肠道菌群调控性纳米药物的抗肿瘤治疗
原文链接:
https://doi.org/10.1038/s41551-019-0423-2
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652472954&idx=6&sn=f71fe308041870024270ef10465f887e&chksm=84e215ceb3959cd8e28fc2c687c3bd8f09789eced6181f4b3e7111acdcfc52b6456b78d5b851&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

中国微米纳米技术学会第十八届学术年会暨微系统与纳米工程高层论坛
中国抗癌协会肿瘤介入学专业委员会换届会议召开



综述 | 膜-核纳米粒子用于纳米医学和中草药对肿瘤微环境的影响
抗癌抗菌的混合纳米粒子问世
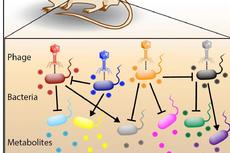
Cell子刊:噬菌体对肠道菌群和代谢组的调控

纳米粒子助力CRISPR,三阴性乳腺癌小鼠肿瘤生长减缓77%
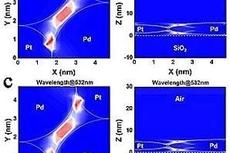
纳米粒子自组装制备2D准纳米片

【走近桂籍科学家】用纳米武装电池新世界
第一届纳米纤维素材料国际研讨会在杭州召开



中国—奥地利纳米科技及新材料研讨和对接洽谈会在深圳举行


