科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-08-14
来源:BioArt
多种类型的成人和小儿肿瘤中会发生neurotrophin receptor tyrosine kinase NTRK基因(NTRK1 NTRK2 NTRK3,编码蛋白neurotrophin receptors TRKA TRKB TRKC)融合。基因融合是肿瘤中TRK激酶过度激活的主要机制。在染色体内或者染色体之间的基因重排(rearrange)导致NTRK基因的3`端的激酶结构域与另外一个基因的5`端基因发生融合。融合基因编码的嵌合蛋白的一个主要的特点是具有不依赖于配体的持续激活的TRK激酶活性。多数TRK融合蛋白的伴侣蛋白(partner)含有寡聚化结构域,包括锌指结构域,WD结构域和盘曲结构域。融合蛋白通过寡聚化结构域形成二聚体,从而激活TRK激酶结构域。TRK激酶激活下游MAKP、PI3K和PKC信号通路,促进肿瘤细胞增殖转移以及侵袭【1】。
第一代针对TRK的抑制剂larotrectinib和entrectinib对75%的TRK融合蛋白阳性的肿瘤有效。第一代TRK抑制的患者耐受性也较好,偶尔会出现TRK抑制剂作用于非肿瘤组织出现的副作用。然而高恶性程度的TRK融合蛋白阳性的肿瘤会对第一代抑制剂产生耐药性。产生耐药性最主要的机制被称为靶点耐药(on-target)。靶点耐药主要是由于TRK激酶结构域产生突变。针对特定位点突变的第二代TRK抑制剂LOXO-195和TPX-0005也进入了临床试验。
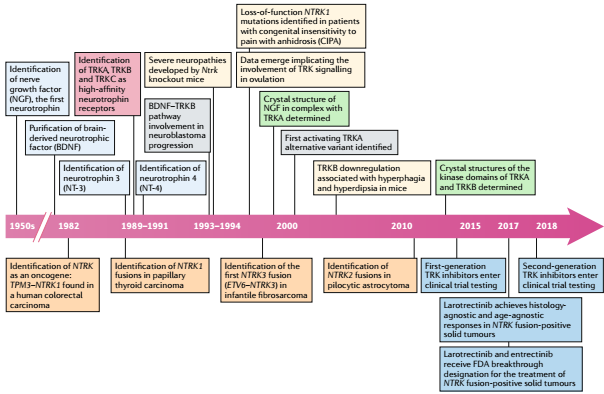
2019年8月12日,来自Memorial Sloan Kettering Cancer Center的Alexander Drilon 和Maurizio Scaltriti课题组在Nature Medicine上发表了题为Resistance to TRK inhibition mediated by convergent MAPK pathwayactivation的文章,指出TRK抑制剂的非靶点耐药(off-target)机制:基因组改变激活MAPK信号通路。联合TRK抑制剂和MEK抑制剂能够延迟肿瘤进展。

为了探索TRK抑制剂耐药的机制,作者收集了临床试验中各种类型的TRK抑制剂治疗以及对照患者的肿瘤样本和循环游离DNA。配对测序筛选出的不存在TRK激酶结构域突变和不能因为突变完全解释TRK抑制剂耐药的病例作为进一步研究的对象。作者在三对配对耐药样本中发现了MAPK信号的上游和下游会产生明显的变化,后续作者拿这三对配对病人样本作更深层次的分析。
第一个病人是发生CTRC-NTRK1基因融合并对larotrectinib耐药的胰腺癌患者。利用cfDNA测序以及(Patient derived xenografts)PDXs的方法发现患者具有BRAFV600E和KRASG12D突变。用二代抑制剂LOXO-195处理样本则会迅速产生疾病进展。这也进一步表明MAPK信号激活是TRK抑制剂非TRRK依赖耐药的机制。
第二个病人是有LMNA-NTRK1基因融合并且对LOXO-195耐药的结肠癌患者。作者发现此患者存在多位点的KRAS突变。这个患者以前给予长期的larotrectinib治疗后产生了NTRK1G595R突变而产生耐药。产生一代抑制剂耐药后给予LOXO-195治疗,最终产生肝转移。肝转移的样本中出现了KRASG12A的突变,切除肝转移后继续使用LOXO-195治疗,但是出现了KRASG12D的新的突变。为了模拟这一变化,在TRK融合蛋白阳性的结肠癌细胞系中异位表达KRASG12A和 KRASG12D发现,这两个突变能够促进MAPK信号的激活以及对larotrectinib 和LOXO-195耐药。
第三个病人是PLEKHA6-NTRK1基因融合并对一代TRK抑制剂entrectinib耐药的胆管癌患者。病人组织以及cfDNA都能够检测出MET基因扩增。FISH和IHC检测发现MET表达上升。但是NTRK1不存在突变。尽管之后给予LOXO195,患者依旧迅速出现疾病进展。
由于这三个病人都是消化道起源的肿瘤,作者检测了所有具有TRK融合的消化道样本发现了另外五例MAKP过度激活的病人样本。这些结果说明TRK抑制剂一代二代都耐药的患者存在MAPK信号通过上游激酶以及下游信号激活而保留活性。所以接下来作者利用联合治疗的方法来验证结论。
首先对第一位病人的PDXs模型用TRK抑制剂和RAF与MEK抑制剂(dabrafenib和trametinib)联合治疗发现会很快抑制肿瘤【2】,并且减少肿瘤中NTRK的融合以及BRAFV600E的突变。第三位胆管癌患者的在LOXO-195的基础上给予MET抑制剂crizotinib,能够在8周时缩小肿瘤并且维持疾病控制4.5月。检测发现联合治疗后NTRK融合以及MET扩增都无法检测到。这些试验表明TRK和MEK双重抑制或许能够推迟治疗产生的非靶点耐药的产生。为了验证这一假设,作者进一步建立了larotrectinib耐药的PDXs模型。之后给予TRK抑制larotrectini、MEK抑制剂btrametinib或者同时给予两种药物。结果发现联合治疗能够限制耐药细胞的群体的扩增。
综上,作者发现了集中于激活MAPK信号的一种TRK抑制剂的非靶点耐药机制,联合TRK和MEK抑制剂治疗能够对付一部分耐药机制,但二者的应用会产生不重叠的毒副作用,更多的研究需要致力于此。
原文链接:
https://doi.org/10.1038/s41591-019-0542-z
参考文献
1. CoccoE, Scaltriti M, Drilon A. NTRK fusion-positive cancers and TRK inhibitortherapy. Nature reviews Clinical oncology. 2018;15:731-47.
2. Caunt CJ, Sale MJ, SmithPD, Cook SJ. MEK1 and MEK2 inhibitors and cancer therapy: the long and windingroad. Nature reviews Cancer. 2015;15:577-92.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652473871&idx=4&sn=55d7e4ab1f1bad43a0cc3eff1cdb1c07&chksm=84e219bbb39590ad7b1395bd0150e02c2c42f9b277ec8431cdaa7a138c7edf24b7bffc17e7e5&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
从单个细胞入手的肿瘤研究
胸腔积液肿瘤细胞学检查

CGCS2021 | 向阳教授领衔,共谈妊娠滋养细胞肿瘤诊治规范——妊娠滋养细胞肿瘤专场

用CRISPR/Cas9在小鼠体内选择性消除肿瘤细胞而不影响健康细胞
胸腔积液肿瘤细胞学检查
肿瘤竟把免疫细胞关进“小黑屋”


Nat Commun:健康细胞或会在胚胎发育期间影响肿瘤的进展
肿瘤干细胞的分离与鉴定


Nat Commun:中性粒细胞或会促进肿瘤细胞死亡

新疗法有助免疫细胞从血管中进入肿瘤 系统根除脑肿瘤