科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-10-06
来源:BioArt
当免疫细胞通过血液和淋巴循环系统,进入体内不同器官和组织间并发挥功能时,它们被周围不同的机械力因素所调控,这种机械力调控免疫细胞功能的过程是一个非常值得研究和探索的领域。研究和探索免疫细胞如何感知、应答和适应这些生物力对深入理解免疫应答机制乃至优化免疫治疗放案具有非常重要的意义。
2019年9月18日,力学免疫学领域的国际权威专家,佐治亚理工大学的Cheng Zhu教授受邀,并与浙江大学医学院的陈伟教授、中国科学院生物物理所的娄继忠研究员合作,在Nature Immunology杂志在线发表了重要观点文章“Mechanosensing through immunoreceptors ”。该观点文章既是一个对这一领域研究工作回顾和总结,也是对该领域我来有研究前景和研究价值的方向进行了展望【1】。

淋巴细胞识别“外来”或“自身异常”的抗原是启动抗感染或癌症等适应性免疫反应的一个关键过程。每个免疫细胞的功能都是由不同免疫受体的共刺激信号决定的,而免疫受体的表达和激活受细胞的发育阶段和外环境的调控(图1)。
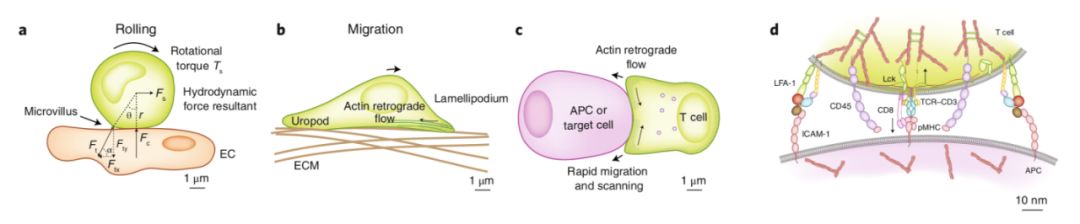 图1 免疫细胞表面分子与环境相互作用示意图。a.淋巴细胞在内皮细胞表面滚动所受到的外力。b,c.在细胞迁移(b)和免疫突触形成过程中(c)肌动球蛋白收缩和肌动蛋白回缩运动所产生的内生力。d. 在免疫突触上的中心,TCR和CD8与抗原呈递细胞上的pMHC相互作用产生拉力以平衡周围的大分子CD45因挤压带来的斥力。在免疫突触上的还有LFA-1和ICAM-1相互结合所产生的生物力。
图1 免疫细胞表面分子与环境相互作用示意图。a.淋巴细胞在内皮细胞表面滚动所受到的外力。b,c.在细胞迁移(b)和免疫突触形成过程中(c)肌动球蛋白收缩和肌动蛋白回缩运动所产生的内生力。d. 在免疫突触上的中心,TCR和CD8与抗原呈递细胞上的pMHC相互作用产生拉力以平衡周围的大分子CD45因挤压带来的斥力。在免疫突触上的还有LFA-1和ICAM-1相互结合所产生的生物力。
最新的研究强调了几种免疫受体-配体互作过程中机械力的存在,以及这些机械力在调控细胞间相互作用和行使功能中的重要作用。作者们认为这些研究为力学免疫学奠定了基础。在本观点综述文章中,作者们以T细胞受体(T cellreceptor,TCR)识别抗原(peptide-majorhistocompatibilitycomplex, pMHC)为例(图2)【2-4】,回顾了目前该领域对免疫受体感受机械力特性的认识。
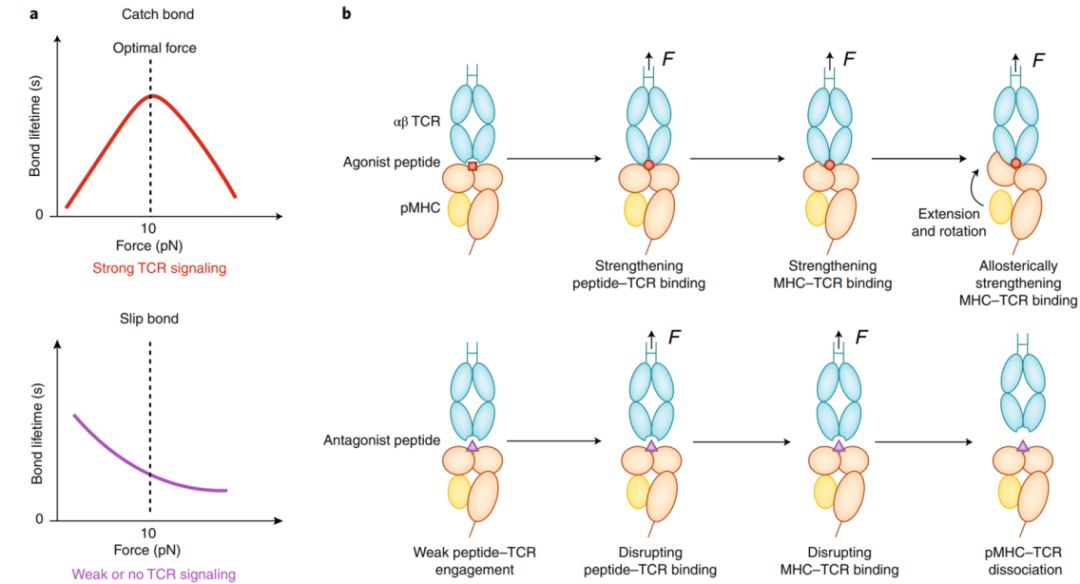
图2 TCR-MHC的动态键[逆锁键(上)和滑移键(下)]由pMHC构象决定并受力调节。a.当TCR与pMHC形成逆锁键时,在低力情况增加力会延长它们相互作用的时间,在高力情况下增加力会缩短时间(上)。当TCR和pMHC形成滑移键时,增加力只会单纯减少它们的相互作用时间(下)。b.当TCR和激活型抗原结合时,力会通过改变pMHC构象(延长或者旋转)来增强TCR和抗原表位的结合,故形成逆锁键(上)。当TCR和非激活型抗原结合时,力无法促使pMHC产生构象变化,只会促进二者的解离,故形成滑移键(下)。(改编自【2】)
文章探索了免疫受体可能会遇到机械力的类型(图3),机械力在受体-配体结合、构象变化和免疫受体触发中的作用以及机械力在下游信号转导、细胞命运决定和免疫细胞效应器功能中的作用。
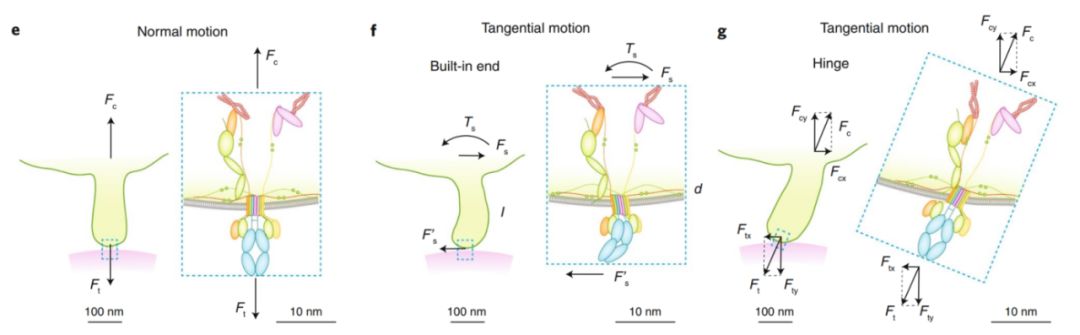
图3 当外力作用方向不同时T细胞受体可能的受力情况。e.在施加外力的力探针沿T细胞表面法向运动的情况下,T细胞微绒毛(左)及TCR(右)都只受到沿长轴方向的拉力Ft。f,g.当施加外力的力探针沿T细胞表面切向运动时,T细胞微绒毛(左)及TCR(右)的受力情况取决于其根部是如何锚定的。假设微绒毛及TCR能够承受弯矩并按悬臂梁的方式来锚定,则跟T细胞表面平行的切向力会在微绒毛及TCR的内部产生切向力及弯矩(f)。如果微绒毛及TCR不能承受转矩或按铰链的方式来锚定,那么它们将随力的方向倾斜传递沿轴向的力(g)。
该综述文章同时强调了新的生物物理工具(例如,单分子力检测技术等)和先进的成像技术在力学免疫学研究中的作用(图4),指出这些研究工具可以帮助更好的理解生物力在免疫细胞及其功能行使中的调控作用。显然,这些新见解将对于更加深入地研究机械力介导的免疫细胞受体调控机制以及应用转化(包括抗肿瘤疫苗和更加有效的细胞疗法)的发展奠定了基础。
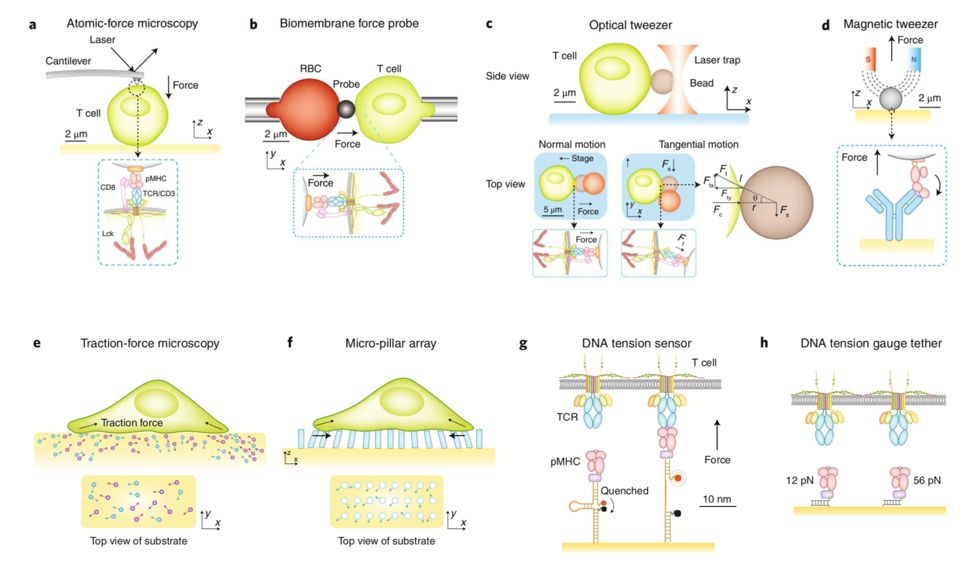
图4 生物力学检测技术示意图。a.原子力显微镜。b.生物膜力学探针。c.光镊。d.磁镊。e.牵引力显微镜(TMF)通过测量柔性基质中的微球位移来测量细胞铺展及迁移过程中产生的力。f.微柱阵列(mPAD)通过测量微柱的弯曲程度来测量细胞铺展及迁移过程中产生的力。g.分子力探针将力信号转换成荧光强度,以此测量受体所受到的力。h.DNA张力计采用一个设计阈值,当超过阈值时DNA的双链会发生断裂分开,以此来限制对受体施加的张力值。
另一方面,由于目前对抗肿瘤的CAR-T细胞(嵌合抗原受体T细胞)的触发机制尚不完全清楚,导致了CAR-T细胞很难达到理想的效果。对于机械免疫学的进一步研究和了解,对未来训练免疫系统防卫癌症的发生和下一代CAR-T疗法的设计有着重要的指导作用,这对于人类对抗肿瘤、拯救生命而言具有深远的意义。
参考文献
1. Zhu, C., Chen, W., Lou,J., Rittase, W. & Li, K. Mechanosensing through immunoreceptors. Nat.Immunol. 20(10):126, (2019).
2. Wu, P. et al. Mechano-regulation of Peptide-MHCClass I Conformations Determines TCR Antigen Recognition. Mol. Cell 73,1015-1027.e7 (2019).
3. Liu, B., Chen, W., Evavold, B. D. & Zhu, C.Accumulation of dynamic catch bonds between TCR and agonist peptide-MHCtriggers T cell signaling. Cell 157, 357–368 (2014).
4. Hong, J. et al. A TCR mechanotransduction signalingloop induces negative selection in the thymus. Nat. Immunol. 19,1379–1390 (2018).
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652476044&idx=4&sn=d090370c9240c3587eb5945489bcc907&chksm=84e20138b395882e5331baebdf1c30a8fa1030ae67bdba2ad695b33d9604159afdf54630166b&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
免疫治疗,肿瘤患者治愈的希望!
“多尺度大陆地球动力学国际研讨会”在武汉召开

力学•创新•追梦•未来

肿瘤免疫治疗丨调节性T细胞及其应用

第十一届“中国青年女科学家奖”获奖者段慧玲的报导
肿瘤营养不良患者细胞免疫治疗

Immunity:肿瘤免疫治疗的十大挑战

Nature Immunology综述 | 肿瘤免疫治疗抵抗的机制

肿瘤免疫治疗标志物的进展与思考

用葡萄酒成分调控肿瘤免疫治疗