科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-17
Combes喹啉合成是伯芳胺与β-二酮在酸催化下缩合为亚胺,然后闭环,生成喹啉的衍生物。
在形成环时,当中间体(缩苯胺)的氮原子的间位有强的邻,对位定向取代基存在时,有利于闭环反应的发生;同时当有强邻、对位定向取代基存在于氮原子的对位时,则会阻碍闭环作用。
简介Combes喹啉合成
芳香胺类与β-二酮缩合得到2,4-二取代喹啉。R通常为烷基,Rˊ可以是烷基或芳基,或取代芳基。在缩苯胺的氮原子的间位有强的邻,对位定向取代基存在时,则闭环反应容易发生;但强邻、对位定向取代基存在于氮原子的对位时,则阻碍闭环作用。
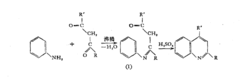
这个反应通过中间体缩苯胺(Ⅰ),此环化作用不能只靠加热来完成,必须与浓硫酸共同温热才能环化。
近年来发现当β-氯乙烯醛和一级芳香胺的溶液在室温容易形成亚胺-烯胺盐酸盐,并且为一般反应,很少有不能形成亚胺-烯胺盐酸盐的例子。3-氯-2-甲酰基丁烯-2-酸甲酯和苯胺,间硝基苯胺和3-氯-2-甲基丁烯-2-醛反应分别得到(Ⅱ)和(Ⅲ)。
PhNHC(Me)═C(CO2Me)—CHO(Ⅱ),m—O2N—C6H4NH—C(Me)═C(Me)—CHO(Ⅲ)
(Ⅲ)不能和另一分子胺进行反应,可能由于间硝基苯胺的低亲核性,关于(Ⅱ)不能和第二个分子苯胺反应还无解释。
当亚胺-烯胺盐酸盐在乙酸或类似沸点的醇(如正丁醇)中回流加热时,得到喹啉,产率良好Ⅲ。
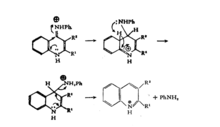
这个反应和经典的由β-二酮与一级芳香胺缩合制备喹啉的贡贝斯方法极类似。1
反应机理苯胺和β-二酮在浓硫酸共同温热的条件下发生环化,得到2,4-二取代喹啉。
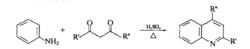
该反应机理如下:
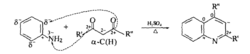
—NH2是邻对位取代基,带正电基团定位于邻对位,但对位的可能性很小。2
应用Combes反应是合成喹啉及其衍生物重要的方法,它是用苯胺(或其衍生物)与无水甘油、浓硫酸及适当的氧化剂一起加热反应而得。Combes反应只有当反应进行激烈时,才能得到较好的产量,但如果反应猛烈,有时较难控制,为避免反应过于剧烈,常加入少量硫酸亚铁或硼酸缓和反应。浓硫酸是脱水剂,也可用磷酸代替。氧化剂常用硝基苯,也可用碘、五氧化二砷、氧化铁等,但不能用强氧化剂。甘油含水多,产率会降低。如用碘做氧化剂,甘油不必无水。
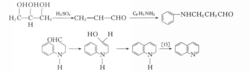
喹啉及其衍生物的生成过程,可能是由浓硫酸首先使甘油脱水成丙烯醛,苯胺与丙烯醛发生1,4-共轭加成,产生β-苯氨基丙醛,再在酸催化下脱水环化,形成1,2-二氢喹啉,在氧化剂的作用下,1,2-二氢喹啉氧化脱氢得到产物,此反应实际上是一步完成,产率很高。其反应过程如下:3
本词条内容贡献者为:
王宁 - 副教授 - 西南大学