科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-19
来源:精准医学与蛋白组学
题目:Proteogenomic Landscape of Breast Cancer Tumorigenesis and Targeted Therapy
发表时间:2020年11月18日
期刊:Cell
影响因子:38.637
作者及单位:麻省理工学院和哈佛大学的Michael A. Gillette,Steven A. Carr,D.R. Mani和贝勒医学院的Matthew J. Ellis等研究团队
主要结论:揭示了迄今为止最大的乳腺癌大队列样本的蛋白基因组特征,并首次分析了乳腺癌乙酰化修饰信号,提出肿瘤发生、诊断标准和治疗靶标等多方面建议。
关键词:异质性;多组学;NMF亚型;免疫调控
乳腺癌 (Breast Cancer, BRCA) 是女性癌症相关死亡的首要原因,现阶段的精准治疗方法主要是通过联合靶向多种细胞通路如DNA修复缺陷、活化蛋白激酶、雌激素受体 (ER) 和免疫肿瘤微环境等。但是这些方法的有效应用取决于我们对肿瘤进行精准分析以识别个体化特征,然而,乳腺癌的异质性给患者个性化治疗带来了很大的挑战。
蛋白表达水平和信号通路的异常是肿瘤最常见的特征。近些年来的研究表明,相比于仅通过基因组分析,蛋白组和修饰组研究包含了更多基因无法识别的新信息,整合基因、转录、蛋白和修饰的多组学数据的蛋白基因组分析能够更全面的认识肿瘤,也为肿瘤未来的精准治疗提供新的思路和方向。
2020年11月18日,来自麻省理工学院和哈佛大学的Michael A. Gillette,Steven A. Carr,D.R. Mani和贝勒医学院的Matthew J. Ellis等研究团队在Cell上发表了最新研究成果。研究采用基于质谱的蛋白质组学、磷酸化/乙酰化修饰组学结合DNA、RNA测序,对122例原发性乳腺癌展开研究,揭示了迄今为止最大的乳腺癌大队列样本的蛋白基因组特征,并首次分析了乳腺癌乙酰化修饰信号,提出肿瘤发生、诊断标准和治疗靶标等多方面建议。
值得一提的是,继7月Cell主刊肺腺癌多修饰组学研究(Cell亮点:Steven Carr团队报道大规模肺腺癌蛋白基因组学研究)后,Steven A. Carr团队再次在大规模肿瘤样本研究中对磷酸化和乙酰化crosstalk进行了细致观测。这引起我们对于肿瘤大样本中其他酰化修饰的密切关注,比如琥珀酰化、巴豆酰化等,为未来相关的研究工作提供指导意义。

1、乳腺癌蛋白基因组整体研究
首先,研究者收集了122例未经治疗的原发性乳腺癌临床样本(样本策略),并针对其展开TMT标记的蛋白组、磷酸化修饰组、乙酰化修饰组和DNA、RNA水平的测序研究(质谱策略),共鉴定到29,647个体细胞突变、23,692个基因水平的copy number改变、23,121个转录本、10,107个蛋白、38,968个磷酸化位点和9,869个乙酰化位点。整合多组学数据,可以将乳腺癌分为四种NMF (Non-negative matrix factorization) 亚型,每种亚型富集不同的信号特征,其中luminal A-inclusive (NMF LumA-I) 和 basal-inclusive (NMF Basal-I) 与PAM50分型基本一致。进一步通过磷酸化修饰组学数据分析发现,不同NMF亚型富集特异性的蛋白激酶,可作为每种亚型潜在的治疗靶标。
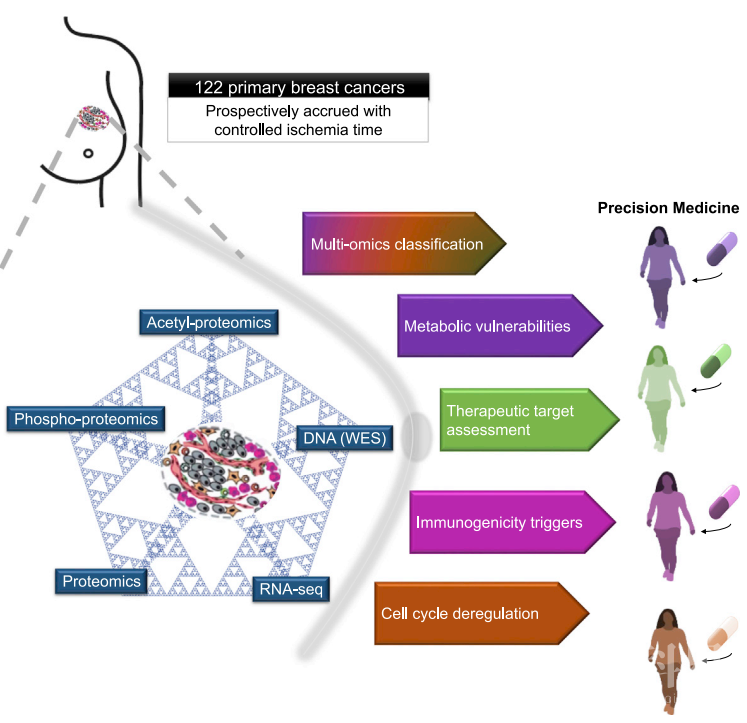
图1 原发性乳腺癌蛋白基因组研究
2、蛋白组和乙酰化修饰组学解析乳腺癌亚型的代谢特征
肿瘤细胞的代谢异常是近些年关注的热点。接下来,研究者通过蛋白组学分析了代谢相关蛋白的表达并将乳腺癌样本分为4个亚型,这4个亚型与NMF亚型密切相关。Cluster 1代表NMF Basal-I,上调DNA延伸、翻译、碳水化合物代谢等蛋白,下调胆固醇合成、氨基酸/维生素代谢等蛋白;clusters 2、3分别与NMF LumA-I and NMF LumB-I一致,相较于cluster 1的代谢特征逆向分布;cluster 4代表NMF HER2-I肿瘤亚型,上调胆固醇合成和脂代谢相关蛋白。
之前的研究表明,蛋白乙酰化修饰与代谢密切相关。进一步整合乙酰化修饰组数据与NMF亚型分析发现,NMF Basal-I亚型中TCA循环和β氧化相关蛋白乙酰化水平上调,NMF LumB-I亚型中葡萄糖代谢和IL-1信号相关蛋白乙酰化修饰水平上调。同时,研究者还发现不同乳腺癌亚型的细胞组分如胞质、线粒体、细胞核以及代谢通路如糖酵解、丝氨酸代谢等乙酰化修饰的调控也存在很大差异。
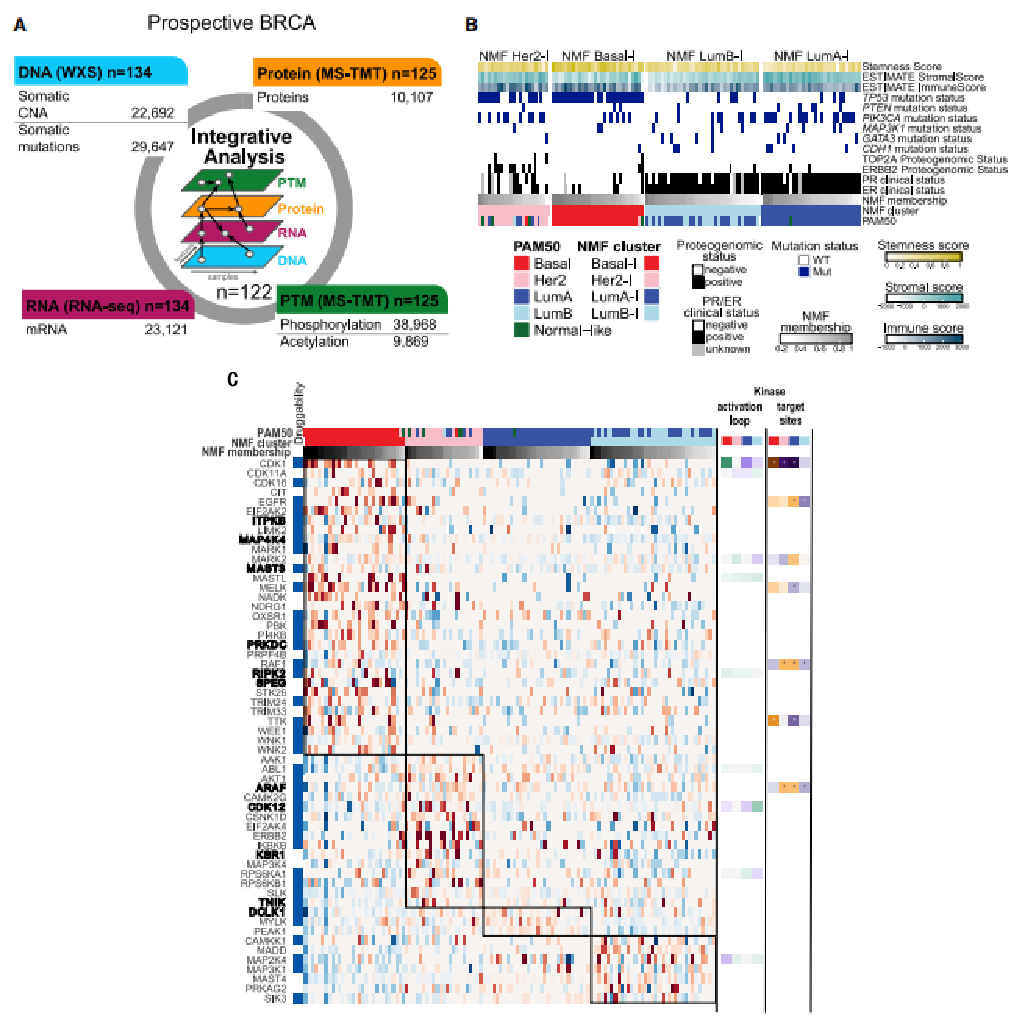
图2 乳腺癌亚型的代谢以及乙酰化修饰特征
3、蛋白基因组学揭示ERBB2和RB状态与临床相关性
之后的研究显示,乳腺癌一些关键蛋白的表达与其进程密切相关,如编码一类表皮生长因子受体家族的ERBB以及参与肿瘤细胞周期进程的Rb等。研究者发现有些ERBB基因扩增的乳腺癌样本表现出特异性药物治疗抵抗,而这部分样本ERBB蛋白表达水平很低。蛋白基因组学能对ERBB的状态进行很好的分型,在ERBB没有扩增的情况下通过靶向ERBB信号通路的潜在driver能起到治疗作用。除此之外,基于蛋白基因组学的Rb表达和修饰状态分析为临床CDK4/6抑制剂的使用提供了指导。
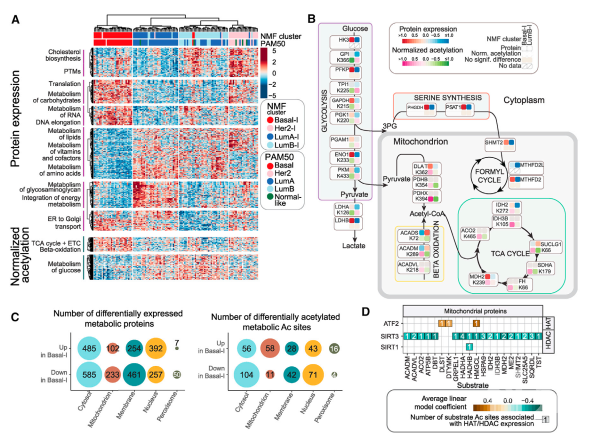
图3 蛋白基因组学揭示ERBB2和RB状态与临床相关性
4、蛋白基因组学分析提示luminal亚型乳腺癌的潜在免疫治疗
免疫信号调控是肿瘤细胞的重要特征,研究者接下来针对乳腺癌样本的整体免疫分布和亚型特征展开分析。基于RNA和蛋白水平的免疫调控因子分析揭示了四种亚型之间存在广泛的免疫信号特征,包括免疫检查点蛋白PD1、PDL1在RNA和磷酸化修饰水平的调控等。PAM50分型的LumB而非LumA亚型中具有获得性免疫应答活化特征,同时研究结果显示绝大部分LumB亚型的肿瘤表现出免疫微环境活化和免疫检查点蛋白、STAT1 / IFNG基因的过表达,提示针对免疫肿瘤微环境活化的luminal亚型肿瘤可以开展免疫治疗。
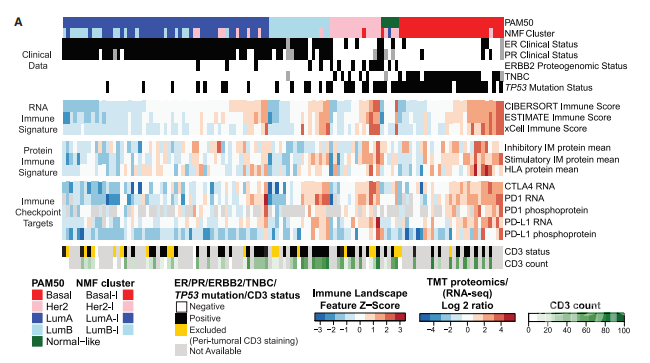
图4 蛋白基因组学分析提示luminal亚型乳腺癌的潜在免疫治疗
小结与展望
乳腺癌的异质性给患者个性化治疗带来了很大的挑战,因此针对乳腺癌临床样本的研究对于其精准分型以及临床治疗具有重要意义。本篇研究利用基于质谱的蛋白质组学、磷酸化/乙酰化修饰组学结合DNA、RNA测序对122例原发性乳腺癌展开研究,提供了对ERBB2扩增的详细分析,明确可以通过免疫检查点治疗的肿瘤亚群,更准确的评估Rb状态以预测CDK4 / 6抑制剂的应答效果。同时,磷酸化修饰组学分析发现了肿瘤抑制因子缺失与靶向激酶之间新的关联;乙酰化修饰组分析揭示了与DNA损伤应答相关核蛋白乙酰化的关键作用以及胞质和线粒体乙酰化代谢等相互调控。综上,本篇研究不仅突出了蛋白基因组学在乳腺癌研究中的重要价值,更为未来相关的临床研究工作提供指导意义。
来源:ptm-biolab 精准医学与蛋白组学
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5NDM5NjQxOA==&mid=2650453785&idx=1&sn=0b987a21c40fa1520eee48b241f46a5d
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

乳腺癌有望实现精准治疗,科学家揭开基因组秘密
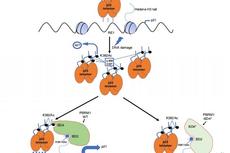
Nat Comm | p53蛋白乙酰化新的重要调控机制

AREB1通过调节组蛋白乙酰化介导杨树干旱响应

Cell | 跨代传递的组蛋白H4K16乙酰化决定未来基因激活

【防癌早知道】乳腺癌系列-肥胖与乳腺癌有何关系?

一种氨基酸水平影响乳腺癌扩散

战胜柯洁后,DeepMind试图用人工智能战胜乳腺癌

【前沿】MIT新开发的 AI 模型有望改进恶性脑瘤治疗
Mol Cell:新研究揭示组蛋白巴豆酰化/乙酰化修饰拮抗调控代谢稳态与基因表达

PNAS: 乙酰化 cGAS 提高机体对 DNA 病毒的抵抗能力