科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-02-24
来源:iNature
与RNA结合蛋白(RBP)的相互作用是RNA功能和细胞调节不可或缺的,并动态反映特定的细胞状况。但是,目前用于预测RBP-RNA相互作用的工具使用RNA序列和/或预测的RNA结构,因此无法捕获其条件依赖性。
2021年2月23日,清华大学张强锋团队在Cell Research 在线发表题为“Predicting dynamic cellular protein–RNA interactions by deep learning using in vivo RNA structures”的研究论文,该研究分析了七种细胞类型的转录组范围内的体内RNA二级结构后,开发了PrismNet,这是一种深度学习工具,它集成了实验的体内RNA结构数据和匹配细胞的RBP结合数据,以准确预测各种细胞条件下的动态RBP结合。
168个RBP的PrismNet结果支持其实用性,既可用于了解CLIP-seq结果,又可广泛扩展此类相互作用数据以准确分析其他细胞类型。此外,PrismNet采用“注意”策略以计算方式识别确切的RBP结合核苷酸,并且该研究发现了动态RBP结合位点之间的富集,这可以将遗传疾病与失调的RBP结合联系起来。该研究丰富的分析数据和基于深度学习的预测工具提供了对以前无法访问的细胞类型特异性RBP-RNA相互作用层的访问,并且对于理解和治疗人类疾病具有明显的实用性。
另外,2021年2月9日,清华大学张强锋,王健伟及丁强共同通讯在Cell 在线发表题为“In vivo structural characterization of the SARS-CoV-2 RNA genome identifies host proteins vulnerable to repurposed drugs”的研究论文,该研究使用icSHAPE技术,确定了SARS-CoV-2 RNA在感染的人细胞中以及从重新折叠的RNA以及SARS-CoV-2和其他六种冠状病毒的调控性非翻译区的结构态势。该研究验证了计算机预测的几种结构元件,并发现了影响细胞中亚基因组病毒RNA的翻译和丰度的结构特征。结构数据提供了一种深度学习工具,可预测与SARS-CoV-2 RNA结合的42种宿主蛋白。引人注目的是,靶向结构元件的反义寡核苷酸和FDA批准的抑制SARS-CoV-2 RNA结合蛋白的药物大大减少了SARS-CoV-2对人细胞的感染。因此,该研究的发现揭示了COVID-19治疗的多种候选疗法。

RNA结合蛋白(RBP)在调节细胞RNA的转录,代谢和翻译中起着至关重要的作用。确定不同条件下的RBP结合谱并阐明其详细的调控机制对于理解其功能至关重要。然而,鉴于RBP的数量庞大,约占人类蛋白质组的10%,因此在RBP及其目标之间建立联系是一个巨大的挑战。
为了解决这个问题,已经开发了许多高通量技术来分析和预测RBP结合。诸如通过指数选择(SELEX),RNAcompete和RNA Bind-n-Seq进行配体的系统进化等方法可以表征RBPs在体外的序列偏好,以及随后的诸如RNA免疫沉淀(RIP)和UV交联的方法通过免疫沉淀(CLIP)和测序可以识别体内RBP结合位点。
除了直接测量的方法外,还开发了其他方法来建模和预测RBP结合。传统上,位置权重矩阵已用于描述RBP结合决定因素并从RNA序列预测RBP结合靶标。还开发了整合不同类型信息的机器学习方法,以更准确地表征RBP的结合模式。最近,深度学习方法已成功应用于模型化蛋白质-RNA相互作用并预测RBP结合位点。
尽管这些学习方法成功捕获了初级序列的RBP结合偏好,但由于RNA序列与体内条件无关,因此它们在不同生理状态下的预测准确性受到限制。多年来,已经开发出了几种方法来在其建模中包括RBP目标的RNA结构特征,但是这些结构是基于计算预测而非体内分析。
在这里,该研究通过确定多种细胞类型中转录组范围的RNA二级结构来弥合这一知识鸿沟。然后,该研究通过使用深度神经网络(PrismNet)进行结构信息化建模,在深度判别性神经网络蛋白质-RNA相互作用的构建中整合此实验衍生的结构信息,该模型可以准确地建模和预测体内RBP目标。该研究应用PrismNet来预测基因组变异如何影响RBP结合,尤其是在人类疾病的背景下。
总之,该研究丰富的分析数据和基于深度学习的预测工具提供了对以前无法访问的细胞类型特异性RBP-RNA相互作用层的访问,并且对于理解和治疗人类疾病具有明显的实用性。
参考消息:
https://www.nature.com/articles/s41422-021-00476-y
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247522250&idx=7&sn=800feae7e7cc26d89662d2cbb5ca24ab
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Cell:首次发现RNA聚合酶III转录的非编码RNA参与自噬调控

新型基因芯片,可快速准确分析RNA表达模式

揭秘细胞外RNA

Cell:流感病毒RNA聚合酶完整的转录周期模型
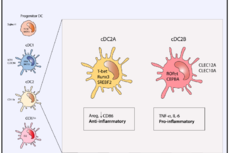
Cell:单细胞分析助力发现新型树突状细胞亚群
细胞外RNA,掀起生物学领域新变革 | “自然展望-细胞外RNA”增刊

人工细胞与生物细胞首次实现成功融合与协作

天价冬虫夏草能否抗癌成“罗生门”
一个小小的细胞就有多达4200万个蛋白质分子

Cell丨CIRTS——RNA编辑新工具