科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2021-02-25
来源:iNature
调节性T细胞(Treg细胞)对于免疫耐受是必不可少的,但在肿瘤微环境中也能促进免疫抑制。因此,针对癌症中Treg细胞的治疗性靶向将需要确定影响其功能的特定环境机制。
2021年2月24日,美国圣裘德儿童研究医院迟洪波团队在Nature 发表题为“Lipid signalling enforces functional specialization of Treg cells in tumours”的研究论文,该研究证明抑制依赖于Treg细胞中固醇调节元素结合蛋白(SREBPs)的脂质合成和代谢信号传导可释放有效的抗肿瘤免疫应答,而无自身免疫毒性。总之,该研究表明代谢重编程可增强Treg细胞在肿瘤中的功能专一性,从而为靶向这些细胞进行癌症治疗提供了新途径。
最后,宾夕法尼亚大学Caroline Perry等人在Nature 在线发表题为“Cancer aided by greasy traitors”的点评文章,系统盘点了该研究。

调节性T细胞(Treg细胞)对于免疫耐受是必不可少的,但在肿瘤微环境中也能促进免疫抑制。因此,针对癌症中Treg细胞的治疗性靶向将需要确定影响其功能的特定环境机制。
在这里,该研究证明抑制依赖于Treg细胞中固醇调节元素结合蛋白(SREBPs)的脂质合成和代谢信号传导可释放有效的抗肿瘤免疫应答,而无自身免疫毒性。该研究发现SREBPs的活性在肿瘤内Treg细胞中被上调。此外,在这些细胞中缺失SREBP裂解激活蛋白(SCAP)(SREBP活性所需的一个因素)可抑制肿瘤生长,并增强针对免疫检查点蛋白PD-1的免疫疗法。SCAP缺失的这些作用与干扰素-γ的不受控制的产生和肿瘤内Treg细胞的功能受损有关。
从机制上讲,通过SCAP和SREBPs进行信号传递可协调这些细胞中脂质合成和抑制性受体信号传递的细胞程序。首先,由脂肪酸合酶(FASN)介导的从头脂肪酸合成有助于Treg细胞的功能成熟,而从Treg细胞中丢失FASN则抑制了肿瘤的生长。其次,肿瘤中的Treg细胞通过依赖于SREBP活性的过程显示出PD-1基因的增强表达,该过程通过甲羟戊酸代谢转化为蛋白geranylgeranyation。阻断PD-1或SREBP信号传导会导致肿瘤内Treg细胞中磷脂酰肌醇3-激酶的活化失调。该研究的发现表明,代谢重编程可增强Treg细胞在肿瘤中的功能专一性,从而为靶向这些细胞进行癌症治疗提供了新途径。
总的来说,该研究结果在肿瘤内Treg细胞中建立了一个代谢检查点,该检查点可增强TME中的功能专门性,并揭示了癌症免疫疗法的新细胞和分子靶标。
来源:Plant_ihuman iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247522293&idx=5&sn=471adf3daf7013bc3ed20f9fe58ebed0
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

Hepatology丨杨鹏远组揭示调控肝癌微环境T细胞免疫耐受新机制
Science子刊:中科院科学家找到癌症免疫耐受新方法!



Treg细胞保护婴儿免受来自母亲的艾滋病毒感染
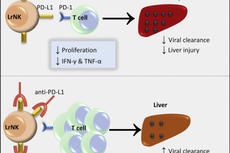
田志刚、彭慧团队《Immunity》发文揭示肝脏定居NK细胞免疫负调功能

周旭宇/高福合作发现核糖体的合成可以选择性控制调节性及常规T细胞的活化
【大师讲堂】免疫耐受是如何产生的?
【大师讲堂】免疫耐受是如何产生的?
微生物所等发现核糖体的合成可以选择性控制调节性及常规T细胞的活化

生物物理所揭示调控肝癌微环境T细胞免疫耐受新机制
【大师讲堂】免疫耐受是如何产生的?