科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2023-07-12
7月4日,《美国国家科学院院刊》(PNAS)在线发表了中国科学院分子细胞科学卓越创新中心许琛琦研究组、生物物理研究所娄继忠课题组,以及浙江大学医学院陈伟课题组合作完成的最新研究成果(Self-programmed dynamics of T cell receptor condensation)。该工作发现了T细胞受体(TCR)通过内置的基于CD3ε/Lck的一套自编程的聚集以及解聚的机制来调控T细胞激活,从相分离的角度阐释了TCR信号通路敏感性以及快速性的分子机制,并进一步丰富了TCR基于Csk的负调控机制。
T细胞是适应性免疫的重要组成部分。TCR复合体作为T细胞膜表面最关键的膜受体,可以识别抗原并介导T细胞激活。TCR复合体有4种CD3信号链(CD3g/d/e/z),共携带20个酪氨酸位点。不同的抗原刺激会引起不同的磷酸化模式,从而产生不同的免疫应答。许琛琦团队致力于T细胞的信号转导及功能调控研究。该团队前期研究发现,在静息状态时,CD3e链和CD3z链的碱性氨基酸富集区(BRS)通过和细胞膜上酸性磷脂发生静电作用,使得ITAM基序被保护起来,免于被下游激酶磷酸化。T细胞活化初期,内流的Ca2+通过中和酸性磷脂所带的负电荷,帮助TCR复合物的胞内段从细胞膜上解离下来,从而发生磷酸化。酪氨酸激酶Lck具有明显的底物选择性,其UD结构域和CD3e链胞内区的BRS序列发生静电相互作用,从而高效介导磷酸化过程。而磷酸化的CD3e链可以通过其ITAM信号基序招募抑制性激酶Csk来负向调控TCR信号强度,使TCR信号能够维持在合适水平。
研究利用体外重组二维膜系统(SLB)对TCR的四种CD3亚基胞内域进行筛选,发现只有CD3ε亚基的胞内域可以与Lck在二维膜上发生相分离。CD3ε亚基胞内域的BRS序列以及Lck的UD结构域对于两者的相分离十分重要。研究通过体外重组液滴以及细胞激活实验发现,相分离不仅增强了CD3ε以及CD3ζ胞内域的磷酸化,而且进一步促进了Lck的激活,且这种自我促进的相分离系统可以帮助T细胞仅凭少量的TCR激活即可快速活化。结合前期数据,研究发现磷酸化的CD3ε可以招募抑制性激酶Csk,而Csk的竞争性结合导致Lck被排出CD3e/Lck相分离。同时,Csk可以使活化的Lck回到非活化状态,进而抑制T细胞的过度活化。
研究工作得到国家自然科学基金、中国科学院战略性先导科技专项(B类)、国家重点研发计划等的支持。浙江大学医学院第一附属医院等的科研人员参与研究。相关荧光成像工作在生物物理所生物成像中心完成。
论文链接
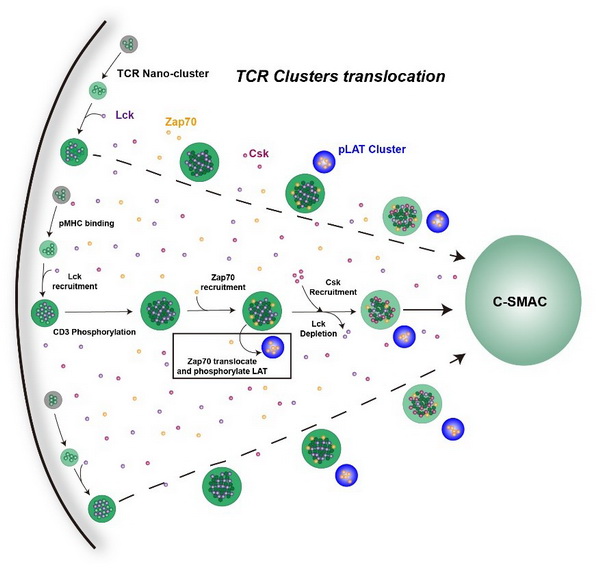
TCR/Lck相分离介导TCR信号转导的模式图
来源:中国科学院
原文链接:http://www.cas.cn/syky/202307/t20230711_4928362.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
《细胞》发文!阿片类药物迎来重大突破

【大师讲堂】诺奖得主Edmond H. Fischer:磷酸化与去磷酸化调控的生物网络

空间蛋白组和磷酸化修饰组联合揭示肝脏内皮细胞全景
从健康细胞到癌细胞,或许只需要几个突变

学术造假必遭严惩,为何仍不断有人冒险
大脑中发现“焦虑细胞”,为治疗焦虑症提供新方向

磷酸化修饰组学揭示新冠肺炎病毒感染肺泡细胞应答机制

于云层和浪花中诞生,生命的起源充满了温柔的诗意

人体细胞内存在“铁路”系统,能自动优化结构
失去细胞核的细胞在3D环境中举步维艰