科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-02-12
来源:BioArt
肿瘤的发生和发展有赖于多种机制,其中很重要的一个方面就是免疫逃逸-躲避免疫系统的识别和消灭。虽然阻断T细胞免疫抑制通路的治疗方法如PD-1/PD-L1抑制剂可以激活适应性免疫系统,并在临床上取得了前所未有的进展,但是目前治疗人群总体响应率仍然不高。其中一个潜在的重要因素是作为免疫系统另一重要分支的先天性免疫系统未能被充分调动起来,因此限制了免疫系统对肿瘤的识别和抑制。
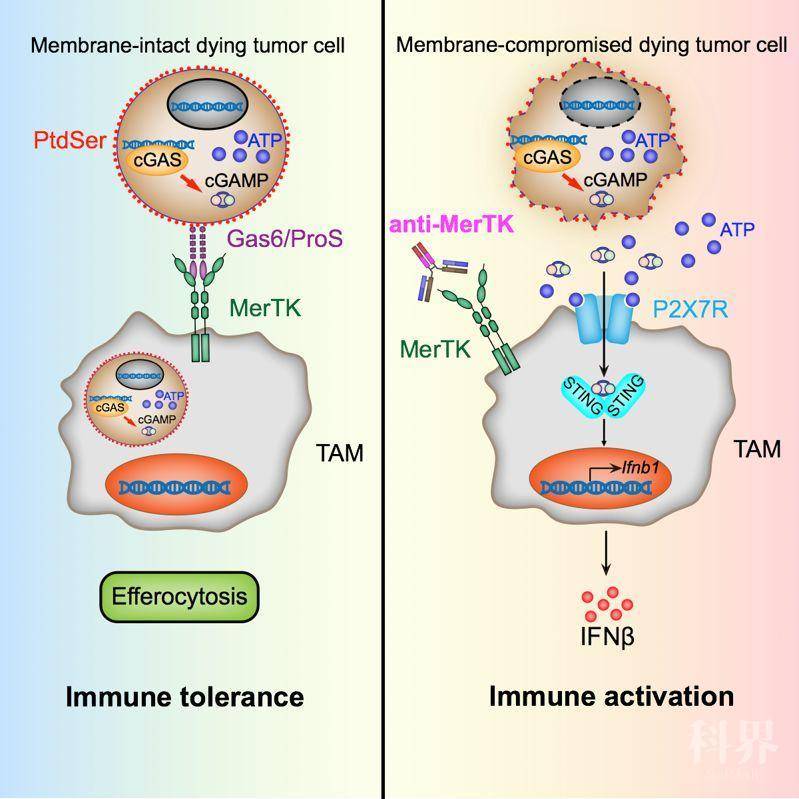
MerTK是在巨噬细胞上表达并具有促进吞噬作用的受体。细胞凋亡时会将磷脂酰丝氨酸(Phosphatidylserine, PtdSer)暴露于细胞表面,MerTK 借助桥梁分子Gas6或Protein S对PtdSer的识别而介导巨噬细胞对凋亡细胞的迅速吞噬和清除, 该过程被称为巨噬细胞的胞葬作用(efferocytosis)。及时而高效清除凋亡细胞防止了损伤相关分子模式 (Damage-Associated Molecular Patterns, DAMPs) 被释放到组织微环境中,确保了所谓的“免疫沉默”,这对于保障正常组织的体内平衡至关重要。同样的,肿瘤在发生和发展过程中很可能利用这一机制,借助肿瘤相关巨噬细胞 (Tumor-Associated Macrophages, TAMs) 来清除凋亡肿瘤细胞,以防止免疫系统对肿瘤的识别,进而消弱针对肿瘤的免疫反应。
2020年2月11日,美国基因泰克Minhong Yan(严民宏)博士团队在Immunity杂志在线发表了题为Blockade of the Phagocytic Receptor MerTK on Tumor-Associated Macrophages Enhances P2X7R-Dependent STING Activation by Tumor-Derived cGAMP 的文章。基因泰克的研究人员们利用特异性功能抗体靶向抑制TAMs上的MerTK,揭示了通过阻断MerTK而增强肿瘤免疫原性和提高抗肿瘤免疫的作用机制及其应用潜力。同时该研究阐明了一种全新的肿瘤微环境中免疫细胞STING信号通路激活的模式。

作者们首先采用一系列体内和体外实验验证了MerTK抗体有效阻断胞葬作用的功能。通过同源小鼠肿瘤实验,作者们发现MerTK抗体治疗会导致凋亡细胞积累,同时在接受治疗的小鼠血浆中能够检测到更多的来自于损伤或死亡细胞的循环肿瘤DNA (ctDNA) 和宿主游离DNA (cfDNA), 表明MerTK抗体确实有效抑制了肿瘤微环境中凋亡细胞的清除。作者们在进一步研究中发现阻断MerTK可以抑制肿瘤生长,而且在不同的小鼠肿瘤模型中MerTK抗体显著增强了PD-1抗体或PD-L1抗体的疗效。当联合使用化疗药物Gemcitabine、PD-1抗体和MerTK抗体时,所有经治疗的小鼠肿瘤几乎完全消失,响应率为100%。
接下来作者们进行了一系列实验来进一步探究阻断MerTK引起的抗肿瘤作用的机制。通过对TAMs进行RNA-seq分析,作者们发现阻断MerTK导致I型干扰素反应特征显著增加,并且该变化仅局限于肿瘤病灶。阻断I型干扰素信号通路导致MerTK抗体的抗肿瘤作用完全丧失,表明诱导I型干扰素的产生是MerTK抗体疗效的一个关键机制。I型干扰素是非常重要的调节免疫反应的细胞因子,能够促进抗原呈递细胞的成熟和功能, 增进T细胞的活化。确实,作者们发现MerTK抗体增加了肿瘤浸润CD8+ T细胞的克隆性和频率,并且提高肿瘤特异性CD8+ T细胞的数量。另外,清除CD8+ T细胞使得MerTK抗体完全丧失了抗肿瘤的功效。
cGAS-STING信号通路是介导I型干扰素产生的一个重要途径,因此如何增强该信号通路也成为研发肿瘤免疫治疗的一个热点。但是目前关于该信号通路在肿瘤中是如何被激活的还是悬而未决、尚无定论。作者们发现MerTK抗体在STING缺失小鼠中全然无效,却能在cGAS敲除小鼠中依然产生I型干扰素反应和抗肿瘤效果。作者们又发现肿瘤细胞中的cGAS对于MerTK抗体的作用至关重要,这些结果表明免疫细胞STING的激活依赖于肿瘤细胞中的cGAS的而非免疫细胞中的cGAS。
cGAS识别胞浆内的双链DNA而被激活,并以ATP和GPT为底物合成cGAMP。作为第二信使的cGAMP结合并激活STING诱导I型干扰素的表达。那么问题在于肿瘤细胞产生的cGAMP是如何抵达免疫细胞的胞浆内并激活STING的?作者们认为MerTK抗体抑制凋亡肿瘤细胞的清除会增加ATP和cGAMP释放到肿瘤微环境中。ATP打开TAMs 上ATP门控的P2X7R离子通道,而促使cGAMP通过P2X7R通道进入TAMs的胞浆内激活STING ,并促进I型干扰素的产生。作者们通过使用P2X7R敲除老鼠,P2X7R 小分子抑制剂 或者过表达CD39(一种降解胞外ATP的酶)的肿瘤细胞进行了一系例研究,其结果有力支持了相关机制。
综上,该研究揭示了一种全新的肿瘤免疫逃逸机制: TAMs通过MerTK依赖性的胞葬作用抑制肿瘤危险信号(比如ATP和cGAMP)的释放以及因此而引起的先天性免疫感知。靶向抑制MerTK这一先天性免疫检查点为增强肿瘤免疫治疗提供了新的机遇。同时,新发现的免疫细胞中ATP-P2X7R-cGAMP-STING机制为设计新一代STING激动剂提供了新的思路。
文章的第一作者为周毅博士(Yi Zhou)和费明健博士(Mingjian Fei)。
原文链接:
https://doi.org/10.1016/j.immuni.2020.01.014
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652480848&idx=1&sn=72b86f90525b0df219d43432f8909b4c&chksm=84e236e4b395bff2a4feb5dc585a61b67c97dd3badadaeeb2ca658ebdc832d23a93328eb2799&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

肿瘤治疗新技术: 不同免疫细胞“组团”,识别多种抗原
Cell:肥胖会抑制免疫细胞的功能,加速肿瘤生长
杀灭病菌肿瘤的免疫细胞竟是脑功能退化元凶



美研究说高剂量手机辐射可致大鼠心脏肿瘤
中国抗癌协会肿瘤介入学专业委员会换届会议召开



ScienceTranslationMedicine:发现肿瘤免疫细胞治疗新策略

全新给药方式可降低癌症复发率

新疗法有助免疫细胞从血管中进入肿瘤 系统根除脑肿瘤

发光纳米颗粒可以更快更精准地检测癌症

新凝胶激活免疫细胞持续攻击肿瘤