科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-02-20
内容来源:人民健康网
近日,西湖大学周强实验室利用冷冻电镜技术,成功解析新冠病毒受体——ACE2的全长结构。这也是西湖大学承担的浙江省新型冠状病毒肺炎防治应急科研攻关任务的重要成果。
新冠肺炎疫情暴发后,武汉病毒研究所的科学家发现,新冠病毒和2003年的SARS病毒一样,也是通过识别ACE2蛋白进入人体细胞的。研究发现,在SARS病毒和新冠病毒侵入人体过程中,ACE2就像是门把手,病毒抓住它,从而打开了进入细胞的大门。
此前,有研究解析出ACE2的一个胞外结构域与SARS病毒S蛋白形成复合物的三维结构。然而,ACE2在细胞膜上以什么状态存在?对比SARS病毒,新冠病毒与ACE2结合有何异同?获取ACE2的全长蛋白及其与S蛋白的复合物结构,将大大有助于解答上述疑问。
作为膜蛋白的ACE2本身很难在体外稳定获得。周强及博士后鄢仁鸿在文献中发现,ACE2与肠道内的一个氨基酸转运蛋白B0AT1能够形成复合物。根据他们过去的研究经验,这个复合物极有可能稳定住ACE2。周强实验室通过共表达的方法获得了ACE2与B0AT1优质稳定的复合物,并利用西湖大学的冷冻电镜平台成功解析了其三维结构,分辨率达到2.9埃,而对于病毒识别至关重要的胞外结构域分辨率为2.7埃。
通过分析ACE2的全长蛋白结构,周强实验室发现ACE2以二聚体形式存在,同时具有开放和关闭两种构象变化,但两种构象均含有与冠状病毒的相互识别界面。这一研究发现,为进一步解析全长ACE2和新冠病毒的S蛋白复合物的三维结构奠定了基础。(记者郑纯胜 通讯员林男)
来源:人民健康网
原文链接:http://health.people.com.cn//n1/2020/0220/c14739-31596486.html
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

ACE2以外的新冠病毒潜在受体发布
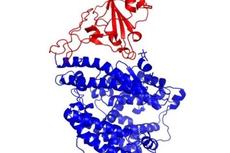
【学术前沿】新冠病毒S蛋白受体结合区域(RBD)与人受体ACE2复合物结构

病毒,不单单是“祸害”

ACE2受体蛋白“纳米气泡”可防治新冠
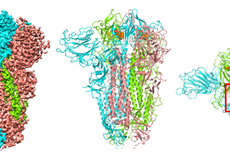
亚油酸能进入口袋阻止S蛋白与ACE2的结合,抑制病毒复制
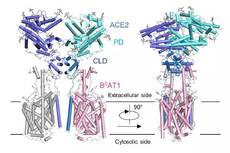
世界首次!西湖大学成功解析出新冠病毒细胞受体ACE2全长结构
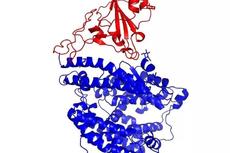
中科院微生物所首次解析新冠病毒S蛋白 RBD与人受体 ACE2 蛋白复合体结构
Science:利用基因相互作用图谱确定蛋白复合物的整体结构
Nature:王新泉/张林琦、李放分别发表新冠病毒与人ACE2受体复合物结构

评论:“坏兔子”病毒闹心,怎样才能将网络恶棍拦在门外