科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-05-03
来源:BioArt
撰文 | 胡小话
有没有考虑过这样一个问题:当你在伸懒腰的时候,被拉伸的组织里紧密排布的细胞会不会因受到挤压而发生损伤?事实上,这种情况通常不会发生。因为细胞内存在一套完整的机械压力的感知与响应系统。科学家们已经鉴定出多个通道蛋白可以协助细胞感知和响应外界机械力的刺激,如Piezo蛋白【1】,以及不久前新发现的TACAN蛋白(详见BioArt报道:Cell∣疼痛如何被感知?)。然而,当存在机械压力时,细胞核,尤其是染色体中的基因组DNA如何避免机械力的损伤,这方面的研究并不多。尽管最近的一些研究工作报道外界微环境来源的机械力可以重塑染色体结构并改变全基因组的表达【2】,但是细胞核是如何消解这些机械压力?染色体又是如何对这些机械压力作出响应?这些关键的科学问题还没有得到回答。
近日,来自芬兰赫尔辛基生命科学研究所的Sara A. Wickstrom教授团队在Cell杂志上发表了题为Heterochromatin-Driven Nuclear Softening Protects the Genome against Mechanical-Stress-Induced Damage的研究,报道了由异染色质驱动的细胞核软化可以保护核DNA免受机械力的损伤,从而揭示了细胞在机械压力下维持基因组稳定的分子机制。

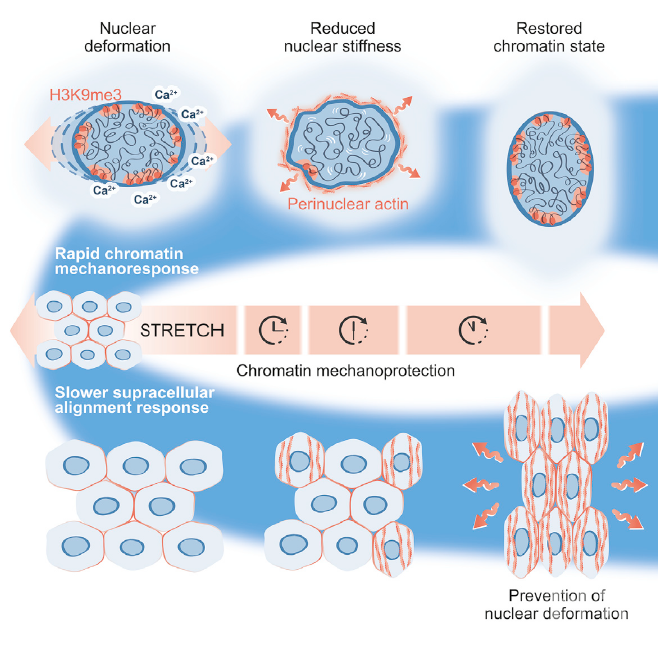
为了探究细胞核如何应对机械压力,作者用单层的皮肤表皮干细胞(EPCs)作为研究对象,并给它施加不同强度的单一方向的拉伸力。作者发现,在不同拉伸强度下,细胞会采取两种完全不同方式去响应外界机械压力:在低拉伸强度下核周围的F-actin会发生多聚化形成actin环进而保护细胞核,而在高拉伸强度下细胞短时间内也会产生actin环但最终会形成超细胞结构共同抵御机械压力。为了区分是什么样的信号传导方式介导了这两种不同的细胞应对模式,作者将细胞在高拉伸强度下分别处理30min和360min,然后进行磷酸化组学分析。其中410个位点磷酸化水平在30min下调但在360min得到回复,通过GO分析,作者发现这类磷酸化位点主要受H3K9me2,3所调控,如laminiaA,B1,B2。而另外一类磷酸化水平始终处于下调的主要与超细胞结构形成的蛋白有关,如adhesion, paxilin。于是,作者去检测了细胞中H3K9me2,3水平,发现H3K9me2,3水平也是在30min下调但在360min恢复正常,并且主要是H3K9me3水平发生了改变。这些结果说明,细胞在不同拉伸强度刺激下会作出不同的响应,而 H3K9me3可能参与调控这一过程。
那么异染色质的H3K9me3是如何调控细胞应对拉伸力呢?为了回答这个问题,作者将这些细胞进行RNA-seq分析。与预期一致的是,拉伸力的确会导致基因组中H3K9me3 的占有率显著下降,但主要集中在非编码区域和染色体的末端,只有少部分在转录区域。为了进一步搞清楚拉伸力如何导致H3K9me3水平的降低,作者又回过头去看磷酸化组学的结果,发现很多下调的磷酸化位点与有丝分裂过程中核膜的消失有关,于是作者把研究方向放到核膜上。果然,细胞在拉伸状态下,核膜出现褶皱,同时伴随着H3K9me3水平的下降。而进一步实验表明核膜出现褶皱原因则是核膜表面张力的降低和细胞核变形能力的增强。接下来,作者想知道异染色体的H3K9me3是否就足以决定细胞核的变形能力。作者发现H3K9me3水平降低是由于拉伸引起的甲基转移酶Suv39H1表达下调所致,而在细胞里过表达Suv39H1会阻碍拉伸引起的H3K9me3下调,进而阻碍细胞核变形,导致DNA损伤的出现。因此,这些结果表明H3K9me3介导了细胞核在应对拉伸时的变形能力,并通过细胞核软化避免对核DNA造成损伤。
那么超细胞结构又是如何影响染色体的机械力传导呢?作者首先通过敲除了α-catenin破坏细胞之间形成超细胞结构的能力,然而α-catenin敲除并不会阻止拉伸引起的H3K9me3下调,但是会阻止H3K9me3在高拉伸强度的回复。由于前面的磷酸化组学结果中出现很多钙调激酶的调控位点,因此作者猜测Ca2+信号是否参与染色体的机械力传导。果然,拉伸状态使得细胞质Ca2+浓度上调,并且用GdCl3抑制Ca2+通道会阻碍拉伸引起的H3K9me3下降与核周围的actin环的形成,但是不会影响超细胞结构的形成。而进一步的实验则表明:细胞感知外界机械力的关键蛋白—Piezo1介导了细胞在发生形变时ER中Ca2+的释放,进而下调H3K9me3水平,促进细胞核的软化。而超细胞结构的形成则会稳定细胞结构,避免机械力传导至细胞核,从而维持染色体的稳定。这也解释了为什么敲除α-catenin 破坏超细胞结构不会影响高拉伸强度引起的异染色质H3K9me3的下降但是会阻止它的回复。
最后,总结一下。Sara A. Wickstrom教授的工作实际上揭示了:当感受到机械压力时,细胞会有两种不同方式去应对机械力的压力去维持基因组的稳定性。第一,细胞自身会迅速响应,使细胞核软化,保护核DNA免受伤害;第二,如果机械力持续存在,单个细胞不足以应付,细胞之间会结成“联盟”,形成超细胞结构去分散机械力,避免机械力传导至细胞核,共同维持染色体结构的稳定。
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652483933&idx=2&sn=6219ee700e50fa41ef5a6009674aeff1&chksm=84e222e9b395abfffdf056fe6081030ef436e7fb37799029ba3726b022f962be33f9d17f94a3#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
《Nature》子刊:具有反常压阻效应的液态金属柔性导电复合材料

研究揭示亚细胞核结构nuclearspeckle在mRNA出核中的功能与机制

CFRP螺栓连接结构在拉伸载荷下损伤过程的声发射

不降低导电性 新型铝线抗拉强度提高50%
失去细胞核的细胞在3D环境中举步维艰

超疏水超疏油的高性能仿壁虎干胶
【科学普及】细胞核起源于病毒?

细胞核中暗藏被忽视的分子机制

CICC科普栏目|打破传统!哈佛大学锁志刚院士团队开发出高韧性、低滞后的可拉伸材料

中国团队发现细胞核内存在病毒DNA识别分子