科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-03-31
来源:BioArt
NLR蛋白(nucleotide-binding domain, leucine repeat domain-containing protein)是胞质内一类模式识别受体(pattern recognition receptors)。该家族成员可在病原性感染或损伤性刺激后激活,引发下游固有免疫通路活化。
NLRP12为NLR家族成员,既往研究已发现NLRP12可在细菌及寄生虫感染后发生活化组成炎症小体,并可下游活化白介素IL-1β及肿瘤坏死因子TNF通路【1-3】。此外,NLRP12参与肠道菌群的调控,可减缓肠道发炎现象,藉此降低结肠炎及相关代谢疾病发生率【4 , 5 】。虽然NLRP12的生理功能与细菌引起的相关发炎反应有关,但关于其如何调控病毒感染后宿主的免疫反应尚不清楚。
近日,“国立阳明大学”陈斯婷博士在Cell Host & Microbe上发表题为NLRP12 Regulates Anti-viral RIG-I Activation via Interaction with TRIM25的研究,首次发现NLRP12可通过TRIM25调控RIG1泛素化修饰,以抑制病毒感染后的干扰素通路活化。

Ⅰ型干扰素是宿主抗病毒免疫的重要的组成。RIG-I (retinoic-acid-inducible gene I ) 属于RLR(RIG-I-like receptor)家族成员,其通过在胞质内感应病毒RNA,启动一连串的下游通路活化,激活Ⅰ型干扰素表达。本研究显示,NLR与RLR两大先天免疫受体家族之间能通过相互调节,影响宿主产生Ⅰ型干扰素的能力。
在RIG-I泛素化修饰调控中,TRIM25 做为一个关键的泛素连接酶,能将RIG-I分子接上Lys63多泛素链,促进RIG-I活化。本研究发现NLRP12能与TRIM25 结合因此减少RIG-I的Lys63泛素化,同时也增加另一泛素连接酶RNF125对RIG-I 的Lys48泛素化修饰,从而影响RIG-I活化并降低了其蛋白水平。
当使用RNA病毒VSV (Vesicular stomatitis virus) 病毒感染后,NLRP12基因表达下调,此时 TRIM25得以释放,可对RIG-1进行修饰完成活化,如同RNA病毒感染的“开关”。研究人员继续利用Nlrp12 基因敲除小鼠及Nlrp12髓系细胞特异性敲除小鼠在病毒感染中进行模型验证,发现敲除小鼠体内具有较高Ⅰ型干扰素及肿瘤坏死因子水平,因此对于病毒感染具有较高的耐受性。

免疫平衡对于维持身体在感染和病理性损伤中扮演着举足轻重的角色。通过寻找免疫系统的“开关”可实现对其的正向和负向调控。本研究显示NLRs家族成员NLRP12在宿主抗病毒感染的过程中扮演RIG-1通路开关的角色,其状态可影响宿主对RNA病毒感染中干扰素通路的响应。
原文链接:
https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(19)30109-X
制版人:半夏
参考文献
[1] Broz P, Dixit V M. Inflammasomes: mechanism of assembly, regulation and signalling[J]. Nat Rev Immunol, 2016, 16(7): 407-20.
[2] Vladimer G I, Weng D, Paquette S W, et al. The NLRP12 inflammasome recognizes Yersinia pestis[J]. Immunity, 2012, 37(1): 96-107.
[3] Ataide M A, Andrade W A, Zamboni D S, et al. Malaria-induced NLRP12/NLRP3-dependent caspase-1 activation mediates inflammation and hypersensitivity to bacterial superinfection[J]. PLoS Pathog, 2014, 10(1): e1003885.
[4] Truax A D, Chen L, Tam J W, et al. The Inhibitory Innate Immune Sensor NLRP12 Maintains a Threshold against Obesity by Regulating Gut Microbiota Homeostasis[J]. Cell Host Microbe, 2018, 24(3): 364-378 e6.
[5] Chen L, Wilson J E, Koenigsknecht M J, et al. NLRP12 attenuates colon inflammation by maintaining colonic microbial diversity and promoting protective commensal bacterial growth[J]. Nat Immunol, 2017, 18(5): 541-551.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652468198&idx=4&sn=d38c94cafff3c8348461031653d8e609&chksm=84e2e052b395694465e8546bbcf96541b1521fa50410bfb179057a1f5b4a20a9192e1d4b6010&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
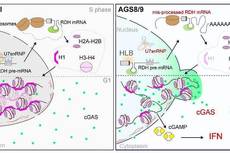
关于cGAS介导的I型干扰素上调的研究
干扰素抗病毒可以更“铁腕”
北大游富平组发表封面文章揭示HIP2K在I型干扰素抗病毒感染中的功能
抗击疫情药物——干扰素的“前世今生”



干扰素协助新冠病毒感染人体,却被用于治疗新冠肺炎

Treg细胞保护婴儿免受来自母亲的艾滋病毒感染
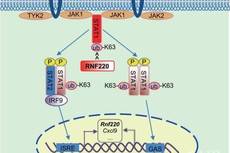
昆明动物所揭示干扰素信号通路的调控新机制
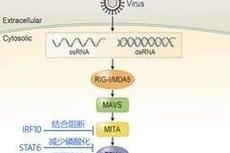
鱼类干扰素的负调控机制研究取得进展

抗病毒战役,不可缺少的经典药物—α干扰素
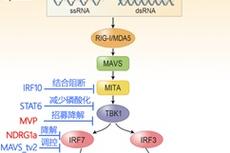
水生所在鱼类干扰素的负调控机制研究中取得进展