科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2019-11-29
来源:BioArt
撰文 | 雪月
利用成年干细胞能够促进受损心脏组织修复。虽然在小鼠中进行的此项实验虽效果一般,但效果稳定。这项研究已经进入临床试验阶段【1】。最开始关于利用成年干细胞能够改善心脏功能机制的研究表明,成年干细胞转分化为新的心肌细胞。但是在随后的研究表明成体干细胞并没有转分化为心肌细胞。利用成年干细胞治疗急性心肌梗塞损伤(MI)或者代偿性心力衰竭的机制也尚不清楚。有些文章提出了旁分泌假说,假设为被移植进入心脏的细胞通过释放一些细胞因子、趋化因子、生长因子等到周围组织中诱导心肌修复,主要促进心脏干细胞激活,心血管形成,抑制凋亡,抑制细胞肥大,并改造细胞外基质【2】。
2019年11月28日,来自美国俄亥俄州辛辛那提儿童医院Jeffery D. Molkentin课题组在Nature上发表了题为“An acute immune response underlines the benefit of cardiac stem-cell therapy”的文章。该文章报道了细胞治疗改善缺血再灌注损伤(I/R injury)的心脏功能主要是由急性无菌免疫反应为基础的伤口愈合反应介导的。移植的细胞招募了CCR2+和CX3CR1+巨噬细胞从而促进改变心脏中成纤维细胞活性,降低细胞外基质含量,促进损伤处的机械性能恢复。

作者重点关注了两类成年干细胞:骨髓来源的单核细胞(MNCs);表达c-kit的心脏间充质细胞,最初又被称为心脏前体细胞(CPCs)。作者将MNCs或者酵母聚糖(一种能够引起天然免疫反应的激动剂)或者生理盐水注射入心脏。通过两周的动态监测发现CD68+的巨噬细胞募集最多,中性粒细胞则无明显区别。接下来作者利用Ccr2-RFP和Cx3cr1-GFP的小鼠对浸润的细胞进一步探索。重复上述注射到这两种工具鼠心脏中。未注射状态下CX3CR1+巨噬细胞在心脏有分布,为CD169+,未检测到CCR2+巨噬细胞。注射后1天CCR2+巨噬细胞聚集在注射部位,而CX3CR1+巨噬细胞分布在注射部位周围。3天达到高峰,7天之后聚集的细胞开始减少,酵母聚糖的效果更持久,这也可能因为酵母聚糖清除较慢。eGFP标记内皮细胞示踪小鼠也发现酵母聚糖促进注射部位内皮细胞数量,细胞注射则没有明显增加。将MNCs CPCs酵母菌素或者生理盐水注射入缺血再灌注损伤的心脏中,前三种注射都能在两周后改善心脏功能。
更进一步分析发现,注射入的细胞确实没有发生转分化。之后作者引入免疫抑制剂环孢霉素A也验证了以上结果。将MNCs注射到CCR2或者CX3CR1敲除的小鼠中,对心功能的改善作用则受到抑制。
研究具体机制发现细胞治疗或者酵母菌素能够抑制细胞外基质含量。并且酵母菌素的注射能够极大的改善心脏的机械力,优于其他方法。体外实验将分离的CCR2+或者CX3CR1+巨噬细胞与心脏成纤维细胞共培养发现CCR2+或者CX3CR1+巨噬细胞能够促进成纤维细胞表达与心脏机械力相关的蛋白的表达(Acta2/αSMA,Lox,Colla2,Ctgf),促进心脏功能恢复。
这一研究表明深入研究目前已有的或者即将进行细胞治疗方法的机制或许能够为找到更好的治疗效果提供一臂之力。
原文链接:
https://doi.org/10.1038/s41586-019-1802-2
参考文献
1. Nguyen PK,Rhee JW, Wu JC. Adult Stem Cell Therapy and Heart Failure, 2000 to 2016: ASystematic Review. JAMA cardiology2016; 1(7): 831-841; doi10.1001/jamacardio.2016.2225.
2. Sanganalmath SK, Bolli R. Cell therapy for heart failure:a comprehensive overview of experimental and clinical studies, currentchallenges, and future directions. Circulationresearch 2013; 113(6): 810-834;doi 10.1161/CIRCRESAHA.113.300219.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652478297&idx=4&sn=61dc93564a27aa6e2aa069508c6b31b8&chksm=84e208edb39581fb3962431baa40f3f2c108153993982e2554965c8e97adf3869a9eeea096fa&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

孙逸仙纪念医院宋尔卫教授团队揭示特殊成纤维细胞亚群调控肿瘤干细胞新机制
我国学者发现炎症巨噬细胞凋亡机制

“基因剪刀”首次让皮肤细胞变身干细胞

硫酸肝素蛋白多糖结合碱性成纤维细胞生长因子促进心肌损伤修复

我们已进入一个移植器官过时的年代

成纤维细胞生长因子受体及相关抗肿瘤 靶向药物的研究进展

Sci Adv:关新元团队发现成纤维细胞帮助肿瘤构建“城墙”抵御免疫攻击

3D迷你大脑,助力脑功能修复研究
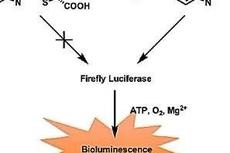
用于成纤维细胞活化蛋白检测的生物发光探针
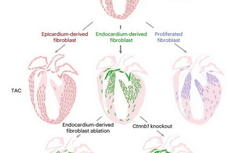
分子细胞卓越中心发现心内膜起源的成纤维细胞调控心脏纤维化