科技工作者之家
科界APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-01-11
来源:BioArt
撰文 | 雪月
肠道神经系统(enteric nervous system, ENS)遍布肠道组织的每个角落,可以将收集到的信息迅速地传递到自体的其他类型的细胞或者肠道定居的微生物,织就一个庞大又复杂的网络系统【1】。最新涌现的多个研究报道发现ENS可以作为免疫系统的感应平台【2】。以前的研究已经深度解析了肠道组织中上皮细胞和免疫系统的相互作用在维护肠道稳态中的重要作用,但是ENS怎么与上皮细胞如何发生联系,媒介是什么,作用方式又是怎样的还未知。
2020年1月9日,耶鲁大学医学院的Richard A. Flavell和Ruaidhrí Jackson联合哈佛医学院的Roni Nowarski在Cell发表了题为Enteric Nervous System-Derived IL-18 Orchestrates Mucosal Barrier Immunity的文章。研究发现ENS神经元分泌IL-18作用于肠道上皮细胞中的杯状细胞,促进杯状细胞抗菌蛋白(antimicrobial protein AMP)的表达,维持肠道稳态。

IL-18是一种促炎细胞因子,在对抗侵入性细菌感染时发挥重要作用。稳态时的上皮细胞高表达IL-18,炎症发生时,髓系细胞则会迅速上调IL-18的表达【3】。然而作者发现特异性敲除免疫细胞或者上皮细胞中的IL-18都不能影响机体对抗肠道受鼠伤寒沙门氏菌(Salmonella typhimurium,S.t.)的侵扰,两种细胞来源的IL-18在炎性状态下对抗细菌中的作用被其他分子所补偿。而上皮来源的IL-18在静息状态下维持肠道组织稳态至关重要。之后作者把目光转向ENS来源的细胞因子。经过一系列染色验证发现结肠组织中的ENS也能够表达IL-18,表达IL-18的神经元大多定位在上皮细胞附近。作者分析了两个公开的单细胞转录组数据集发现ENS所有类型的神经元都能表达IL-18,但是IL-1β的表达丰度远低于IL-18。
接下来作者利用多种工具鼠构建ENS特异性敲除IL-18的小鼠(Il18f/f NesERT+ ;Il1f/fPlp1+肠神经胶质细胞特异性 ;Il18f/fHand2+,Hand2是ENS分化必需的转录因子)和多种细胞类型特异性敲除IL-18R的小鼠(Il18r1f/f NesERT+ ;Il18r1f/fPlp1+ ;Il18r1f/fHand2+; Il18r1f/fFlk1+ ,造血干细胞和内皮细胞特异性; Il18r1f/fVil1+)结合单细胞转录组技术来探究ENS来源IL-18的功能以及作用方式。最终发现ENS特异性来源的IL-18通过IL18R诱导结肠杯状细胞AMP的表达,达到抵抗细菌侵袭的作用。并且IL-18不影响杯状细胞的分化,促进肠蠕动以及产生儿茶酚胺等作用,特异性促进AMP的表达,抑制细菌的浸润和感染。
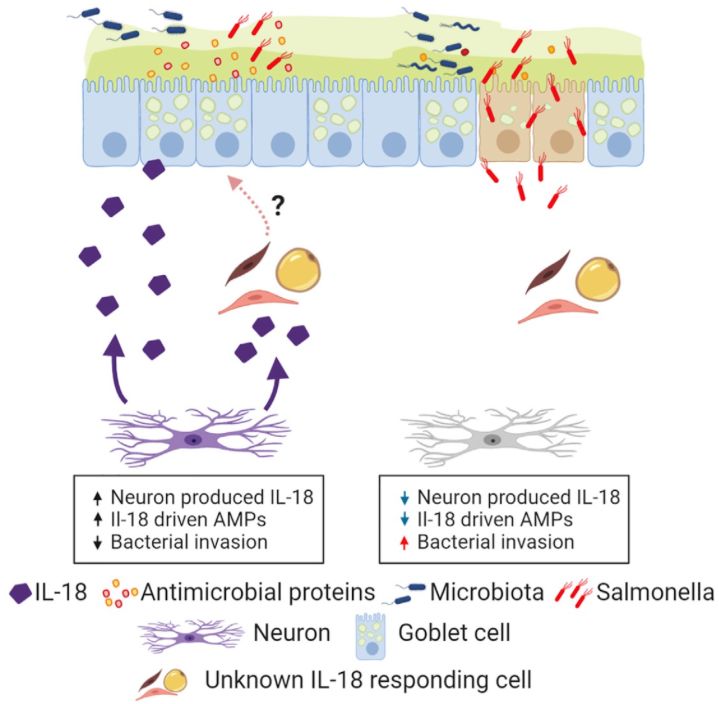
在过去的五年中,对ENS如何调控肠道组织的研究迅速增多。越来越多的研究关注在神经系统和肠道组织其他细胞类型的相互作用。本文首次揭示了ENS能够产生免疫调节因子IL-18,这群特定来源的IL-18驱动结肠杯状细胞分泌AMP,抵抗细菌 入侵。
原文链接:
https://doi.org/10.1016/j.cell.2019.12.016
参考文献
1. Matheis, F., Muller, P.A., Graves, C.L., Gabanyi, I., Kerner, Z.J., Costa-Borges, D., and Mucida, D. (2019). Adrenergic signaling in muscularis macrophages limits neuronal death following enteric infection. bioRxiv. https://doi.org/10.1101/556340.
2. Lai, N.Y., Musser, M.A., Pinho-Ribeiro, F.A., Baral, P., Ma, P., Potts, D.E., Chen, Z., Paik, D., Soualhi, S., Shi, H., et al. (2019). Gut-innervating nociceptor neurons protect against enteric infection by modulating the microbiota and Peyer’s patch microfold cells. bioRxiv. https://doi.org/10.1101/580555.
3. Nowarski, R., Jackson, R., Gagliani, N., de Zoete, M.R., Palm, N.W., Bailis, W., Low, J.S., Harman, C.C., Graham, M., Elinav, E., and Flavell, R.A. (2015). Epithelial IL-18 Equilibrium Controls Barrier Function in Colitis. Cell 163, 1444–1456.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652479820&idx=2&sn=a88ec2e45edf7825f71882e731b26416&chksm=84e232f8b395bbee37618d283ce17c086b01ad324596033ce233c2549faf911f7484bca560d8&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
《细胞》子刊:意义非凡!肠道外援益生菌放大招,延缓帕金森发展 | 肠道君周刊

人工细胞与生物细胞首次实现成功融合与协作

肠道簇细胞内苦味受体可抵御寄生虫
Cell:利用新型肠道上皮细胞培养方法探索肠道炎症损伤与修复机制
禁食促进肠道干细胞再生
科学家发现抑制肠道真菌的免疫细胞

人体细胞内存在“铁路”系统,能自动优化结构
一个小小的细胞就有多达4200万个蛋白质分子

《细胞》:肠道细菌感染会诱使神经细胞“自杀”?

学术造假必遭严惩,为何仍不断有人冒险