科技工作者之家
加好友
科技工作者之家 2021-10-06
因哺乳动物脑组织固有的光散射特征,对活体小鼠进行一定深度和视场的非侵入式(或微损)神经细胞成像目前主要依赖于双光子显微镜。
双光子成像技术所具有的非线性特性可以在无共聚焦条件下,实现高分辨的结构和功能成像。
然而,为了实现更大深度的成像需要增加激光功率,这样会在组织表层产生荧光信号,导致图像的背景噪声增加。
因此,一般情况下小鼠脑组织的非侵入式双光子成像深度被限制在1毫米以内,即通常所说的脑皮层成像。
三光子成像技术利用了更高阶的非线性效应,除了表层组织的背景噪声更小之外,由于采用了更长波长的光子来激发荧光信号,生物组织对激发光的散射减弱,可以实现更大的穿透深度。
之前的研究表明,三光子显微镜可以获得超过1mm深度的脑组织图像。
与双光子成像技术一样,在大深度生物组织成像时,三光子技术同样面临样品不均一性引起的光学像差。
深度增加,像差也随之增加。
再叠加其他不利因素,常规的光学技术难以将激光完全聚焦于深层组织中的精细结构上来获得高解析度的图像。
图1:用于调制光场的变形镜。
可以把他们看作是能随意变形的哈哈镜。
多亏了这面镜子,可以看到大脑深处神经元细胞的清晰图像。
鉴于此,9月30日,欧洲分子生物学实验室(EMBL)与德国海德堡大学共同完成,以“High-resolution structural and functional deep brain imaging using adaptive optics three-photon microscopy”为题在 Nature Methods 报道了一项自适应光学三光子成像显微技术,这一开创性技术将使科学家能够以前所未有的高分辨率捕捉大脑深部神经元的精细细节。
自适应光学最初用于天文学中对天体的观察,利用一个变形镜来补偿大气的光学像差,以获得更清晰的图像。
在显微镜中,研究人员采用类似的方法对组织本身的光学像差进行预补偿,实现对激发光的更高效聚焦(图2)。
图2 自适应光学显微镜原理不同之处在于,这个补偿需要在激光进入样品组织之前进行,类似于把变形镜放置于大气层之外。
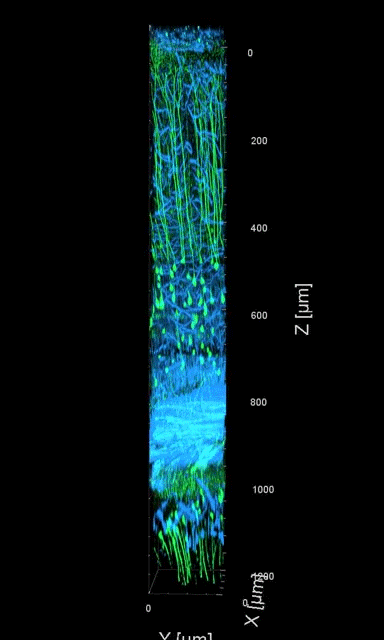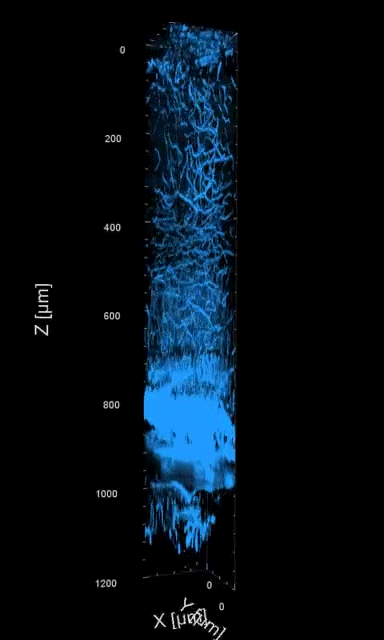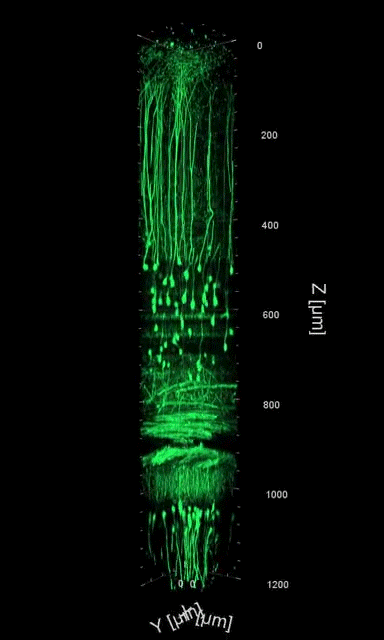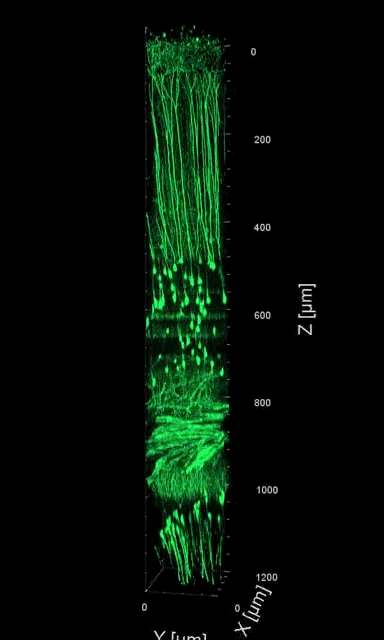
研究团队展示了活体小鼠大脑组织高达1.4mm深度的高分辨三维图像(图3),首次实现了无损状态下海马(大脑中负责记忆)区域中神经元的树突与轴突的高分辨成像,以及纤维状星形胶质细胞的动态功能成像。
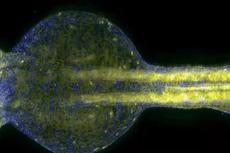
图3 小鼠脑皮层和海马区域的三维图像,青色与绿色分别为三次谐波图像和绿色荧光蛋白标记的神经细胞图像。
这是一项飞跃性的,更先进的,非侵入式的,研究活体组织的显微成像技术。
除了研究脑组织,该技术也可以应用于他生物体组织。
显而易见,该技术将为基于动物实验的疾病和生理学研究扩展出更大的空间。

来源:两江科技评论
原文链接:http://mp.weixin.qq.com/s?__biz=MzU0NDgwMjI0MQ==&mid=2247499671&idx=1&sn=0371ce4dd8aad4d5f88815adccb39294
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
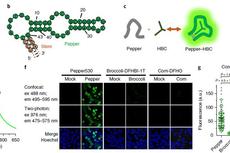
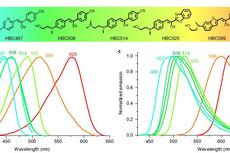
华东理工大学开发拟荧光蛋白RNA ,实现荧光RNA从概念到实用的突破

诺奖得主Martin Chalfie:让绿色荧光蛋白点亮生物学研究之光

徐涛课题组报道新型荧光蛋白

【经典演讲】钱永健教授:荧光蛋白的发现历程

【经典演讲】钱永健教授:荧光蛋白的发现历程

骆利群等利用双钙离子成像同步记录学习过程中不同脑区神经元动态变化
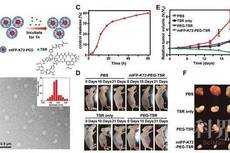
Adv. Mater.:经过工程改造的近红外荧光蛋白组件用于生物成像和治疗
【经典演讲】钱永健教授:荧光蛋白的发现历程
【大师讲堂】诺奖得主Martin Chalfie:绿色荧光蛋白的发展历程
活细胞成像:更深、更快、更宽|Science·职业