科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-29
来源:BioArt
肿瘤中常常含有B细胞和浆细胞【1】,但这些肿瘤内的B细胞的功能和抗原特异性目前仍不清楚。
近日,来自埃默里大学医学院的Rafi Ahmed 和Andreas Wieland合作在Nature杂志发表文章Defining HPV-specific B cell responses in patients with head and neck cancer,在HPV阳性的头颈癌患者的样本中检测到HPV特异性B细胞反应,并且原位检测到HPV特异性IgG抗体。肿瘤微环境中存在HPV特异性抗体分泌细胞(ASCs),而招募来的流感病毒特异性ASCs较少,表明肿瘤微环境中存在局部性抗原特异性ASC反应。HPV特异性ASC反应与血浆中IgG的滴度具有相关性,并且靶向HPV蛋白E2、E6和E7,其中靶向E2的占大多数。利用肿瘤内B细胞和浆细胞产生几种HPV特异性人源单抗,具有高度的体细胞突变的特点,与长期的抗原暴露的特征相一致。单细胞测序显示肿瘤微环境中存在激活的B细胞、生发中心B细胞和ASCs。

研究人员首先收集表达了p16(HPV状态的标记物)的头颈鳞状细胞癌(HNSCC)样本,并在肿瘤样本中检测到HPV基因组DNA。随后在原位肿瘤的肿瘤浸润淋巴细胞(TILs)、转移性肿瘤淋巴结(metLNs)和外周血单核细胞(PBMCs)中定量抗体分泌细胞(ASCs),发现metLNs和TILs中ASCs的数量显著高于PBMCs,且ASCs主要产生IgG类型的抗体,IgA和IgM类型的抗体次之,这与PBMCs中抗体亚型的丰度组成不同。进一步检测发现,metLNs和TILs中IgG+ ASCs能够产生HPV蛋白E2、E6、E7的特异性抗体,且E2特异性抗体反应占据大部分,p16+ HNSCC患者的循环中很容易检测到HPV特异性IgG+记忆B细胞,而p16- HNSCC患者则呈现出减少的淋巴细胞浸润,总的ASCs数量相当但缺乏HPV特异性IgG+ ASCs,且没有HPV特异性IgG+记忆B细胞(MBCs)。在p16+ HNSCC患者的肿瘤微环境(TME)中对比流感病毒和HPV特异性ASCs,发现外周血中流感特异性MBCs明显增高,但TME中HPV特异性ASC占主导地位。即尽管可能会出现一些不相关抗原特异性的激活如流感,但在肿瘤微环境中HPV特异性ASC反应主要是抗原驱动的。检测血浆中E2、E6和E7的IgG抗体滴度,发现p16+ HNSCC明显区别于p16- HNSCC和健康对照,主要由抗HPV E抗原的IgG1组成,IgG3次之,而IgG2和IgG4则没有检测到。此外,HPV特异性IgG的滴度和metLNs中HPV特异性IgG+ ASCs的比例具有相关性。
研究人员利用荧光标记E2蛋白从HPV+ metLNs中纯化分离HPV特异性“激活的B细胞(ABCs)”,随后产生单克隆抗体。约86%的ABCs成功产生识别E2的抗体,且其可变区的重链和轻链展示出高度的体细胞突变特征。从HPV+ HNSCC患者的metLNs和TILs中纯化分离出激活的B细胞进行单细胞RNA测序分析,发现具有4个细胞簇,分别是ABCs、ASCs、生发中心B细胞(GCBs)和过渡细胞,而接种季节性流感疫苗的PBMCs中缺乏GCB和过渡细胞群。即肿瘤微环境中包含几个抗原激活的B细胞亚群,如ABCs、GCBs和ASCs。
从HPV+ HNSCC患者的metLNs和TILs中分离ASCs、ABCs和GCBs,同时利用接种季节性流感的健康受试者的PBMCs的ASCs和ABCs作为对照,进行RNA-seq分析。PCAs分析以及K值聚合分析都显示ASCs、ABCs和GCBs三者基因表达具有差异,不同组织来源之间也具有差异。不考虑组织来源,ASCs不仅高表达常规ASC相关基因XBP1、MZB1、CD27和CD38,低表达B细胞谱系基因如MS4A1、IRF8和CD24,同时高表达浆细胞相关基因如PRDM1、SDC1和CD9。GCBs表达高水平的BCL6、AICDA、MME和S1PR2,促进生发中心的形成。而从PBMCs中分离的流感特异性细胞则不同于肿瘤来源细胞,高表达细胞迁移相关基因如CD52、S1PR4和ITGA3。最后,研究人员利用多重免疫组化染色定位HPV+ HNSCC肿瘤微环境中B细胞和ASCs的位置,发现相比于肿瘤实质区域,总的B细胞和ASCs更多定位于间质。肿瘤间质中激活的B细胞呈高密度,形成ABCs簇,表明肿瘤间质中存在生发中心反应。
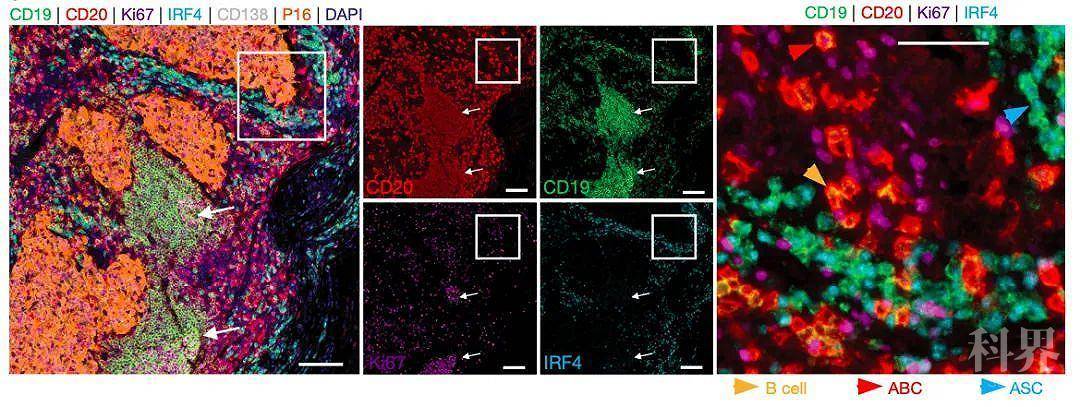 总的来说,该研究对HPV阳性的头颈鳞状细胞癌的肿瘤微环境中的体液免疫进行研究,发现肿瘤微环境中存在HPV特异性激活的B细胞、抗体分泌细胞和生发中心B细胞,即存在HPV特异性B细胞反应,且反应倾向于发生在肿瘤间质而不是肿瘤实质内。该发现有助于加深我们对人类肿瘤微环境中体液免疫的理解,同时提示肿瘤浸润的B细胞或可用于开发治疗药物。
总的来说,该研究对HPV阳性的头颈鳞状细胞癌的肿瘤微环境中的体液免疫进行研究,发现肿瘤微环境中存在HPV特异性激活的B细胞、抗体分泌细胞和生发中心B细胞,即存在HPV特异性B细胞反应,且反应倾向于发生在肿瘤间质而不是肿瘤实质内。该发现有助于加深我们对人类肿瘤微环境中体液免疫的理解,同时提示肿瘤浸润的B细胞或可用于开发治疗药物。
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652511812&idx=5&sn=b59a9c0d8b396474ad2fa45e6be68777
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn
中山大学苏士成团队《Cell》发文揭示补体调控肿瘤相关B细胞的双向作用
Cell :抗体的抗原亲和力影响记忆B细胞和生发中心B细胞的命运决定
嗜碱性粒细胞计数(B)
Nature:三篇文章聚焦B细胞与肿瘤免疫治疗效果的关联
中国抗癌协会肿瘤介入学专业委员会换届会议召开



《细胞》细胞因子风暴会阻止免疫器官的生发中心形成,减少记忆B细胞

蛋白基因组又一力作:揭示头颈部鳞状细胞癌分型及治疗靶标

中年人要担心的不只是油腻,45岁起就该开始结直肠癌筛查

发光纳米颗粒可以更快更精准地检测癌症
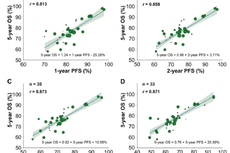
弥漫大B细胞淋巴瘤替代终点研究成果荣登血液肿瘤学顶级期刊《Leukemia》