科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-11-28
来源:生物探索
人类遗传学研究发现了成千上万个基因座的遗传变异与复杂的人类疾病之间的关联。特别是,对基于三重基因的全外显子测序(WES)的分析表明,存在大量的从头丧失功能的变异,这些变异导致了神经发育病理的风险,包括自闭症谱系障碍和神经发育延迟(ASD / ND) 。由于生成和分析单个基因敲除动物模型以进行功能研究的劳动密集型和耗时的性质,因此开发可扩展,通用,高分辨率的表型鉴定组织识别方法至关重要。
2020年11月27日,博德研究所的Paola Arlotta、张锋、Aviv Regev及Xin Jin等在Science 在线发表题为“In vivo Perturb-Seq reveals neuronal and glial abnormalities associated with autism risk genes” 的研究论文,该研究应用了一种可扩展的遗传筛选方法,体内Perturb-Seq,功能上评估了35个自闭症谱系障碍/神经发育延迟(ASD / ND)从头开始丧失功能的风险基因。
使用CRISPR-Cas9,该研究在子宫内发育中的小鼠大脑内的库中的这些风险基因中引入了移码突变,然后对产后大脑中受干扰的细胞进行单细胞RNA测序。该研究从神经元和神经胶质细胞分类中鉴定了细胞类型特异性和进化保守的基因模块。总之,体内Perturb-Seq可以用作大型基因组的系统遗传研究的可扩展工具,以揭示其在复杂组织中单细胞分辨率下的细胞内在功能。
另外,2020年9月16日,张锋团队在新英格兰医学期刊(NEJM)发表题为:Detection of SARS-CoV-2 with SHERLOCK One-Pot Testing 的文章,张锋团队公布了升级版基于SHERLOCK技术的新冠病毒检测流程——STOPCovid.V2。升级版的STOPCovid.V2在原有基础上更进一步,在样本制备的过程中通过加入磁珠富集样本中的RNA,从而通过提高PCR反应的起始RNA数量,进一步提高了STOPCovid.V2的检测灵敏度。此外,2.0版还精简了磁珠富集RNA的操作步骤,去除了乙醇清洗和洗脱过程,让整个RNA富集过程不超过15分钟。最后,研究团队进行了一项双盲检测,对202个新冠病毒阳性和200个新冠病毒阴性鼻咽拭子样本的检测结果表明,STOPCovid.V2能够达到93.1%的灵敏度和98.5%的特异性。且阳性样本只需15-45分钟就能获得结果(点击阅读)。
2020年8月28日,博德研究所张锋团队在Science 在线发表题为“Diverse enzymatic activities mediate antiviral immunity in prokaryotes”的研究论文,该研究通过系统的防御基因预测和异源重组,发现29种广泛的抗病毒基因盒,共同存在于32%的所有已测序细菌和古细菌基因组中,它们介导了针对特定噬菌体的保护。这些系统结合了以前没有参与抗病毒防御的酶促活性,包括RNA编辑和卫星DNA合成逆转录。 此外,该研究在计算上预测了仍有待鉴定的各种其他推定防御基因。这些结果突出了微生物对病毒使用的大量分子功能。该研究对于理解自然微生物种群中的抗病毒抗性和宿主病毒相互作用以及技术应用(例如开发抗菌治疗剂,核酸编辑,分子检测和靶向细胞破坏)具有广泛的意义。
2020年3月17日,博德研究所张锋团队在Molecular Cell 在线发表题为“Highly Parallel Profiling of Cas9 Variant Specificity”的研究论文,该研究该研究描述了基于标签的标签整合位点测序(TTISS)方法,这是一种有效的,可扩展的分析双链断裂(DSB)的方法。该研究将其并行应用于跨59个靶标的8个Cas9变体。此外,该研究生成了成千上万个其他Cas9变体,并筛选了具有增强的特异性和活性的变体,从而确定了LZ3 Cas9,这是一种具有唯一+1插入模式的高特异性变体。总之,这项全面的比较揭示了Cas9活性和特异性之间的一般权衡,并提供了有关+1插入产生频率的信息,这对纠正移码突变具有影响。

https://science.sciencemag.org/content/370/6520/eaaz6063
人类遗传学研究发现了成千上万个基因座的遗传变异与复杂的人类疾病之间的关联。特别是,对基于三重基因的全外显子测序(WES)的分析表明,存在大量的从头丧失功能的变异,这些变异导致了神经发育病理的风险,包括自闭症谱系障碍和神经发育延迟(ASD / ND) 。与通过全基因组关联研究(GWAS)确定的常见变体相比,此类从头风险变体通常具有较大的效应量,高度渗透性,并出现在基因的编码区域内,因此为疾病建模和机制研究提供了关键的切入点。
但是,主要的挑战仍然是确定许多风险基因中每个基因的作用点。例如,ASD / ND包括具有高度异质遗传贡献的神经发育障碍的广泛集合,包括数百种高度渗透的从头风险新变异基因。此外,这些基因编码的基因产物的功能也存在很大差异,从而排除了对大脑发育过程中潜在的脑细胞类型,发育过程和分子途径的明确先验预测。
这些风险基因很少在动物或细胞模型中进行研究,因此,它们在大脑发育过程中的功能仍知之甚少。由于生成和分析单个基因敲除动物模型以进行功能研究的劳动密集型和耗时的性质,因此开发可扩展,通用,高分辨率的表型鉴定组织识别方法至关重要。
为了解决这些挑战,该研究开发了一种可扩展的遗传筛查方法体内Perturb-Seq,以在体内复杂组织中以单细胞分辨率研究大量基因的功能。该研究在小鼠子宫内应用了Perturb-Seq,以研究一组ASD / ND风险基因对大脑发育的影响。该研究应用了一种可扩展的遗传筛选方法,体内Perturb-Seq,功能上评估了35个自闭症谱系障碍/神经发育延迟(ASD / ND)从头开始丧失功能的风险基因。
使用CRISPR-Cas9,该研究在子宫内发育中的小鼠大脑内的库中的这些风险基因中引入了移码突变,然后对产后大脑中受扰动的细胞进行单细胞RNA测序。 该研究从神经元和神经胶质细胞分类中鉴定了细胞类型特异性和进化保守的基因模块。 基因模块和细胞类型在整个扰动中都受到影响,代表了跨ASD / ND风险基因集的关键细胞效应。 体内Perturb-Seq能够研究多样化的突变如何影响发育中生物的细胞类型和状态。
总之,体内Perturb-Seq可以用作大型基因组的系统遗传研究的可扩展工具,以揭示其在复杂组织中单细胞分辨率下的细胞内在功能。
来源:biodiscover 生物探索
原文链接:http://mp.weixin.qq.com/s?__biz=MzU2MTQ2MDE0Ng==&mid=2247522142&idx=3&sn=cc100e903a0a5e89dfa1e855814b982e
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

研究揭示人类小脑功能异质背后的遗传学证据
遗传学:测试与中国男性痛风风险相关的基因变异
遗传学:早期复杂社会通过母系传承权力
中国遗传学会遗传诊断分会成立大会10月27日在上海召开


人类遗传学:让寒冷刺骨的突变基因
第三届全球华人遗传学大会在杭州浙江大学隆重举行


遗传学:关联强迫症的基因
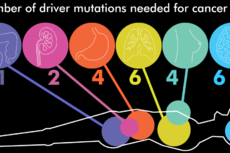
从健康细胞到癌细胞,或许只需要几个突变
光遗传学 & 化学遗传学——打开神经调控的开关
光遗传学: 用光对哺乳动物骨骼肌的首次刺激