科技工作者之家
科技工作者之家APP是专注科技人才,知识分享与人才交流的服务平台。
科技工作者之家 2020-10-30
来源:MedSci梅斯
导语:不同类型的细胞表达不同的细胞表面磷酸酶,RIPR方法有望作为多种激酶特异性受体抑制的工具,为多种疾病的治疗开辟了新的方向。拮抗细胞外受体-配体相互作用的抗体可以抑制细胞表面受体的信号传递,目前广泛应用于包括肿瘤在内的多种疾病的治疗。比如,共受体(如PD-1和CTLA-4)对T细胞信号的调节一直是肿瘤免疫治疗的关键。受体磷酸化受多个过程的调节,包括磷酸酶(如CD45)的反向调节。
抗PD-1抗体有效地阻断了配体激活的信号传导,但它们不抑制持续的细胞内PD-1信号传导,而后者会持续抑制T细胞功能。
2020年10月21日,《Nature》发表了斯坦福大学医学院K. Christopher Garcia团队名为“Immune receptor inhibition through enforced phosphatase recruitment”的研究,该研究发现通过磷酸酶募集抑制受体可增强T细胞活性,并显着小细胞肺癌和结肠腺癌进展。
首先,研究人员用抗CD3ε活化Jurkat T细胞,观察到在没有PD-1的情况下,CD69和CD25上调了约50%。相比之下,PD-1过表达可抑制CD69上调。并且,在PD-1转导的静息Jurkat T细胞中可检测到PD-1磷酸化。
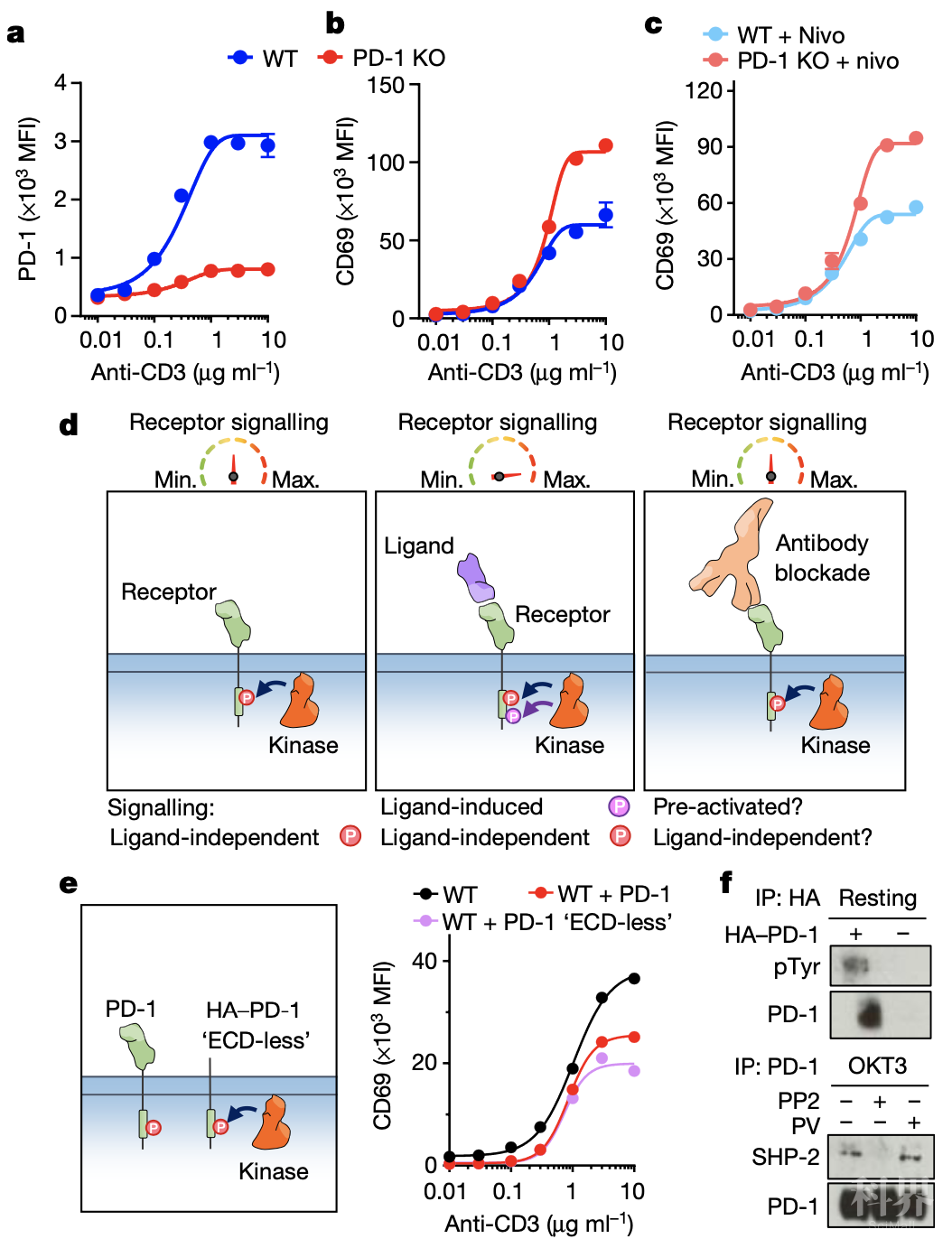
非配体依赖的PD1信号减少T细胞活化
CD45是一种组成型活性细胞表面酪氨酸磷酸酶,并具有较大的细胞外结构域(ECD),可使用抗CD45抗体与双特异性分子选择性结合到PD-1的ECD。研究人员设计了一种可与CD45和PD-1 ECD结合的异质双特异性双价抗体,使PD-1和CD45在T细胞表面顺式结合(RIPR-PD1)。研究结果表明,RIPR-PD1可增强T细胞活化。
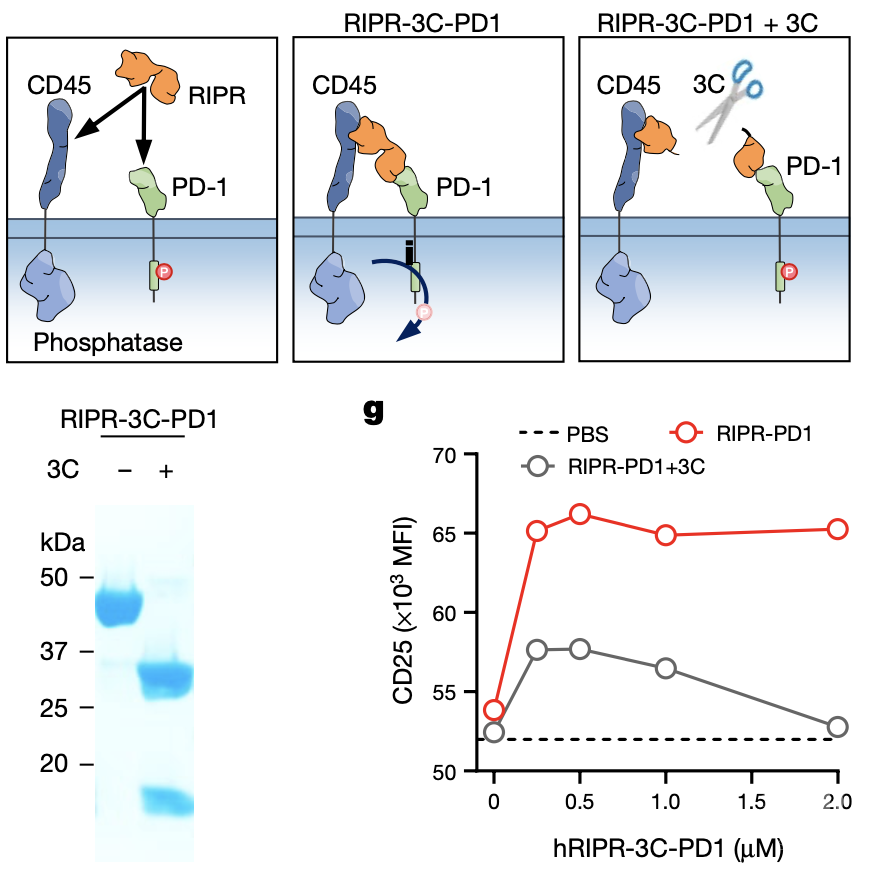
CD45与PD-1的交联可增强T细胞活化
此外,在小细胞肺癌和结肠癌的小鼠模型中,小鼠RIPR-PD1单独或与化疗药物联用可增加肿瘤近端和肿瘤远端淋巴结中效应记忆T细胞的比例,并抑制肿瘤进展。
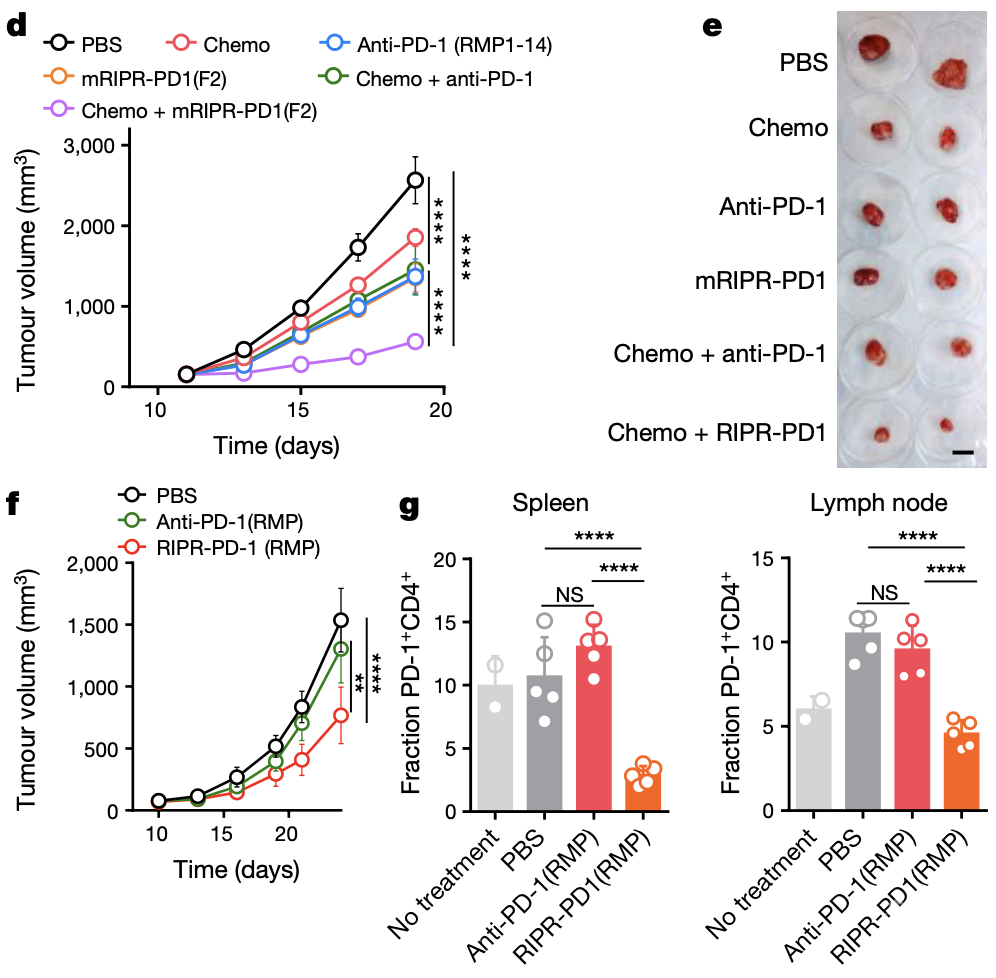
小细胞肺癌和结肠癌的小鼠模型中,小鼠RIPR-PD1可降低肿瘤进展
总而言之,该研究提出了一种减弱细胞表面受体信号的替代方法,称为通过磷酸酶募集(RIPR)抑制受体。另外,研究人员设计了RIPR-PD1,可诱导PD-1与CD45的交联,抑制补体和配体激活的信号传导,在小鼠肿瘤模型中抗肿瘤效果显着。
不同类型的细胞表达不同的细胞表面磷酸酶,RIPR方法有望作为多种激酶特异性受体抑制的工具,为多种疾病的治疗开辟了新的方向。
原始出处:
Ricardo A Fernandes, Leon Su, Yoko Nishiga, et al.Immune receptor inhibition through enforced phosphatase recruitment.Nature. 2020 Oct;586(7831):779-784. doi: 10.1038/s41586-020-2851-2. Epub 2020 Oct 21.
来源:MedSci_cn MedSci梅斯
原文链接:http://mp.weixin.qq.com/s?__biz=MzI0Njc5ODM4MQ==&mid=2247521840&idx=7&sn=2f646461900b9e6c3be9e8453bd254e9&chksm=e9bb1772decc9e648139e9c24d16302377b1390e21b6113d615bfc5ed679cbe46437d00275fc&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

基底细胞癌免疫治疗!赛诺菲/再生元抗PD-1疗法Libtayo展现强劲疗效!
PD-1新用途:纪如荣团队发现PD-1调节吗啡镇痛
中国首部PD-1/PD-L1单抗使用后导致的肺炎诊疗共识发布

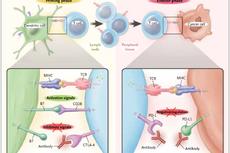

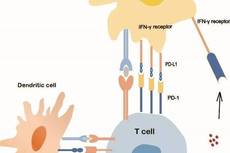
特邀英文综述:PD-1/PD-L1抑制剂治疗肺癌的前景与挑战
研究发现磷酸葡萄糖变位酶1抑制肝癌恶性进展的新机制----中国科学院
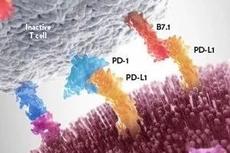
Anti-PD-L1/PD-1治疗失败的元凶原来是外泌体中的PD-L1
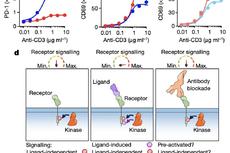
Nature:除了抗PD-1,还可以通过磷酸酶募集来抑制免疫受体
重磅!PD-1/PD-L1抑制剂临床研究趋势要点梳理
抗癌新思路,仁济医院开发新型抑制剂
PD-1/PD-L1抑制剂治疗肺癌的前景与挑战